
 .
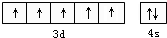
.分析 根據4s能量小于3d,某元素原子3d軌道上有5個電子,則4s能級上肯定有電子,已知M2+離子3d軌道上有5個電子,則M的原子序數是2+8+13+2=25,即M是Mn元素.
(1)根據構造原理可以得出錳原子的外圍電子排布圖;
(2)Mn原子的最外層電子數是2個,最高能級是3d,含有5個電子;
(3)錳元素位于元素周期表的第四周期第ⅦB族.
解答 解:(1)M2+離子3d軌道上有5個電子,則M的原子序數是2+8+13+2=25,即M是Mn元素,原子核外有25個電子,所以核外電子排布式為:1s22s22p63s23p63d54s2,其基態原子的外圍電子排布式為3d54s2 ,錳原子的外圍電子排布圖 ,
,
故答案為: ;
;
(2)Mn元素,原子核外有25個電子,核外電子排布式為:1s22s22p63s23p63d54s2,原子的最外層電子數是2個,4s能量小于3d,最高能級是3d,含有5個電子,
故答案為:2;5;
(3)原子核外電子層數與其周期數相等,錳元素位于元素周期表的第四周期,其基態原子的外圍電子排布式為3d54s2 ,位于第ⅦB族,
故答案為:第四周期、ⅦB族.
點評 本題考查原子核外電子排布,題目難度中等,把握構造原理是解答關鍵,側重考查學生的邏輯推理能力和規范的答題能力.


科目:高中化學 來源: 題型:選擇題
 丙泊酚,其化學名為2,6-雙異丙基苯酚,是目前臨床上普遍用于麻醉誘導、麻醉
丙泊酚,其化學名為2,6-雙異丙基苯酚,是目前臨床上普遍用于麻醉誘導、麻醉| A. | 分子式為C10H20O | |
| B. | 分子中所有碳原子可能在同一平面中 | |
| C. | 該物質的1H核磁共振譜圖中有5個特征峰,峰值強度比大概為:1:1:2:2:12 | |
| D. | 該物質結構中有2個手性碳原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
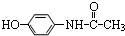 ,則有關它的性質錯誤的是( )
,則有關它的性質錯誤的是( )| A. | 與氫氧化鈉溶液共熱消耗2molNaOH | B. | 能與濃溴水發生取代反應 | ||
| C. | 不能使酸性高錳酸鉀溶液褪色 | D. | 遇三氯化鐵溶液呈現紫色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 短周期元素R、T、Q、W在元素周期表中的相對位置如圖所示,其中T所處的周期序數與族序數相等.下列說法不正確的是( )
短周期元素R、T、Q、W在元素周期表中的相對位置如圖所示,其中T所處的周期序數與族序數相等.下列說法不正確的是( )| A. | 最高價氧化物對應水化物的酸性:Q<W | |
| B. | 最簡單氣態氫化物的熱穩定性:R>Q | |
| C. | 原子半徑:T>Q>R | |
| D. | 含T的鹽溶液一定顯酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 既可以與Br2的CCl4溶液發生加成反應,又可以在光照下與Br2發生取代反應 | |
| B. | 既可以與FeCl3溶液發生顯色反應,又可以與NaHCO3溶液反應放出CO2氣體 | |
| C. | 既可以催化加氫,又可以使酸性KMnO4溶液褪色 | |
| D. | 1 mol該化合物最多可以與3 mol NaOH反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 24Mg32S 晶體中電子總數與中子總數之比為 1:1 | |
| B. | CO2和 PCl5分子中各原子最外層都滿足 8 電子結構 | |
| C. | 若 aXm+ 和 bYn- 兩種離子電子層結構相同,則 a-b=n-m | |
| D. | 元素周期表中第 4 列元素形成的化合物數目最多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗目的或結論 |
| A | SO2通入溴水中,溶液褪色 | 檢驗SO2的漂白性 |
| B | 向2mL淀粉溶液中加入稀硫酸,加熱2min,加入新制Cu(OH)2在加熱,無明顯現象. | 淀粉在酸性條件下不水解 |
| C | 將制得的阿司匹林粗產品與飽和碳酸氫鈉溶液充分反應后過濾 | 除去阿司匹林中的聚合物 |
| D | 等體積、pH同為3的酸A和B分別與足量的Zn反應,酸A放出的氫氣多 | 酸性A比B強 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com