
| A. | 1 mol Na2O2晶體中含有的陰離子數目為2NA | |
| B. | 1 mol Na2O2與足量CO2反應時,轉移2NA個電子 | |
| C. | 1 mol•L-1的NaOH溶液中含Na+數目為NA | |
| D. | 1 mol鈉與足量氧氣反應生成Na2O或Na2O2時,失電子數目均為NA |
分析 A、過氧化鈉由2個鈉離子和1個過氧根構成;
B、過氧化鈉與二氧化碳的反應為歧化反應;
C、溶液體積不明確;
D、鈉反應后變為+1價.
解答 解:A、過氧化鈉由2個鈉離子和1個過氧根構成,故1mol過氧化鈉中含1mol陰離子即NA個,故A錯誤;
B、過氧化鈉與二氧化碳的反應為歧化反應,故1ol過氧化鈉轉移1mol電子即NA個,故B錯誤;
C、溶液體積不明確,故溶液中的鈉離子的個數無法計算,故C錯誤;
D、鈉反應后變為+1價,故1mol金屬鈉反應后失去1mol電子即NA個,與產物種類無關,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
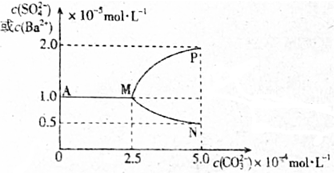
| A. | T℃時Ksp(BaSO4)<Ksp(BaCO3) | |
| B. | 當c(CO32-)大于2.5×10-4mol•L-1時開始有BaCO3沉淀生成 | |
| C. | 圖象中代表沉淀轉化過程中c(Ba2+)隨c(CO32-)變化的曲線是MP | |
| D. | 反應BaSO4(s)+CO32-(aq)?BaCO3(s)+SO42-(aq)的平衡常數K=0.04 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 反應I2(aq)+I-(aq)?I3-(aq)△H<0 | |
| B. | 溫度為T1時,向該平衡體系中加入KI固體,平衡不移動 | |
| C. | 若T1時,反應進行到狀態d時,一定有v正>v逆 | |
| D. | 狀態a與狀態b相比,狀態b時I2的轉化率更低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
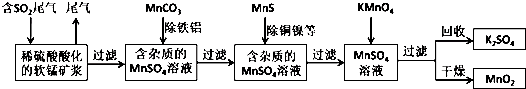
| A. | 高錳酸鉀是氧化劑,Na2O2既是氧化劑,又是還原劑 | |
| B. | 反應的氧化產物只有氧氣 | |
| C. | 當反應產生標準狀況下2.24 L O2 時,反應轉移的電子為0.1mol | |
| D. | 通常所說的酸化的高錳酸鉀溶液是指滴加了濃鹽酸的高錳酸鉀溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “殲-20”飛機上使用的碳纖維是一種新型的有機高分子材料 | |
| B. | 工業上通常用電解Na、Mg、Al對應的氯化物制取該三種金屬單質 | |
| C. | 石油裂解、煤的干餾、玉米制醇、蛋白質的變性和納米銀粒子的聚集都是化學變化 | |
| D. | 燃料電池的燃料都在負極發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 所用HNO3為濃度為10mol/L | B. | NO的體積為6.72升 | ||
| C. | NO2的體積為3.36升 | D. | 被還原的HNO3為1mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | +184.6kJ•mol-1 | B. | -92.3kJ•mol-1 | C. | -69.2kJ•mol-1 | D. | +92.3kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com