
 2NH3.在10s內N2的濃度由5mol/L降至4mol/L下列說法正確的是( )
2NH3.在10s內N2的濃度由5mol/L降至4mol/L下列說法正確的是( )| △c |
| △t |
| 5mol/L-4mol/L |
| 10s |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市青浦區高三上學期期末教學質量調研化學試卷(解析版) 題型:填空題
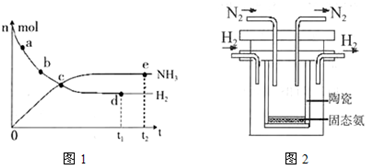
科學家一直致力于“人工固氨”的新方法研究。目前合成氨技術原理為:N2(g) +3H2(g)  2NH3(g)+92.4 kJ/mol673K,30MPa下,上述合成氨反應中n(NH3)和n(H2)隨時間變化的關系如右圖所示。
2NH3(g)+92.4 kJ/mol673K,30MPa下,上述合成氨反應中n(NH3)和n(H2)隨時間變化的關系如右圖所示。

(1)下列敘述正確的是
A.點a的正反應速率比點b的大
B.點c處反應達到平衡
C.點d和點e處的n (N2)相同
D.773K,30MPa 下,反應至t2時刻達到平衡,則n(NH3)比圖中e點的值大
(2)在容積為2.0 L恒容得密閉容器中充入0.80 mol N2(g)和1.60 mol H2(g),673K、30MPa下達到平衡時,NH3的體積分數為20%。該條件下,N2(g)+3H2(g)  2NH3(g)的平衡常數值為:___。
2NH3(g)的平衡常數值為:___。
(3)K值越大,表明反應達到平衡時( )。
A. H2的轉化率一定越高 B.NH3的產量一定越大
C.正反應進行得越完全 D.化學反應速率越大
(4)1998年希臘亞里斯多德大學的兩位科學家采用高質子導電性的SCY陶瓷(能傳遞H+),實現了高溫、常壓下高轉化率的電解合成氨。其實驗裝置如圖。陽極的電極反應為:H2-2e→2H+,則陰極的電極反應為:_____________。

查看答案和解析>>
科目:高中化學 來源:2012-2013學年上海市青浦區高考一模化學試卷(解析版) 題型:填空題
科學家一直致力于“人工固氨”的新方法研究。目前合成氨技術原理為:
N2(g) +3H2(g)  2NH3(g)+92.4 kJ/mol
2NH3(g)+92.4 kJ/mol
673K,30MPa下,上述合成氨反應中n(NH3)和n(H2)隨時間變化的關系如右圖所示。

(1)下列敘述正確的是( )
A.點a的正反應速率比點b的大
B.點c處反應達到平衡
C.點d和點e處的n (N2)相同
D.773K,30MPa 下,反應至t2時刻達到平衡,則n(NH3)比圖中e點的值大
(2)在容積為2.0 L恒容得密閉容器中充入0.80 mol N2(g)和1.60 mol H2(g),673K、30MPa下達到平衡時,NH3的體積分數為20%。該條件下,N2(g)+3H2(g)  2NH3(g)的平衡常數值為:_____________。
2NH3(g)的平衡常數值為:_____________。
(3)K值越大,表明反應達到平衡時( )。
A. H2的轉化率一定越高 B.NH3的產量一定越大
C.正反應進行得越完全 D.化學反應速率越大
(4)1998年希臘亞里斯多德大學的兩位科學家采用高質子導電性的SCY陶瓷(能傳遞H+),實現了高溫、常壓下高轉化率的電解合成氨。其實驗裝置如圖。陽極的電極反應為:H2-2e 2H+,則陰極的電極反應為:_____________。
2H+,則陰極的電極反應為:_____________。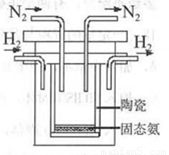
查看答案和解析>>
科目:高中化學 來源:2012年蘇教版高中化學必修2 2.1化學反應速率與反應限度練習卷(解析版) 題型:選擇題
一定的固體硝酸銀置于一容積不變的2L密閉容器中,在一定條件下發生如下反應:2AgNO3(固) 2Ag(固)+2NO2(氣)+O2(氣),2NO2(氣)
2Ag(固)+2NO2(氣)+O2(氣),2NO2(氣) 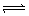 N2O4(氣),2min末,測得固體減重6.2g,且C(NO2)=0.04mol/L,則下列說法正確的是
( )
N2O4(氣),2min末,測得固體減重6.2g,且C(NO2)=0.04mol/L,則下列說法正確的是
( )
A.2min后容器內C(N2O4)=0.04mol/L B.2min內V(O2)= 0.0125mol/(L·min)
C.混合氣體的平均密度為3.1g/L D.混合氣體中NO2的體積分數為11%
查看答案和解析>>
科目:高中化學 來源:同步題 題型:不定項選擇題
 2Ag(固)+2NO2(氣)+O2(氣),2NO2(氣)
2Ag(固)+2NO2(氣)+O2(氣),2NO2(氣) N2O4(氣),2min末,測得固體減重6.2g,且C(NO2)=0.04mol/L,則下列說法正確的是
N2O4(氣),2min末,測得固體減重6.2g,且C(NO2)=0.04mol/L,則下列說法正確的是 查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com