
氨氣是氮循環中的重要物質,在人類的生產和生活中有著廣泛的應用。
(1)如圖是N2與H2反應過程中能量變化的示意圖,則該反應生成液態氨的熱化學方程式是 。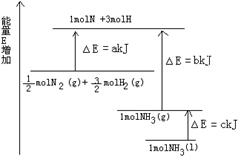
(2)已知:①H2O(g)=H2O(l) ΔH=-Q1 kJ·mol-1
②C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-Q2 kJ/mol ③C2H5OH(g)=C2H5OH(l) ΔH=-Q3 kJ/mol
則23 g液體酒精完全燃燒生成CO2(g)和H2O(l),釋放出的熱量為 kJ(請用Q1、Q2、Q3來表示 )
(1)N2(g) +3H2(g)  2NH3(l) △H=" -2(b+c-a)" kJ/mol(2)(0.5Q2+1.5Q1-Q3)
2NH3(l) △H=" -2(b+c-a)" kJ/mol(2)(0.5Q2+1.5Q1-Q3)
解析試題分析:(1)根據圖示可知:由反應物的能量與生成物的能量的關系可知N2與H2反應生成液態氨的熱化學方程式是N2(g) +3H2(g)  2NH3(l) △H=" -2(b+c-a)" kJ/mol。(2)②-③+3×①整理可得C2H5OH(g)+ 3O2(g)=2CO2(g)+3H2O(l) △H=-(Q2+3Q1-Q3) kJ/mol。1mol的乙醇質量為46g.所以23 g液體酒精即0.5mol完全燃燒生成CO2(g)和H2O(l),釋放出的熱量為(0.5Q2+1.5Q1-Q3)KJ.
2NH3(l) △H=" -2(b+c-a)" kJ/mol。(2)②-③+3×①整理可得C2H5OH(g)+ 3O2(g)=2CO2(g)+3H2O(l) △H=-(Q2+3Q1-Q3) kJ/mol。1mol的乙醇質量為46g.所以23 g液體酒精即0.5mol完全燃燒生成CO2(g)和H2O(l),釋放出的熱量為(0.5Q2+1.5Q1-Q3)KJ.
考點:考查熱化學方程式的書寫及反應熱的計算的知識。


 永乾教育寒假作業快樂假期延邊人民出版社系列答案
永乾教育寒假作業快樂假期延邊人民出版社系列答案科目:高中化學 來源: 題型:填空題
在化學反應中,只有極少數能量比平均能量高得多的反應物分子發生碰撞時才可能發生化學反應,這些分子被稱為活化分子。使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位通常用kJ·mol-1表示。
請認真觀察下圖,然后回答問題。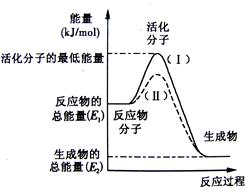
(1)圖中所示反應是 (填“吸熱”或“放熱”)反應,引發該反應時 (填“需要”或“不需要”)加熱,該反應的熱效應的絕對值為
(用含E1、E2的代數式表示)。
(2)已知反應:H2(g)+1/2 O2(g)=H2O(g)的熱效應為為241.8 kJ·mol-1,則其逆反應的活化能為_____kJ·mol-1。
(3)對于同一反應,圖中虛線(Ⅱ)與實線(Ⅰ)相比,活化能大大降低,活化分子百分數增多,反應速率加快,你認為最可能的原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(18分)MnO2和Zn是制造干電池的重要原料,工業上用軟錳礦(主要成分MnO2)和閃鋅礦(主要成分ZnS)聯合生產MnO2和Zn的工藝流程如下圖所示:
(1)操作I用到硅酸鹽材質的儀器有燒杯、玻璃棒和_______ _____(填儀器名稱)。
(2)稀硫酸浸泡時反應的離子方程式為_______________________________________;該反應中若析出19.2g單質A,共轉移____________mo1電子。浸泡時反應速率較慢,下列措施不能提高浸泡時反應速率的是________(填代號)。
a.將礦石粉碎
b.提高浸泡溫度
c.適當增大硫酸濃度
d.改變軟錳礦與閃鋅礦的比例
(3)由硫酸錳溶液可得到固體碳酸錳,然后在空氣中煅燒碳酸錳制備MnO2。已知: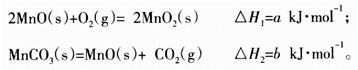
寫出碳酸錳在空氣中煅燒生成MnO2的熱化學方程式_________________________。
(4)用惰性電極電解硫酸酸化的硫酸錳溶液制備MnO2的裝置如下圖所示: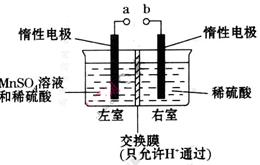
①a應與直流電源的_________(填“正”或“負”)極相連。.
②電解過程中氫離子的作用是______________和_____________;若轉移的電子數為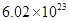 個,左室溶液中
個,左室溶液中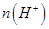 的變化量為________________。
的變化量為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)近幾年來,我國中東部地區陷入嚴重的霧霾天氣,面對全球近期的氣候異常,環境問題再次成為焦點。非金屬氧化物的合理控制和治理是優化我們生存環境的有效途徑之一。請運用化學反應原理知識,回答下列問題:
Ⅰ、目前,消除氮氧化物污染有多種方法。
(1)用CH4催化還原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-57kJ?mol-1
②4CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
③H2O(g)=H2O(l) △H=-44.0kJ?mol-1
寫出CH4(g)與NO2(g)反應生成N2(g),CO2(g)和H2O(l)的熱化學方程式________________。
(2)用活性炭還原法處理氮氧化物。有關反應為:C(s)+ 2NO(g) N2(g)+CO2(g)某研究小組向恒容密閉容器中加入一定量的活性炭和NO,恒溫(T℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:
N2(g)+CO2(g)某研究小組向恒容密閉容器中加入一定量的活性炭和NO,恒溫(T℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:
| 濃度(mol/L) 時間(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分) 氨氣是一種重要的化工原料,工業上用N2和H2合成NH3。現已知N2(g)和H2(g)反應生成1 mol NH3(g)過程中能量變化示意圖如下左圖。回答下列問題: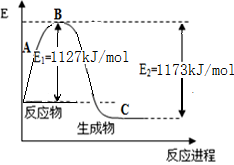
(1)該反應為 (填“吸熱”或“放熱”)反應。
(2)合成氨的熱化學方程式為 。
(3)若又已知鍵能數據如上表,結合以上數據求出N-H鍵鍵能為 kJ/mol。
(4)工業上,以氨氣為原料生產硝酸的第一步為氨催化氧化,請寫出該反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
紅磷P(s)和Cl2(g)發生反應生成PCl3(g)和PCl5(g)。反應過程和能量關系如圖所示( 圖中的△H表示生成1mol產物的數據)。根據圖示,回答下列問題: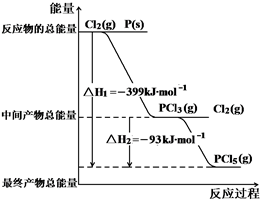
⑴P和Cl2反應生成PCl3(g)的熱化學方程式 。
⑵PCl5(g)分解成PCl3(g)和Cl2的熱化學方程式 。
⑶白磷能自燃,紅磷不能自燃。白磷轉變成紅磷為 (“放”或“吸”) 熱反應。如果用白磷替代紅磷和Cl2反應生成1molPCl5的△H3,則△H3 △H1 (填“<”、“>” 或 “=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以下是一些烷烴的燃燒熱(kJ/mol)數據,回答下列問題:
| 化合物 | 燃燒熱 | 化合物 | 燃燒熱 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1560.8 | 異丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 2-甲基丁烷 | 3 531.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲醇是一種用途廣泛的化工原料。
(1)工業上常用下列兩種反應制備甲醇:
①CO(g) + 2H2(g)  CH3OH(g) ΔH1= -90.1KJ/mol
CH3OH(g) ΔH1= -90.1KJ/mol
②CO2(g)+ 3H2(g)  CH3OH(g) + H2O(l) ΔH2
CH3OH(g) + H2O(l) ΔH2
已知:CO(g)+ H2O (g) = CO2 (g) + H2 (g) ΔH3=-41.1 KJ/mol ③
H2O (l) =H2O (g) ΔH4=+44.0KJ/mol ④
則ΔH2=
(2)實驗室模擬用CO和H2反應來制甲醇。在250℃下,將一定量的CO和H2投入10L的密閉容器中,各物質的物質的量濃度(mol?L-1)變化如下表所示:(前6min沒有改變條件)
| | 2min | 4min | 6min | 8min | … |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知H+(aq)+OH-(aq) H2O(l) ΔH="-57.3" kJ·mol-1,回答下列問題。
H2O(l) ΔH="-57.3" kJ·mol-1,回答下列問題。
(1)用含20 g NaOH的稀溶液跟足量稀鹽酸反應放出 kJ的熱量。
(2)用含2 mol H2SO4的稀溶液跟足量稀NaOH反應,此反應的中和熱為 。
(3)如果將(1)反應中的稀鹽酸換成稀醋酸,反應放出的熱量 (填“大于”“小于”或“等于”)原來(1)放出的熱量。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com