
物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。

請回答下列問題:
(1)寫出下列物質(zhì)的化學式:B 、E 、G ;
(2)利用電解可提純C物質(zhì),在該電解反應中陽極物質(zhì)是 ,陰極物質(zhì)是 ,電解質(zhì)溶液是 ;
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K= 。若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則B的平衡濃度 (填“增大”、“不變”或“減小”),氧氣的轉化率 (填“升高”、“不變”或“降低”),D的體積分數(shù) (填“增大”、“不變”或“減小”)。
(1)SO2 H2SO4 Cu2O
(2) 粗銅 精銅 CuSO4溶液
(3)Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(4)23.8mol-1·L 減小 降低 減小
本題主要結合無機框圖推斷,考查常見無機物之間的相互轉化關系,以及電解原理和化學平衡的移動知識的綜合應用。注重考查考生的邏輯推理能力和綜合運用所學知識靈活作答的能力。磚紅色沉淀G是葡萄糖和新制Cu(OH)2的反應,則G和單質(zhì)C分別為Cu2O和Cu,結合反應①條件可確定B、D分別為SO2、SO3; E和F分別為H2SO4和CuSO4。粗銅電解精煉時,陽極為粗銅,陰極為精銅;可用CuSO4溶液作為電解質(zhì)溶液。(4)中發(fā)生反應為2SO2(g)+O2(g)![]() 2SO3(g),根據(jù)題中數(shù)據(jù),可算出平衡時SO2(g)、O2(g)和SO3(g)的物質(zhì)的量濃度分別為0.11mol/L、0.05mol/L和0.12mol/L,根據(jù) K=
2SO3(g),根據(jù)題中數(shù)據(jù),可算出平衡時SO2(g)、O2(g)和SO3(g)的物質(zhì)的量濃度分別為0.11mol/L、0.05mol/L和0.12mol/L,根據(jù) K=![]() ,帶入數(shù)據(jù)求得K=23.8mol-1·L。平衡后通入O2,可以提高SO2的轉化率,但O2自身轉化率減小,再打到平衡時SO3的體積分數(shù)也會減小。
,帶入數(shù)據(jù)求得K=23.8mol-1·L。平衡后通入O2,可以提高SO2的轉化率,但O2自身轉化率減小,再打到平衡時SO3的體積分數(shù)也會減小。


科目:高中化學 來源:2010年普通高等學校招生全國統(tǒng)一考試理綜化學部分(新課標全國I卷) 題型:填空題
(14分)
物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。
請回答下列問題:
(1)寫出下列物質(zhì)的化學式:B 、E 、G ;
(2)利用電解可提純C物質(zhì),在該電解反應中陽極物質(zhì)是 ,陰極物質(zhì)是 ,電解質(zhì)溶液是 ;
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K= 。若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則B的平衡濃度 (填“增大”、“不變”或“減小”),氧氣的轉化率 (填“升高”、“不變”或“降低”),D的體積分數(shù) (填“增大”、“不變”或“減小”)。
查看答案和解析>>
科目:高中化學 來源:2013屆河南省高二下學期第一次考試化學試卷(解析版) 題型:推斷題
(12分)物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。(提示:葡萄糖結構簡式為CH2OH(CHOH)4CHO )
請回答下列問題:

(1) 寫出下列物質(zhì)的化學式:B 、E 、G
(2)利用電解精煉法可提純C物質(zhì),在該電解反應中陽極電極材料是 ,陰極電極材料是 ,電解質(zhì)溶液是
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K = (保留一位小數(shù))若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則:
B的平衡濃度 (填“增大”、“不變”或“減小”),
氧氣的轉化率 (填“升高”、“不變”或“降低”),
D的體積分數(shù) (填“增大”、“不變”或“減小”)。
查看答案和解析>>
科目:高中化學 來源:2010年普通高等學校招生全國統(tǒng)一考試(課標Ⅰ卷)理綜化學部分全解全析 題型:填空題
(14分)
物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。

請回答下列問題:
(1)寫出下列物質(zhì)的化學式:B 、E 、G ;
(2)利用電解可提純C物質(zhì),在該電解反應中陽極物質(zhì)是 ,陰極物質(zhì)是 ,電解質(zhì)溶液是 ;
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K= 。若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則B的平衡濃度 (填“增大”、“不變”或“減小”),氧氣的轉化率 (填“升高”、“不變”或“降低”),D的體積分數(shù) (填“增大”、“不變”或“減小”)。
查看答案和解析>>
科目:高中化學 來源:2010年普通高等學校招生全國統(tǒng)一考試理綜化學部分(新課標全國I卷) 題型:填空題
(14分)
物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。

請回答下列問題:
(1)寫出下列物質(zhì)的化學式:B 、E 、G ;
(2)利用電解可提純C物質(zhì),在該電解反應中陽極物質(zhì)是 ,陰極物質(zhì)是 ,電解質(zhì)溶液是 ;
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K= 。若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則B的平衡濃度 (填“增大”、“不變”或“減小”),氧氣的轉化率 (填“升高”、“不變”或“降低”),D的體積分數(shù) (填“增大”、“不變”或“減小”)。
查看答案和解析>>
科目:高中化學 來源:2012屆河南省許昌市高二下學期聯(lián)考化學試卷 題型:填空題
(12分)物質(zhì)A~G有下圖所示轉化關系(部分反應物、生成物沒有列出)。其中A為某金屬礦的主要成分,經(jīng)過一系列反應可得到B和C。單質(zhì)C可與E的濃溶液發(fā)生反應,G為磚紅色沉淀。(提示:葡萄糖結構簡式為CH2OH(CHOH)4CHO )
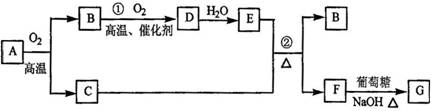
請回答下列問題:
(1) 寫出下列物質(zhì)的化學式:B 、E 、G
(2)利用電解精煉法可提純C物質(zhì),在該電解反應中陽極電極材料是 ,陰極電極材料是 ,電解質(zhì)溶液是
(3)反應②的化學方程式是 。
(4)將0.23 mol B和0.11 mol氧氣放入容積為1 L的密閉容器中,發(fā)生反應①,在一定溫度下,反應達到平衡,得到0.12 mol D,則反應的平衡常數(shù)K = (保留一位小數(shù))若溫度不變,再加入0.50 mol氧氣后重新達到平衡,則:
B的平衡濃度 (填“增大”、“不變”或“減小”),
氧氣的轉化率 (填“升高”、“不變”或“降低”),
D的體積分數(shù) (填“增大”、“不變”或“減小”)。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com