
| A. | 1 L水中溶解了58.5 g NaCl,該溶液的物質的量濃度為1 mol/L | |
| B. | 從1 L 2 mol/L的H2SO4溶液中取出0.5 L,該溶液中氫離子的濃度為2 mol/L | |
| C. | 配制480 mL 0.5 mol/L的CuSO4溶液,需稱取62.5 g膽礬 | |
| D. | 中和100 mL 1mol/L的H2SO4溶液,需NaOH為4 g |
分析 A.所得溶液體積不是1L,則溶液濃度不是1mol/L;
B.2mol/L硫酸溶液中氫離子濃度為4mol/L,氫離子濃度與溶液體積大小無關;
C.配制480mLL 0.5mol/L硫酸銅溶液,實際上配制的是500mL 0.5mol/L的硫酸銅溶液,根據n=cV計算出硫酸銅的物質的量,再根據m=nM計算出需要硫酸銅的質量;
D.根據n=cV計算出硫酸的物質的量,然后根據中和反應實質計算出需要氫氧化鈉的物質的量及質量.
解答 解:A.58.5gNaCl的物質的量為1mol,由于溶液體積不是1L,則溶液濃度不是1mol/L,故A錯誤;
B.2 mol/L的H2SO4溶液中氫離子濃度為4mol/L,溶液具有均一性,取出的0.5 L溶液中氫離子的濃度為4mol/L,故B錯誤;
C.配制480 mL 0.5 mol/L的CuSO4溶液,實際上配制的是500mL 0.5mol/L硫酸銅溶液,需要硫酸銅的物質的量為:0.5mol/L×0.5L=0.25mol,需要膽礬的質量為:250g/mol×0.25mol=6.25g,故C正確;
D.100 mL 1mol/L的H2SO4溶液中含有硫酸的物質的量為:1mol/L×0.1L=0.1L,含有氫離子的物質的量為0.2mol,則需要氫氧化鈉的物質的量為0.2mol,需要氫氧化鈉的質量為:40g/mol×0.2mol=8g,故D錯誤;
故選C.
點評 本題考查了物質的量濃度的相關計算,題目難度不大,明確物質的量濃度與物質的量、摩爾質量之間的關系為解答關鍵,試題得知基礎知識的考查,培養了學生的分析能力及化學計算能力.


 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化學 來源: 題型:選擇題
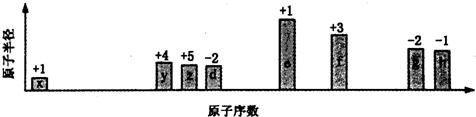
| A. | 離子半徑的大小順序:e>f>g>h | |
| B. | 與x形成簡單化合物的沸點:y>z>d | |
| C. | x、z、d三種元素形成的化合物可能含有離子鍵 | |
| D. | e、f、g、h四種元素對應最高價氧化物的水化物相互之間均能發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SiO3.H2S CO2 | B. | H2O NH3•H2O HClO. | ||
| C. | H2SO3.Ba(OH)2BaSO4 | D. | Cu(OH)2CH3COOH CH3COONa |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
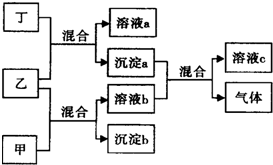 現有四瓶貼有甲、乙、丙、丁標簽的溶液,它們可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液.現進行如下實驗,并記錄部分現象(如圖):
現有四瓶貼有甲、乙、丙、丁標簽的溶液,它們可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液.現進行如下實驗,并記錄部分現象(如圖):查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 172.5 kJ | B. | 1 149 kJ | C. | 283 kJ | D. | 517.5 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com