
①氯化鐵溶液加熱蒸干最終得不到氯化鐵固體
②鐵在潮濕的空氣中容易生銹
③實驗室可用排飽和食鹽水的方法收集氯氣
④常溫下,將1 mL pH=3的醋酸加水稀釋至100 mL,測得其pH<5
⑤鈉與氯化鉀共融制備鉀:Na(l)+KCl(l) K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮與四氧化二氮的平衡體系,加壓后顏色加深
A. ①②③ B. ②⑥ C. ①③④⑤ D. ②⑤⑥
 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源:廣東省2016-2017學年高一上學期期末考試化學試卷 題型:選擇題
下列離子方程式書寫正確的是( )
A. 用FeCl3溶液腐蝕銅線路板:Cu + Fe3+ = Cu2+ + Fe2+
B. Na2O2固體與H2O反應產生O2 :2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑
C. Ba(OH)2溶液中加入稀硫酸 Ba2+ + OHˉ + H+ + SO42-= BaSO4↓+ H2O
D. 向氯化鋁溶液中加入過量的氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O
查看答案和解析>>
科目:高中化學 來源:2017屆陜西省榆林市高考模擬第一次測試理綜化學試卷(解析版) 題型:簡答題
煤的氣化主要反應是煤中碳與水蒸氣反應生成CO、H2等。回答下列問題:
(1)CO與H2分別與O2都可以設計成燃料電池。CO與O2設計成燃料電池(以熔融碳酸鹽為電解質)負極的電極反應為:______________;
(2)在煤的氣化獲得的化工原料氣中含有少量羰基硫(COS),能引起催化劑中毒、大氣污染等。COS的電子式為___________;羰基硫與燒堿溶液反應生成水喝兩種正鹽的離子方程式為:__________;羰基硫的脫硫常用兩種方法,其反應式分別為:
①氫解反應:COS(g) + H2(g) = H2S(g) + CO(g) ΔH1 =+7kJ/mol
②水解反應:COS(g) + H2O(g) = H2S(g) + CO2(g) ΔH2
已知反應中相關的化學鍵鍵能數據如下:
化學鍵 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
鍵能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
則ΔH2 =____________kJ/mol。
(3)脫硫處理后的CO和H2在催化劑作用下合成甲醇:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH2 =-90.14kJ/mol。該反應能自發的理由是_______
CH3OH(g)+H2O(g) ΔH2 =-90.14kJ/mol。該反應能自發的理由是_______
①一定溫度下,在兩個容積都為為VL的恒容莫比容器中,按如下方式加入反應物,一段時間后達到平衡:
容器 | 甲 | 乙 |
反應物投入量 | 1molCO2、3molH2 | a molCO2、3a molH2、 n molCH3OH(g)、n molH2O(g) |
若甲中平衡后氣體的壓強為開始的0.8倍,要使平衡后乙與甲中相同組分的體積分數相等,且起始時維持化學反應向逆反應方向進行,則n的取值范圍為_____________;
②甲容器保持恒容,欲增大H2的平衡轉化率,可采取的措施有:________(答兩點即可)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高二下學期開學考試化學試卷(解析版) 題型:選擇題
在2 L的密閉容器中發生反應xA(g)+yB(g) zC(g)。圖甲表示200 ℃時容器中A、B、C物質的量隨時間的變化,圖乙表示不同溫度下平衡時C的體積分數隨起始n(A)∶n(B)的變化關系。則下列結論正確的是( )。
zC(g)。圖甲表示200 ℃時容器中A、B、C物質的量隨時間的變化,圖乙表示不同溫度下平衡時C的體積分數隨起始n(A)∶n(B)的變化關系。則下列結論正確的是( )。
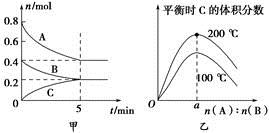
A. 200 ℃時,反應從開始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B. 200℃時,該反應的平衡常數為25 L2/mol2
C. 當外界條件由200℃降溫到100℃,原平衡一定被破壞,且正逆反應速率均增大
D. 由圖乙可知,反應xA(g)+yB(g) zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高二下學期開學考試化學試卷(解析版) 題型:選擇題
已知反應:①101kPa時,C(s) + 1/2O2(g)=CO(g) △H1=-110.5kJ/mol
②稀溶液中,H+(aq) + OH-(aq)=H2O(1) △H2=-57.3kJ/mol
下列結論正確的是( )
A. 若碳的燃燒熱用△H3來表示,則△H3<△H1
B. 若碳的燃燒熱用△H3來表示,則△H3>△H1
C. 濃硫酸與稀NaOH溶液反應的中和熱為57.3kJ/mol
D. 稀醋酸與稀NaOH溶液反應生成1mol水,放出57.3kJ熱量
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高一下學期第一次模塊考試化學試卷(解析版) 題型:計算題
常溫下,將20.0 g質量分數為14.0%的KNO3溶液與30.0 g質量分數為24.0%的KNO3溶液混合,得到的密度為1.15 g/cm3的混合溶液。計算:
(1)混合后溶液的質量分數。
(2)混合后溶液的物質的量濃度。
(3)在1 000 g水中需溶解多少摩爾KNO3才能使其濃度恰好與上述混合后溶液的濃度相等?
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高一下學期第一次模塊考試化學試卷(解析版) 題型:選擇題
將12mol/L的鹽酸(ρ=1.19g/cm3)50mL稀釋成6mol/L的鹽酸(ρ=1.10g/cm3),需加水的體積為( )
A. 50mL B. 50.5mL C. 55mL D. 59.5mL
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省大連市高二上學期期末考試(理)化學試卷(解析版) 題型:簡答題
根據下列電化學裝置,回答下列問題:
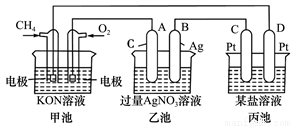
(1)圖中甲、乙池的名稱:甲池是__________裝置,乙池是__________裝置。(填“原電池”或“電解池”)
(2)A(石墨)電極的名稱是____________。
(3)通入CH4一極的電極反應式為___________________________________。
(4)乙池中的電解方程式為___________________________________________。
(5)當乙池中B極的質量增加5.4 g時,甲池中理論上消耗O2_____mL(標準狀況下)。此時丙池某電極析出1.6 g某金屬,則丙池溶液中的溶質可能是___________(填序號)。
A.MgSO4 B.CuSO4 C.Na2SO4
查看答案和解析>>
科目:高中化學 來源:2017屆河南省高三3月高考適應性測試理綜化學試卷(解析版) 題型:選擇題
下列有關實驗操作、現象、解釋或結論都正確的是
選項 | 實驗操作 | 現象 | 解釋或結論 |
A | 充分吸收了Na2SiO3飽和溶液的小木條,瀝干后放在酒精燈外焰加熱 | 小木條不燃燒 | Na2SiO3可作防火劑 |
B | 將H2再充滿Cl2的集氣瓶中燃燒 | 集氣瓶口上方有白煙生成 | H2、Cl2化合生成HCl |
C | 將SO2通入酸性高錳酸鉀溶液中 | 溶液褪色 | SO2具有漂白性 |
D | 出去表面氧化膜的鋁箔,在酒精燈上充分加熱 | 鋁不能滴落下來 | 鋁熔點高,沒能熔化 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com