
【題目】2019年諾貝爾化學獎由來自美、英、日的三人分獲,以表彰他們在鋰離子電池研究方面做出的貢獻,他們最早發明用LiCoO2作離子電池的正極,用聚乙炔作負極。回答下列問題:
(1)基態Co原子價電子排布圖為______________(軌道表達式)。第四電離能I4(Co)比I4(Fe)小,是因為_____________________。
(2)LiCl的熔點(605℃)比LiF的熔點(848℃)低,其原因是_________________________.
(3)乙炔(C2H2)分子中δ鍵與π鍵的數目之比為_______________。
(4)鋰離子電池的導電鹽有LiBF4等,碳酸亞乙酯( )是一種鋰離子電池電解液的添加劑。
)是一種鋰離子電池電解液的添加劑。
①LiBF4中陰離子的空間構型是___________;與該陰離子互為等電子體的分子有_____________。(列一種)
②碳酸亞乙酯分子中碳原子的雜化方式有_______________________。
(5)Li2S是目前正在開發的鋰離子電池的新型固體電解質,其晶胞結構如圖所示,已知晶胞參數a=588pm。

①S2-的配位數為______________。
②設NA為阿伏加德羅常數的值,Li2S的晶胞密度為____________(列出計算式)![]() 。
。
【答案】![]() Co失去的是3d6上的一個電子,而
Co失去的是3d6上的一個電子,而![]() 失去的是半充滿狀態3d5上的一個電子,故
失去的是半充滿狀態3d5上的一個電子,故![]() 需要的能量較高 LiCl和LiF均為離子晶體,Cl-半徑比F-大,LiCl的晶格能比LiF的小 3:2 正四面體 CF4 sp2、sp3 8
需要的能量較高 LiCl和LiF均為離子晶體,Cl-半徑比F-大,LiCl的晶格能比LiF的小 3:2 正四面體 CF4 sp2、sp3 8 ![]()
【解析】
(1)基態Co原子價電子排布式為3d74s2,再得價電子排布圖;Co3+為3d6,Fe3+為3d5,Fe3+半滿,穩定,難失去電子,因此得到結論。
(2)LiCl與LiF都為離子晶體,主要比較離子晶體中離子半徑,鍵能和晶格能。
(3)乙炔(C2H2)分子中碳碳三鍵,因此可得分子δ鍵與π鍵的數目之比。
(4)①先計算LiBF4中陰離子的電子對,再得空間構型,根據左右價電子聯系得出與該陰離子互為等電子體的分子。
②分別分析碳酸亞乙酯分子中每個碳原子的δ鍵和孤對電子得到結論。
(5)①以最右面中心S2-分析,分析左右連接的鋰離子個數。
②先計算晶胞中有幾個硫化鋰,再根據密度公式進行計算。
(1)基態Co原子價電子排布式為3d74s2,其價電子排布圖為![]() ;第四電離能I4(Co)比I4(Fe)小,其Co3+為3d6,Fe3+為3d5,Fe3+半滿,穩定,難失去電子,因此原因為Co失去的是3d6上的一個電子,而
;第四電離能I4(Co)比I4(Fe)小,其Co3+為3d6,Fe3+為3d5,Fe3+半滿,穩定,難失去電子,因此原因為Co失去的是3d6上的一個電子,而![]() 失去的是半充滿狀態3d5上的一個電子,故
失去的是半充滿狀態3d5上的一個電子,故![]() 需要的能量較高,故答案為:
需要的能量較高,故答案為:![]() ;Co失去的是3d6上的一個電子,而
;Co失去的是3d6上的一個電子,而![]() 失去的是半充滿狀態3d5上的一個電子,故
失去的是半充滿狀態3d5上的一個電子,故![]() 需要的能量較高。
需要的能量較高。
(2)LiCl的熔點(605℃)比LiF的熔點(848℃)低,它們都為離子晶體,離子晶體熔點主要比較半徑,鍵能和晶格能,因此其原因是LiCl和LiF均為離子晶體,Cl-半徑比F-大,LiCl的晶格能比LiF的小,故答案為:LiCl和LiF均為離子晶體,Cl-半徑比F-大,LiCl的晶格能比LiF的小。
(3)乙炔(C2H2)分子中碳碳三鍵,因此分子δ鍵與π鍵的數目之比為3:2,故答案為:3:2。
(4)①LiBF4中陰離子的電子對為![]() ,因此空間構型是正四面體型;B-的價電子等于C的價電子,因此與該陰離子互為等電子體的分子有CF4,故答案為:正四面體;CF4。
,因此空間構型是正四面體型;B-的價電子等于C的價電子,因此與該陰離子互為等電子體的分子有CF4,故答案為:正四面體;CF4。
②碳酸亞乙酯分子中碳氧雙鍵的碳原子,δ鍵有3個,沒有孤對電子,因此雜化方式為sp2,另外兩個碳原子,δ鍵有4個,沒有孤對電子,因此雜化方式為sp3,所以碳原子的雜化方式有sp2、sp3,故答案為:sp2、sp3。
(5)①以最右面中心S2-分析,連接左邊有4個鋰離子,右邊的晶胞中也應該有4個鋰離子,因此配位數為8,故答案為:8。
②設NA為阿伏加德羅常數的值,根據晶胞計算鋰離子有8個,硫離子8個頂點算1個,6個面心算3個即總共4個,Li2S的晶胞密度 ,故答案為:
,故答案為:![]() 。
。


科目:高中化學 來源: 題型:
【題目】經X射線研究證明PCl5在固態時,其空間構型分別是正四面體和正八面體的兩種離子構成,下列關于PCl5的推斷正確的是( )
A.PCl5晶體是分子晶體
B.PCl5晶體由[PCl3]2+和[PCl2]2-構成,且離子數目之比為1∶1
C.PCl5晶體由[PCl4]+和[PCl6]-構成,且離子數目之比為1∶1
D.PCl5晶體具有良好的導電性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W、Q、R均為前四周期元素,且原子序數依次增大。其相關信息如下表所示:
X元素的基態原子中電子分布在三個不同的能級中,且每個能級中的電子總數相同 |
Y元素的氣態氫化物與其最高價氧化物對應的水化物能發生化合反應 |
Z元素的族序數是其周期數的三倍 |
W原子的第一至第六電離能分別為:I1=578KJ·mol-1I2=1817KJ·mol-1I3=2745KJ·mol-1 I4=11575KJ·mol-1I5=14830KJ·mol-1I6=18376KJ·mol-1 |
Q為前四周期中電負性最小的元素 |
元素R位于周期表的第10列 |
回答下列問題:
(1)Y元素的基態原子中未成對電子數為______;X、Y、Z三種元素原子的第一電離能由小到大的順序為____________(用元素符號表示)。
(2)W的氯化物的熔點比Q的氯化物的熔點__________(填“高”或“低”),理由是__________________________________________________。
(3)光譜證實元素W的單質與強堿性溶液反應有[W(OH)4]-生成,則[W(OH)4]-中存在(填字母)_____________。
a.極性共價鍵 b.非極性共價鍵 c.配位鍵 d.氫鍵
(4)含有X、R和鎂三種元素的某種晶體具有超導性,其結構如下圖所示。則該晶體的化學式為_______;晶體中每個鎂原子周圍距離最近的R原子有_______個。
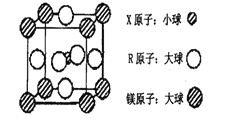
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】恒溫時,將2molA和2molB氣體投入固定容積為2L密閉容器中發生反應:2A(g)+B(g)![]() xC(g)+D(s),10s時,測得A的物質的量為1.7mol,C的反應速率為0.0225mol·L—1·s—1;40s時反應恰好處于平衡狀態,此時B的轉化率為20%。請填寫下列空白:
xC(g)+D(s),10s時,測得A的物質的量為1.7mol,C的反應速率為0.0225mol·L—1·s—1;40s時反應恰好處于平衡狀態,此時B的轉化率為20%。請填寫下列空白:
(1)x=____________
(2)從反應開始到10s,B的平均反應速率為____________
(3)從反應開始到40s達平衡狀態,A的平均反應速率為____________
(4)平衡時容器中B的體積分數為____________
(5)下列各項能表示該反應達到平衡狀態是____________
A.消耗A的物質的量與生成D的物質的量之比為2∶1
B.容器中A、B的物質的量n(A)∶n(B)=2∶1
C.氣體的平均相對分子質量不再變化
D.壓強不再變化
E.氣體密度不再變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將濃度均為0.5molL-1氨水和KOH溶液分別滴入到體積均為20mL且濃度相同的AlCl3溶液中,測得溶液的導電率與加入堿的體積關系如圖所示,下列說法中錯誤的是( )

A.AlCl3溶液的物質的量濃度為0.2molL-1
B.根據圖象可以確定導電率與離子種類有關
C.cd段發生的反應是Al(OH)3+OH-=AlO2-+2H2O
D.e點時溶液中的離子濃度:c(K+) =c(Cl-) +c(AlO2-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中華傳統文化蘊含著很多科學知識,下列說法錯誤的是
A. “丹砂(HgS燒之成水銀,積變又還成丹砂”描述的是可逆反應
B. “水聲冰下咽,沙路雪中平”未涉及化學變化
C. “霾塵積聚難見路人”形容的霾塵中有氣溶膠,具有丁達爾效應
D. “含漿似注甘露缽,好與文園止消渴”說明柑橘糖漿有甜味,可以止渴
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己烯雌酚(結構簡式如圖所示》,是一種激素類藥物。下列敘述正確的是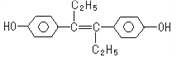
A. 己烯雌酚分子式為C18H12O2
B. 己烯雌酚與NaOH溶液、NaHCO3溶液均能反應
C. 1mol己烯雌酚最多能與4mol溴發生反應
D. 己烯雌酚可以發生加成反應,取代反應、氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T 時,向2.0 L恒容密閉容器中充入1.0 mol PCl5,
反應:PCl5(g)![]() PCl3(g)+Cl2(g)經一段時間后達到平衡,反應過程中測定的部分數據見下表:
PCl3(g)+Cl2(g)經一段時間后達到平衡,反應過程中測定的部分數據見下表:
t/s | 0 | 50 | 150 | 250 | 250 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列說法正確的是
A. 反應在前50 s內的平均速率v(PCl3)=0.0032mol/(L·s)
B. 保持其他條件不變,升高溫度,平衡時c(PCl3)=0.11mol/L,該反應為放熱反應
C. 相同溫度下,起始時向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,達到平衡前的v正>v逆
D. 相同溫度下,起始時向容器中充入2.0 mol PCl3、2.0 mol Cl2,達到平衡時,PCl3的轉化率小于80%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學一選修3:物質結構與性質]
金屬材料在國民經濟建設等領域具有重要應用,鎂、鎳、銅是幾種重要的金屬元素,請回答下列問題:
(1)鎳元素的核電荷數為28,則原子基態電子排布式為 ________ ,結構中有 ___ 種不同形狀的電子云。
(2)MgO的熔點高于CuO的原因是__________________________
(3)Mg元素的第一電離能反常地高于同周期后一種元素,原因是_____________________
(4)Ni與CO能形成配合物Ni(CO)4,該分子中σ鍵與π鍵個數比為 _____________________
(5)配合物[Cu(CH3C≡N)4]BF4中碳原子雜化軌道類型為______ ,BF4-的空間構型為_________________ 。
(6)銅與氧元素可形成如圖所示的晶胞結構,其中Cu均勻地分散在立方體內部,a、b的坐標參數依次為(0,0,0)、(1/2,1/2,1/2),則d的坐標參數為 ____________,已知該品體的密度為ρg/cm3,NA是阿伏加德羅常數值,則晶胞參數為 _______________ cm(列出計算式即可)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com