
若NA表示阿伏加德羅常數的值,下列敘述正確的是 ( )
①標準狀況下,2.24L四氯化碳含碳原子數為0.1NA
②標準狀況下,a L的氧氣和氮氣的混合物含有的分子數為a/22.4 NA
③電解精煉銅時,若陰極得到電子數為2NA個,則陽極質量減少64g
④7g CnH2n中含有的氫原子數為2NA
⑤常溫下,7.1g氯氣與足量的氫氧化鈉溶液反應轉移的電子數為0.1NA
⑥標況下22.4LNO和11.2LO2混合后所得氣體分子數為NA
⑦2L1mol/L的鹽酸中所含氯化氫分子數為2NA
A.①④⑦ B.②⑤⑥ C.③④⑤ D.②⑤
D
【解析】
試題分析:標準狀況下,四氯化碳不是氣態,不能適用于氣體摩爾體積,①錯誤;標準狀況下,a L的氧氣和氮氣的混合物的物質的量是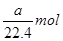 ,②正確;粗銅精練時,陽極最初不是銅失去電子,所以若陰極得到電子數為2NA個,則陽極質量不一定減少64g,③不正確;7g CnH2n中含有的氫原子的物質的量是
,②正確;粗銅精練時,陽極最初不是銅失去電子,所以若陰極得到電子數為2NA個,則陽極質量不一定減少64g,③不正確;7g CnH2n中含有的氫原子的物質的量是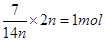 ,④不正確;氯氣和氫氧化鈉溶液的反應中,氯氣既是氧化劑,也是還原劑,轉移1個電子。7.1g氯氣是0.1mol,轉移0.1mol電子,⑤正確;22.4LNO和11.2LO2混合后恰好反應生成22.4LNO2,但NO2和N2O4之間存在可逆反應2NO2
,④不正確;氯氣和氫氧化鈉溶液的反應中,氯氣既是氧化劑,也是還原劑,轉移1個電子。7.1g氯氣是0.1mol,轉移0.1mol電子,⑤正確;22.4LNO和11.2LO2混合后恰好反應生成22.4LNO2,但NO2和N2O4之間存在可逆反應2NO2 N2O4,所以混合后所得氣體分子數小于NA,⑥錯誤;鹽酸溶液中氯化氫是完全電離但,不存在氯化氫分子,⑦不正確,答案選D。
N2O4,所以混合后所得氣體分子數小于NA,⑥錯誤;鹽酸溶液中氯化氫是完全電離但,不存在氯化氫分子,⑦不正確,答案選D。
考點:考查阿伏加德羅常數的有關計算和判斷
點評:阿伏加德羅常數是歷年高考的“熱點”問題,為高考必考題目,這是由于它既考查了學生對物質的量、粒子數、質量、體積等與阿伏加德羅常數關系的理解,又可以涵蓋多角度的化學知識內容。要準確解答好這類題目,一是要掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系;二是要準確弄清分子、原子、原子核內質子中子及核外電子的構成關系。


科目:高中化學 來源: 題型:
| a |
| 22.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com