
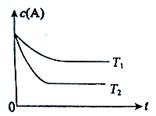
反應A(g) 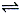 B(g) +C(g)在容積為1.0L的密閉容器中進行,A的初始濃度為0.050mol/L。溫度T1和T2下A的濃度與時間關系如圖所示。回答下列問題:
B(g) +C(g)在容積為1.0L的密閉容器中進行,A的初始濃度為0.050mol/L。溫度T1和T2下A的濃度與時間關系如圖所示。回答下列問題:
(1)上述反應的溫度T1 T2,平衡常數K(T1) K(T2)。(填“大于”、“小于” 或“等于”)
(2)若溫度T2時,5min后反應達到平衡,A的轉化率為70%,則:
①平衡時體系總的物質的量為 。
②反應的平衡常數K= 。
③反應在0~5min區間的平均反應速率v(A)= 。
(1)小于 小于 (2)①0.085mol ②0.082mol/L ③0.007mol/(L·min)
【解析】
(1)圖中顯示,T2時達到平衡所用時間少,反應速率大所以溫度高;而溫度越高c(A)越小,說明升溫反應向正反應方向移動,則正反應為吸熱反應,升溫K將增大。
(2)根據反應: A(g) 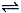 B(g) +C(g)
B(g) +C(g)
反應前:(mol/L) 0.050 0 0
轉化量:(mol/L) 0.035 0.035 0.035
平衡時:(mol/L) 0.015 0.035 0.035
則①平衡時體系總的物質的量為(0.015+0.035+0.035)mol/L×1L=0.085mol。
②反應的平衡常數K=c(B)c(C)/c(A)=(0.035 mol/L)2/0.015 mol/L =0.082mol/L。
反應在0~5min區間的平均反應速率v(A)= (0.035 mol/L)/5min=0.007mol/(L·min)。
【考點定位】本題考查化學反應速率和化學平衡。


科目:高中化學 來源: 題型:
(10分)回答下列問題:
(1)反應A(g)+B(g)![]() C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、
C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、
或“無法確定”)。
(2)在Al2O3、Ni催化下氣態甲酸發生下列反應:
甲酸(g)= CO (g)+ H2O (g) △H1= +34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2= —7.0kJ/mol
則甲酸的分子式為 ,在該條件下,氣態CO2和氣態H2反應生成氣態CO和氣態H2O的熱化學方程式為 。
(3)如圖所示,水槽中試管內有一枚鐵釘,放置數天觀察:
I若試管內液面上升,則正極反應: 。
II若試管內液面下降,則發生 腐蝕。
III若溶液甲為水,溶液乙為海水,則鐵釘在 (填“甲”或“乙”)溶液中腐蝕的速度快。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年福建省龍巖一中高二第二學段(模塊)考試化學試卷 題型:填空題
(10分)回答下列問題:
(1)反應A(g)+B(g) C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、
C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、
或“無法確定”)。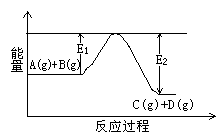
(2)在Al2O3、Ni催化下氣態甲酸發生下列反應:
甲酸(g)=" CO" (g)+ H2O (g) △H1=" +34.0" kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2=" —7.0" kJ/mol
則甲酸的分子式為 ,在該條件下,氣態CO2和氣態H2反應生成氣態CO和氣態H2O的熱化學方程式為 。
(3)如圖所示,水槽中試管內有一枚鐵釘,放置數天觀察:
I若試管內液面上升,則正極反應: 。
II若試管內液面下降,則發生 腐蝕。
III若溶液甲為水,溶液乙為海水,則鐵釘在 (填“甲”或“乙”)溶液中腐蝕的速度快。
查看答案和解析>>
科目:高中化學 來源:2013屆福建省高二第二學段(模塊)考試化學試卷 題型:填空題
(10分)回答下列問題:
(1)反應A(g)+B(g) C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H
0(填“>”、“<”、
C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H
0(填“>”、“<”、
或“無法確定”)。

(2)在Al2O3、Ni催化下氣態甲酸發生下列反應:
甲酸(g)= CO (g)+ H2O (g) △H1= +34.0 kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2= —7.0 kJ/mol
則甲酸的分子式為 ,在該條件下,氣態CO2和氣態H2 反應生成氣態CO和氣態H2O的熱化學方程式為 。
(3)如圖所示,水槽中試管內有一枚鐵釘,放置數天觀察:

I若試管內液面上升,則正極反應: 。
II若試管內液面下降,則發生 腐蝕。
III若溶液甲為水,溶液乙為海水,則鐵釘在 (填“甲”或“乙”)溶液中腐蝕的速度快。
查看答案和解析>>
科目:高中化學 來源:2013屆江西省南北校區高二9月份聯考化學試卷 題型:填空題
(原創題)(8分)反應A(g)+B(g)  C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。
C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。

(1)該反應是__________反應(填“吸熱”“放熱”);
(2)當反應達到平衡時,升高溫度,A的轉化率________
(填“增大”“減小”“不變”)。
(3)在反應體系中加入催化劑,反應速率增大,E1和E2的變化
是:E1_______,E2_______(填“增大”“減小”“不變”)。
(4)已知下列熱化學方程式:
①H2(g) +1/2O2 (g) =H2O(l);ΔH=-285 kJ·mol-1
②H2(g) +1/2O2 (g) =H2O(g);ΔH=-241.8 kJ·mol-1
③C(s) +1/2O2 (g) =CO(g);ΔH=-110.5 kJ·mol-1
④ C(s) +O2 (g) =CO2(g);ΔH=-393.5 kJ·mol-1
回答下列問題:
① 燃燒1gH2生成液態水,放出的熱量為 。
②寫出CO燃燒熱的熱化學方程式 。
查看答案和解析>>
科目:高中化學 來源:0103 期中題 題型:填空題
 C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。
C(g)+D(g)過程中的能量變化如圖所示,回答下列問題。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com