
【題目】CO2可作為合成低碳烯烴的原料加以利用。如:2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1如圖所示為在體積為1 L的恒容容器中,投料為3 mol H2和1 mol CO2時,測得的溫度對CO2的平衡轉化率和催化劑催化效率的影響。
CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1如圖所示為在體積為1 L的恒容容器中,投料為3 mol H2和1 mol CO2時,測得的溫度對CO2的平衡轉化率和催化劑催化效率的影響。

已知:H2和CH2=CH2的標準燃燒熱分別是-285.8 kJ·mol-1和-1411.0 kJ·mol-1。H2O(g) ![]() H2O(l) ΔH=-44 kJ·mol-1
H2O(l) ΔH=-44 kJ·mol-1
請回答:
(1)a=__________kJ·mol-1。
(2)上述由CO2合成CH2=CH2的反應在____________下自發(填“高溫”或“低溫”),理由是____________。
(3)計算250 ℃時該反應平衡常數的數值K=____________。
(4)下列說法正確的是____________。
a.平衡常數大小:M>N
b.反應物活化分子百分數大小:M>N
c.其他條件不變,若不使用催化劑,則250℃時CO2的平衡轉化率可能位于點M1
d.其他條件不變,若投料改為4 mol H2和1 mol CO2時,則250℃時CO2的平衡轉化率可能位于點M2
e.當壓強、混合氣體的密度或n(H2)/n(CO2)不變時均可視為化學反應已達到平衡狀態
(5)保持某溫度(大于100℃)不變,在體積為V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反應物,至t0時達到化學平衡。t1時將容器體積瞬間擴大至2V L并保持不變,t2時重新達平衡。作出容器內混合氣體的平均相對分子質量![]() 隨時間變化的圖像。
隨時間變化的圖像。

【答案】(1)-127.8
(2)低溫;該反應的ΔH<0,ΔS<0(其他合理答案均可)
(3)0.088(或![]() )
)
(4)a、d
(5)如圖,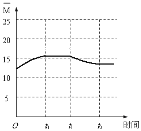 ,起點坐標為(0,12.5),t0達平衡時 應在區間(12.5,20),t2達平衡時 應大于12.5。
,起點坐標為(0,12.5),t0達平衡時 應在區間(12.5,20),t2達平衡時 應大于12.5。
【解析】
試題分析:(1)根據題意(1)①6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)△H1
CH2=CH2(g)+4H2O(g)△H1
②H2(g)+![]() O2(g)=H2O(l)△H2=-285.8kJmol-1
O2(g)=H2O(l)△H2=-285.8kJmol-1
③CH2=CH2(g)+3O2(g)=2CO2(g)+2H2O(l)△H3=-1411kJmol-1
④H2O(g) = H2O(l) ΔH=-44 kJ·mol-1
根據蓋斯定律:②×6-③-④×4=①,則△H1=6△H2-△H3-4△H=-127.8kJmol-1;故答案為:-127.8;
(2)CO2合成CH2=CH2的反應屬于熵減小的反應,根據△G=△S-T△H,反應要自發進行,△G<0,由于△S<0,△H<0,因此低溫自發,故答案為:低溫;該反應的ΔH<0,ΔS<0;
(3) 6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)
CH2=CH2(g)+4H2O(g)
起始(mol)3 1 0 0
反應 1.5 0.5 0.25 1
平衡 1.5 0.5 0.25 1
平衡常數K=![]() =
=![]() =
=![]() ,故答案為:
,故答案為:![]() ;
;
(4)a.該反應放熱,溫度升高,平衡逆向移動,平衡常數減小,平衡常數大小:M>N,正確;b.溫度越高,活化分子百分數越大,活化分子百分數M<N,錯誤;c.催化劑對化學平衡沒有影響,CO2的平衡轉化率不變,錯誤;d.其他條件不變,若投料改為4 mol H2和1 mol CO2時,相當于充入氫氣,平衡右移,CO2的平衡轉化率增大,正確;e.混合氣體的密度始終不變,不能說明化學反應已達到平衡狀態,錯誤。故選a、d;
(5)保持某溫度(大于100℃)不變,在體積為V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反應物,至t0時達到化學平衡。起始![]() =
=![]() =12.5,隨著反應的進行,物質的量減小,
=12.5,隨著反應的進行,物質的量減小,![]() 增大,t0達到化學平衡時,
增大,t0達到化學平衡時,![]() =
= ![]() =15.38,t1時將容器體積瞬間擴大至2V L并保持不變,相當于減小壓強,平衡逆向移動,氣體的物質的量增大,
=15.38,t1時將容器體積瞬間擴大至2V L并保持不變,相當于減小壓強,平衡逆向移動,氣體的物質的量增大,![]() 減小,但大于12.5,因此圖像大致為
減小,但大于12.5,因此圖像大致為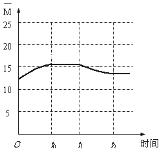 ,故答案為:
,故答案為:


科目:高中化學 來源: 題型:
【題目】反-2-己烯醛(D)是一種重要的合成香料,下列合成路線是制備D的方法之一。根據該合成路線回答下列問題:

已知:
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名稱是__________;B分子中共面原子數目最多為__________;C分子中與環相連的三個基團中,不同化學環境的氫原子共有__________種。
(2)D中含氧官能團的名稱是__________,寫出檢驗該官能團的化學反應方程式:__________。
(3)E為有機物,能發生的反應有__________。
a.聚合反應b.加成反應c.消去反應d.取代反應
(4)B的同分異構體F與B有完全相同的官能團,寫出F所有可能的結構:________。
(5)以D為主要原料制備己醛(目標化合物),在方框中將合成路線的后半部分補充完整。

(6)問題(5)的合成路線中第一步反應的目的是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期X、Y、Z、W四種元素在元素周期表中位置如圖所示。有關表述正確的是( )

A. X、Y、W的最高價氧化物對應水化物均屬強酸
B. Y的氫化物能與Y的最高價氧化物對應水化物反應
C. 原子半徑從大到小依次為X>Z>Y>W
D. Z的氫化物的沸點低于W的氫化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】t℃時Ag2CrO4在水中的沉淀溶解平衡曲線如圖所示。下列說法正確的是( )

A.加熱蒸發飽和Ag2CrO4溶液再恢復到t℃,可使溶液由Y點變到Z點
B.在X點沒有Ag2CrO4沉淀生成,則此時溫度低于t℃
C.向飽和Ag2CrO4溶液中加入少量AgNO3固體,可使溶液由Z點到Y點
D.在t℃時,Ag2CrO4的Ksp為1×10-9
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知鋅能溶解在NaOH溶液中,產生H2。某同學據此設計了測定鍍鋅鐵皮鍍層厚度的實驗方案:將單側面積為S、質量為m1的鍍鋅鐵皮與石墨用導線相連,放入6 mol.L-1 NaOH溶液中,當石墨棒上不再有氣泡產生時,取出鐵片,用水沖洗、烘干后稱量,質量為m2。下列說法正確的是( )
A.設鋅鍍層厚度為h,鋅的密度為ρ,則h=(m1-m2)/( ρS)
B.鋅電極的電極反應式為 2H2O + 2e- = H2 + 2OH-
C.鋅和石墨在堿溶液中形成原電池,外電路中電流從鋅流向石墨
D.當石墨上不再有氣泡時,立即取出鐵皮,沖洗后用酒精燈加熱烘干,鐵片可能部分被氧化導致實驗結果偏低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠礬(FeSO47H2O)是治療缺鐵性貧血藥品的重要成分。下面是以市售鐵屑(含少量錫、氧化鐵等雜質)為原料生產純凈綠礬的一種方法:

查詢資料,得有關物質的數據如下表:

(1)操作Ⅱ中,通入硫化氫至飽和的目的是______________;在溶液中用硫酸酸化至pH=2的目的是______________。
(2)濾渣Ⅱ的主要成分是______________。
(3)操作IV得到的綠礬晶體用少量冰水洗滌,其目的是:①除去晶體表面附著的硫酸等雜質;②______________。
(4)測定綠礬產品中Fe2+含量的方法是:a.稱取2.850g綠礬產品,溶解,在250mL容量瓶中定容;b.量取25.00mL待測溶液于錐形瓶中;c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至終點,消耗KMnO4溶液體積的平均值為20.00mL.
①滴定時盛放KMnO4溶液的儀器為______________(填儀器名稱).
②判斷此滴定實驗達到終點的方法是______________。
③計算上述樣品中FeSO47H2O的質量分數為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有一套電化學裝置,如下圖所示,E 為沾有 Na2SO4溶液的濾紙,并加入幾滴酚酞。A、B分別為Pt片,壓在濾紙兩端,R、S為電源的電極。M、N是用多微孔的 Ni 制成的電極材料,它在堿性溶液中可以視為惰性電極。G為電流計,K為開關。C、D和電解池中都充滿濃KOH溶液。若在濾紙中央點上一滴紫色的 KMnO4溶液,斷開K,接通外電源一段時間后,C、D中有氣體產生。
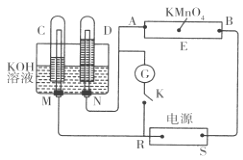
(1)S為________(填“正”或“負”)極。
(2)A極附近溶液的現象是______________, B 極附近發生的電極反應式為___________。
(3)濾紙上的紫色點向______(填“A”或“B”)方移動。
(4)當 C、D里的氣體產生到一定量時,切斷外電源并接通開關K,經過一段時間,C、D中氣體逐漸減少,D中的電極為________ (填“正”或“負”)極,電極反應式為___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦及其合金具有密度小、強度高、耐酸、堿腐蝕等優良性能,被廣泛用于航天、航空、航海、石油、化工、醫藥等部門。由釩鈦磁鐵礦經“選礦”得到的鈦鐵礦提取金屬鈦(海綿鈦)的主要工藝過程如下:

(1)鈦鐵礦的主要成分為FeTiO3。控制電爐熔煉溫度(<1500K),用等物質的量的碳還原出鐵,而鈦以二氧化鈦的形式進入爐渣浮于熔融鐵之上,使鈦與鐵分離,鈦被富集。寫出相關反應:
(2)已知氯化反應過程中會產生一種無色可燃性氣體,請寫出在1073—1273K下氯化反應的化學方程式:
(3)氯化得到的TiCl4中含有的VOCl3必須用高效精餾的方法除去。實際生產中常在409 K下用Cu還原VOCl3,反應物的物質的量之比為1:1,生成氯化亞銅和難溶于TiCl4的還原物,寫出此反應方程式:
(4)TiCl4的還原通常在800oC的條件下進行,反應過程中通入氬氣的目的是 ,試寫出從還原產物中分離出海綿鈦的步驟
(5)電解法冶煉鈦的一種生產工藝是將TiO2與粉末與黏結劑混合后,壓制成電解陰極板,用石墨作陽極,熔融氧化鈣作電解質,電解過程中陽極生成O2和CO2氣體,破碎洗滌陰極板即得到電解鈦。試寫出陰極反應方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸鈉鋁[NaaAlb(OH)c(CO3)d]可用作阻燃劑、抗酸劑等。其制備方法是:控制溫度、pH,向NaHCO3稀溶液中加入Al(OH)3,并攪拌,充分反應后過濾、洗滌、干燥,得堿式碳酸鈉鋁。
(1)堿式碳酸鈉鋁[NaaAlb(OH)c(CO3)d]中a、b、c、d之間的關系為________。
(2)堿式碳酸鈉鋁作為阻燃劑的可能原因:①在分解過程中大量吸熱;②本身及產物無毒且不可燃;③________________________。
(3)若pH過高,則對產品的影響是________________________。
(4)為確定堿式碳酸鈉鋁的組成,進行如下實驗:
①準確稱取2.880 g樣品用足量稀硝酸溶解,得到CO2 0.448 L(已換算成標準狀況下),并測得溶液中含有0.02 mol Al3+。
②加熱至340 ℃以上時樣品迅速分解,得到金屬氧化物、CO2和H2O。當樣品分解完全時,樣品的固體殘留率(固體樣品的剩余質量/固體樣品的起始質量×100%)為56.9%,根據以上實驗數據確定堿式碳酸鈉鋁的組成(寫出計算過程)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com