
| A. | 平衡時,其他條件不變,升高溫度平衡正向移動 | |
| B. | 平衡時,其他條件不變,增加NH3的濃度,廢氣中氮氧化物的轉化率減小 | |
| C. | 其他條件不變,使用高效催化劑,廢氣中氮氧化物的轉化率增大 | |
| D. | 單位時間內消耗NO和N2的物質的量比為1:2時,反應達到平衡 |
分析 對應反應2NH3(g)+NO(g)+NO2(g)$?_{催化劑}^{180℃}$2N2(g)+3H2O(g),反應物氣體的計量數小于生成物氣體的計量數之和,則增大壓強平衡逆向移動,正反應放熱,升高溫度,平衡逆向移動,以此解答該題.
解答 解:A.正反應為放熱反應,升高溫度,平衡向逆反應方向移動,故A錯誤;
B.增大一個反應物濃度,其它反應物轉化率增大,故B錯誤;
C.使用催化劑平衡不移動,廢氣中氮氧化物的轉化率不變,故C錯誤;
D.單位時間內消耗NO和N2的物質的量比為1:2時,等于化學計量數之比,反應到達平衡,故D正確.
故選D.
點評 本題考查外界條件對化學反應速率的影響、平衡狀態的判斷等,為高頻考點,側重于學生的分析能力的考查,注意把握反應的特征以及平衡移動的影響因素,難度不大.


科目:高中化學 來源: 題型:解答題
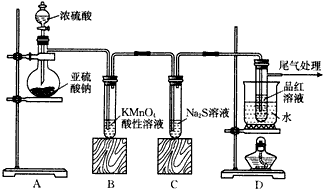
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
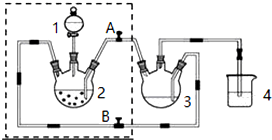
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
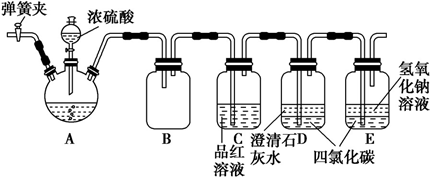
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 溫度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗序號 | 金屬質量 | 金屬狀態 | c(H2SO4)/mol•L-1 | V(H2SO4)/mL | 溶液溫度/℃ | 金屬消失的時間/s | |
| 反應前 | 反應后 | ||||||
| 1 | 0.10 | 絲 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 絲 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | 絲 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | 絲 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | 絲 | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | 絲 | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | 絲 | 1.1 | 50 | 30 | 44 | 40 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在一定條件下,某可逆反應正向是吸熱反應,則其逆向必是放熱反應 | |
| B. | 1 mol A(強酸)與1 mol B(強堿)發生中和反應所放出的熱量叫做中和熱 | |
| C. | 二次電池充電時將電能轉化為化學能 | |
| D. | 需要加熱才能發生的反應可能是吸熱反應也可能是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com