
���}Ŀ���҇����й����߽�����������(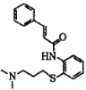 �����܌� 2019- nCoV�Я�Ч������ĺϳ�·����D��
�����܌� 2019- nCoV�Я�Ч������ĺϳ�·����D��

��֪��
��
![]()

��R-NO2![]() R-NH2
R-NH2
������І��}
(1)F�ĽY����ʽ��__________��G��H �ķ��������____________��
(2)E�е��������܈F���Q��______________��
(3)B��C����ԇ�����l����_______________ ��
(4)�ЙC�� D �c���ƚ������~�ҝ�Һ���ӟᣩ�ķ�������ʽ��_________��
(5)J�� E��ͬ�֮����w�������������Зl����J �ĽY����ʽ_______�����ɷN����
���ܰl(f��)���y�R����
��J �Ƿ����廯����ұ��h(hu��n)�ϵ�һ�ȴ���ֻ�ЃɷN
�ۺ˴Ź�����V�� 5 �M�壬�ҷ���e֮�Ȟ� 2 ��2 ��2 ��1 ��1
(6)���������ϳ�·������֪��Ϣ�������ɼױ��ͱ�����(CH3CH2COCl) ��ԭ�Ϻϳ�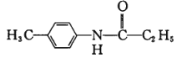 ��·����___________��
��·����___________��
���𰸡�![]() ȡ������ ̼̼�p�I���Ȼ� �������c��Һ���ӟ�
ȡ������ ̼̼�p�I���Ȼ� �������c��Һ���ӟ� ![]() +2Cu(OH)2 + NaOH
+2Cu(OH)2 + NaOH ![]()
![]() +Cu2O ��+3H2O
+Cu2O ��+3H2O ![]() ��
��![]() ��
��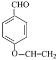 ������2�N
������2�N ![]()
![]()
![]()
![]()
![]()
![]()
��������
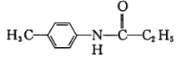
A�c�Țⷴ�����l(f��)��ȡ����������B����֪A��![]() ��B��
��B��![]() ��B��C�^���У�ʧȥCl������OH���tC��
��B��C�^���У�ʧȥCl������OH���tC��![]() ��C��Cu�c����ӟ��£�����D���tD��
��C��Cu�c����ӟ��£�����D���tD��![]() ��E��
��E��![]() ������(j��)��֪�٣���֪F��
������(j��)��֪�٣���֪F��![]() ��F�cH�����õ�
��F�cH�����õ�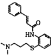 ����֪H��
����֪H��![]() ��G��
��G��![]() ����(j��)������
����(j��)������
(1)����(j��)������֪F�ĽY����ʽ��![]() ��H��
��H��![]() ��G��
��G��![]() ��G��H �ķ��������ȡ���������ʴ𰸞飺
��G��H �ķ��������ȡ���������ʴ𰸞飺![]() ��ȡ��������
��ȡ��������
(2)E��![]() �����е��������܈F���Q��̼̼�p�I���Ȼ����ʴ𰸞飺̼̼�p�I���Ȼ���
�����е��������܈F���Q��̼̼�p�I���Ȼ����ʴ𰸞飺̼̼�p�I���Ȼ���
(3) B��![]() ��C��
��C��![]() ��ȡ���������tB��C����ԇ�����l���������c��Һ���ӟᣬ�ʴ𰸞飺�������c��Һ���ӟ
��ȡ���������tB��C����ԇ�����l���������c��Һ���ӟᣬ�ʴ𰸞飺�������c��Һ���ӟ
(4)�ЙC�� D ��![]() �c���ƚ������~�ҝ�Һ(�ӟ�)�ķ�������ʽ�飺
�c���ƚ������~�ҝ�Һ(�ӟ�)�ķ�������ʽ�飺![]() +2Cu(OH)2 + NaOH
+2Cu(OH)2 + NaOH ![]()
![]() +Cu2O ��+3H2O���ʴ𰸞飺
+Cu2O ��+3H2O���ʴ𰸞飺![]() +2Cu(OH)2 + NaOH
+2Cu(OH)2 + NaOH ![]()
![]() +Cu2O ��+3H2O��
+Cu2O ��+3H2O��
(5) E��![]() ����ͬ�֮����wJ�����ܰl(f��)���y�R�������f������ȩ�������������J �Ƿ����廯����ұ��h(hu��n)�ϵ�һ�ȴ���ֻ�ЃɷN���f���б��h(hu��n)�����h(hu��n)�Ϻ��Ѓɂ���ͬ��ȡ��������̎�ڌ�λ�ϻ��Ѓɂ���ͬ��ȡ��������̎����λ�ϣ��ۺ˴Ź�����V�� 5 �M�壬�ҷ���e֮�Ȟ� 2 ��2 ��2 ��1 ��1���f����5�N�䣬�M�����
����ͬ�֮����wJ�����ܰl(f��)���y�R�������f������ȩ�������������J �Ƿ����廯����ұ��h(hu��n)�ϵ�һ�ȴ���ֻ�ЃɷN���f���б��h(hu��n)�����h(hu��n)�Ϻ��Ѓɂ���ͬ��ȡ��������̎�ڌ�λ�ϻ��Ѓɂ���ͬ��ȡ��������̎����λ�ϣ��ۺ˴Ź�����V�� 5 �M�壬�ҷ���e֮�Ȟ� 2 ��2 ��2 ��1 ��1���f����5�N�䣬�M�����![]() ��
��![]() ��
�� ���ʴ𰸞飺
���ʴ𰸞飺![]() ��
��![]() ��
�� ������2�N��
������2�N��
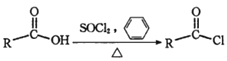
(6)����(j��)��֪��Ϣ��ʾ��![]() ����Fe��HCl�ڼӟ����Ƶ�
����Fe��HCl�ڼӟ����Ƶ� ![]() ��
��![]() �ͱ�����(CH3CH2COCl)��һ���l���µõ�
�ͱ�����(CH3CH2COCl)��һ���l���µõ� ���ױ��l(f��)�����������õ�
���ױ��l(f��)�����������õ�![]() ���t
���t �ĺϳ�·���飺
�ĺϳ�·���飺![]()
![]()
![]()
![]()
![]()
![]()
 ���ʴ𰸞飺
���ʴ𰸞飺![]()
![]()
![]()
![]()
![]()
![]()
 ��
��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����������像U����Cr2O3��CuO��Fe2O3��CaO����ԭ����ȡ�~�ۺ�K2Cr2O7����Ҫ������D��
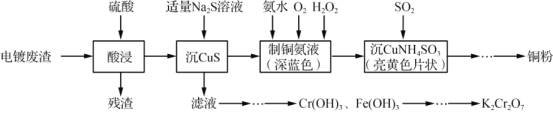
��1����������r�����Ú�������Ҫ�ɷ���___________��
��2������ CuS���r����������c����m�������^�����ܮa(ch��n)���ĺ����_________�����x�ӷ���ʽ��ʾ����
��3��һˮ�������İ����~�ӟᵽ650��ɷֽ���~�����⡢���������ˮ�Լ�һ�N�o��Ⱦ���w�������仯�W����ʽ___________��
��4������CuNH4 SO3���r������D�b�ã��A�֡��ӟ�x���ԣ���
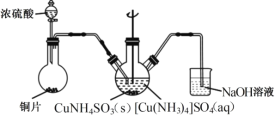
������CuNH4SO3���r������Һ�������45�棬���m�ļӟ᷽ʽ��____________��
��NaOH��Һ��������___________��
��5���y���a(ch��n)Ʒ��K2Cr2O7�����ķ������£��Qȡ�a(ch��n)Ʒԇ��2.0g���250 mL��Һ������Һ��ȡ��25.00 mL���F��ƿ�У���������ϡ�����ữ���ټ����ָʾ������0.1000mol��L�C1���၆�F�@(NH4)2Fe(SO4)2�˜�Һ�M�еζ����؏��M�ж��Ό�����֪Cr2O72-��߀ԭ��Cr3+��
�������Ό������(NH4)2Fe(SO4)2�˜�Һ��ƽ���w�e��25.00mL���t���îa(ch��n)ƷK2Cr2O7�ļ��Ȟ�_____%��[��֪M(K2Cr2O7)=294g��mol-1��Ӌ��Y��������С��(sh��)�c���λ]��
������������K2Cr2O7�l(f��)������߀ԭ������������Һ�г�����Cr3+�⣬߀����һ����ȵ� Fe3+�s�|(zh��)����ͨ�^�ӉA�{(di��o)pH�ķ���ʹ�����D(zhu��n)�����������֪c(Cr3+)=2��10�C5 mol��L-1���t����Һ���_ʼ����Cr(OH)3����rFe3+�Ƿ������ȫ?____________��ͨ�^Ӌ���f��ԭ��{��֪��Ksp[Fe(OH)3]=4.0��10-38��Ksp[Cr(OH)3]=6.0��10-31}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��������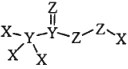 ��һ�N��Ч������������������Һ�����к��Ě���������������Ŀǰ�¹ڲ��������µ���������������X��Y��Z ��ԭ����(sh��)��������Ķ�����Ԫ�ء����Д������_����
��һ�N��Ч������������������Һ�����к��Ě���������������Ŀǰ�¹ڲ��������µ���������������X��Y��Z ��ԭ����(sh��)��������Ķ�����Ԫ�ء����Д������_����
A.ԭ�Ӱ돽��X>Y>Z
B.Ԫ�صķǽ����ԣ�X<Y<Z
C.ԓ��������Z�Ļ��σr����-2 �r
D.ԓ�������� X��Y��Z���M�� 8 ��ӷ�(w��n)���Y��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����һ�K�����cͶ�뵽������ɫʯ��ԇҺ��ʢ��ˮ�ğ�����,��ͬ�W�J����^�쵽���ЬF(xi��n)��,�������_����( )
���cͶ��ˮ��,�ȳ���ˮ��,��ˮ��
���c�����cˮ����,���К��w�a(ch��n)��
�۷�������Һ׃�t
���c�۳��W����С��
��С����ˮ������̎�΄�
���С�˻˻������l(f��)��
A. �٢ڢۢ� B. �ڢۢܢ�
C. �ڢܢݢ� D. �ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���x��[���W���x��3:���|(zh��)�Y���c���|(zh��)] (15����X��Y��Z��W��R��Q��ǰ30̖Ԫ�أ���ԭ����(sh��)��������X������Ԫ����ԭ�Ӱ돽��С�ģ�Y�������ܼ�����ÿ���ܼ��ϵ���Ӕ�(sh��)��ȣ�Zԭ�ӆ���Ӕ�(sh��)��ͬ����Ԫ������࣬W�cZͬ���ڣ���һ��x�ܱ�Z�ĵͣ�R�cYͬһ���壬Q�������ֻ��һ����ӣ�������ӌ���Ӿ�̎��͠�B(t��i)��Ո�ش����І��}��
��1��R��������Ų�ʽ��__________________��
��2��X��Y��Z��W�γɵ��ЙC��YW(ZX2��2��Y��Z���s��܉����ͷքe��__________��ZW3-�x�ӵ����w������__________��
��3��Y��R����߃r������ķ��c�^�ߵ���_____________����Wʽ����ԭ����_________________��
��4����Q���|(zh��)�ķ�ĩ���뵽ZX3�ĝ���Һ�У���ͨ��W2����ַ�������Һ�����{ɫ��ԓ�������x�ӷ���ʽ��______________________________________��
��5��W��Na��һ�N�x�ӻ�����ľ����Y�����D��ԓ�x�ӻ������____________����Wʽ����Na+����λ��(sh��)��_____________����һ����x���܇������������x�Ӟ���c���ɵĎ��w��__________����֪ԓ�������ܶȞ���g��cm-3�������ӵ��_����(sh��)��NA���t�ɂ������W�x���g���x�� nm(�ú�����NA��Ӌ��ʽ��ʾ����

�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��Cu2O��һ�N�댧�w���ϣ����ھGɫ���W�����OӋ����ȡCu2O��늽��ʾ��D���ң�늽⿂�����飺2Cu��H2O![]() Cu2O��H2���������f�����_����
Cu2O��H2���������f�����_����

A. ʯī늘O�Ϯa(ch��n)�����
B. �~늘O�l(f��)��߀ԭ����
C. �~늘O��ֱ���Դ��ؓ�O
D. ����0.1 mol����D(zhu��n)�ƕr����0.1 mol Cu2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����A��B��C��D��E��NԪ�أ�����A��B��C��D�������Ԫ�أ�AԪ�ص����ڔ�(sh��)�����唵(sh��)��ԭ����(sh��)��ͬ��Bԭ�Ӻ�����3�N������ͬ��ԭ��܉����ÿ�N܉���е���Ӕ�(sh��)��ͬ��Cԭ�ӵăr��Ә��͞�csccpc+1��DԪ�ص�ԭ���������Ӕ�(sh��)�ȴ������Ӕ�(sh��)��2����D����x���cE����x����ӌӽY����ͬ��D��E���γɻ�����E2D��
(1)����Ԫ���У���һ��x����С��Ԫ�ص�ԭ�ӽY��ʾ��D��__��D�ăr����Ų��D��__��
(2)���з��ӽY���D�е���������ʾ����Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣�С���c��ʾ�]���γɹ��r�I���������ӣ��̾���ʾ���r�I��

�t�����Ϸ����У�����ԭ�Ӳ���sp3�s���γɻ��W�I����__(����ӵĻ��Wʽ)�� �ڢ۵ķ�������__�����I��__�����I��
(3)A��C��D���γɼȾ����x���I�־��й��r�I�Ļ�����仯�Wʽ���ܞ�__��������C�Ě仯��ˮ��Һ�cCuSO4��Һ�������ɵ������仯�Wʽ��__��Ո�f��ԓ�����������ԭ���c��λ�w����(n��i)���c���֮�g�ij��I��r��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����ǹ��r(n��ng)�I(y��)���a(ch��n)����Ҫ�Ļ��A���|(zh��)���о��ϳɰ������đ��þ�����Ҫ���x��
��1����֪��N2(g)+3H2(g)=2NH3(g)��H=-92kJ/mol��N2(g)+3H2(g)![]() 2NH3(g)�Ļ�ܞ�508kJ/mol���t2NH3(g)
2NH3(g)�Ļ�ܞ�508kJ/mol���t2NH3(g)![]() N2(g)+3H2(g)�Ļ�ܞ�___________kJ/mol
N2(g)+3H2(g)�Ļ�ܞ�___________kJ/mol
��2���҇������ˆT���Ƴ�Ti-H-Fe�p�^(q��)������Ti-H�^(q��)�cFe�^(q��)�ز�ɳ��^100�棩��Ti-H-Fe�p�^(q��)���ϳɰ��ķ����v�����Dһ�����������ڴ����������N�á�*����ע��
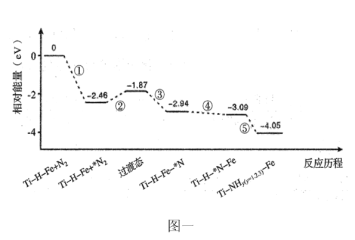
�����f�������_����___________��
A���ٞ�![]() �Ĕ����^��
�Ĕ����^��
B���٢ڢ��ڸߜ^(q��)�l(f��)�����ܢ��ڵ͜^(q��)�l(f��)��
C���ܞ�Nԭ����Fe�^(q��)����Ti-H�^(q��)��Ă��f�^��
D��ʹ��Ti-H-Fe�p�^(q��)�����r�ϳɰ������D(zhu��n)׃?y��u)����ᷴ�?/span>
��3������CO2��ԭ�Ϻϳ����صķ�����2NH3(g)��CO2(g)![]() CO(NH2)2(l)��H2O(g)�����I(y��)���a(ch��n)�r����Ҫԭ�Ϛ⎧��ˮ���⣬�D�����������ʾ�ڲ�ͬˮ̼��[
CO(NH2)2(l)��H2O(g)�����I(y��)���a(ch��n)�r����Ҫԭ�Ϛ⎧��ˮ���⣬�D�����������ʾ�ڲ�ͬˮ̼��[![]() ]�r��CO2��ƽ���D(zhu��n)�����c��̼��[
]�r��CO2��ƽ���D(zhu��n)�����c��̼��[![]() ]֮�g���Pϵ��
]֮�g���Pϵ��
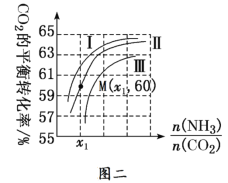
����������ˮ̼��������________���Д�����(j��)��________��
�ڜy��M�c�����ƽ���D(zhu��n)���ʞ�40%���tx1��______��
��4�������������������^���а���(j��ng)��������Ě��w������800�棩������s��100�����£�һ�����ȥ������H2O��ʹNO(g)��O2(g)�l(f��)����������һ����ضȵ�����������NO2(g)��
2NO(g)��O2(g)![]() 2NO2(g)�ķ����v�̷փɲ���
2NO2(g)�ķ����v�̷փɲ���
��.2NO(g)![]() N2O2(g)(�����죬˲�g�_��ƽ��)��H1��0
N2O2(g)(�����죬˲�g�_��ƽ��)��H1��0
v1����k1��c2(NO) v1����k1��c(N2O2)
��.N2O2(g)��O2(g)![]() 2NO2(g)(������)��H2��0
2NO2(g)(������)��H2��0
v2����k2��c(N2O2)c(O2) v2����k2��c2(NO2)
����k1��k2�����ʳ���(sh��)���S�ض�����������
�t:��һ���ض��£�����2NO(g)��O2(g)![]() 2NO2(g)�_��ƽ���B(t��i)��Ո������k1����k1����k2����k2����ʾ��ƽ�ⳣ��(sh��)���_ʽK��_____������(j��)���ʷ��̷��������ߜض�ԓ���������ʜpС��ԭ����__________��
2NO2(g)�_��ƽ���B(t��i)��Ո������k1����k1����k2����k2����ʾ��ƽ�ⳣ��(sh��)���_ʽK��_____������(j��)���ʷ��̷��������ߜض�ԓ���������ʜpС��ԭ����__________��
���Ɍ�(sh��)��(j��)�õ�v2����c(O2)���Pϵ������D��ʾ����x�c���ߵ�ijһ�ضȕr�����������_��ƽ�⣬�t����׃?y��u)��������c��__(����ĸ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��A��B��C��D���ЌW���W��Ҋ�Ć��|(zh��)���ס��ҡ����黯������ڳ��س�����oɫ�oζ��Һ�w��Ԫ��A�п�׃���σr������֮�g�������D����ʾ���D(zhu��n)���Pϵ���ɴ��Ɣࣺ
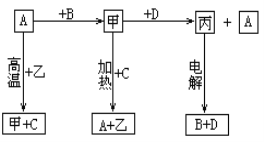
��1���Ļ��Wʽ��_____________�����Ļ��Wʽ��______________��
��2��������D�����Ļ��W����ʽ___________________________________________��
��3����z�������Ԫ�صĻ��σr����Ҫ�õ���ˎƷ��_________________________��
A��ϡ���� B���}�� C�����軯���Һ D�����i�����Һ
��4����y��A���Ҹߜط��������ù��w�л�������|(zh��)���֔�(sh��)��ȡ���������ù��w���OӋ����
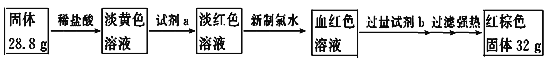
��������|(zh��)���֔�(sh��)��________________��
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com