
分析 此時容器內壓強比反應前減少20%,可知物質的量減少20%,假設達到平衡時消耗2molSO2,則
2SO2+O2?2SO3
起始(mol) 4 2 0
轉化(mol) x 0.5x x
平衡(mol) 4-x 2-0.5x x
結合容器內壓強比反應前減少20%計算該題.
解答 解:此時容器內壓強比反應前減少20%,可知物質的量減少20%,假設達到平衡時消耗2molSO2,則
2SO2+O2?2SO3
起始(mol) 4 2 0
轉化(mol) x 0.5x x
平衡(mol) 4-x 2-0.5x x
則(4+2)×(1-20%)=(4-x+2-0.5x+x),
x=2.4,
則轉化率為$\frac{2.4}{6}×100%$=60%,
故答案為:60%.
點評 本題考查化學平衡的有關計算,為高頻考點,側重于學生的分析、計算能力的考查,本題可用三段式法,也可用差量法計算參加反應的SO2的物質的量,生成的SO3的物質的量,簡化計算,注意優化解題方法.


科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Ba2+、Cl-、NO3- | B. | K+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
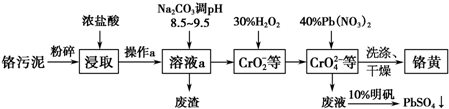
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯
某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯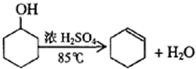
| 密度(g/cm3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
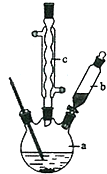 苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線:
苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線: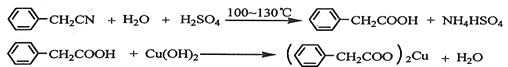
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、C1-、Mg2+、SO42- | B. | A13+、Cu2+、SO42-、C1- | ||
| C. | Ba2+、K+、NO3-、OH- | D. | Ca2+、Na+、C1-、A1O2- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2p1>p2 | B. | PCl5的分解率增大 | ||
| C. | p1>p2 | D. | Cl2的體積分數增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com