
 (1)明礬可用于凈水,用離子方程式解釋其原因Al3++3H2O?Al(OH)3(膠體)+3H+.把FeCl3溶液蒸干、灼燒、最后得到的主要固體產物是Fe2O3.
(1)明礬可用于凈水,用離子方程式解釋其原因Al3++3H2O?Al(OH)3(膠體)+3H+.把FeCl3溶液蒸干、灼燒、最后得到的主要固體產物是Fe2O3.分析 (1)明礬水解生成具有吸附性的氫氧化鋁膠體;將FeCl3溶液蒸干時,鐵離子水解生成Fe(OH)3和HCl,升高溫度促進HCl揮發,所以蒸干溶液時得到堿,灼燒Fe(OH)3時,Fe(OH)3會分解;
(2)醋酸鈉溶液中,醋酸根離子結合水電離的氫離子,溶液顯示堿性;
(3)①根據電荷守恒,和溶液呈中性;
②恰好完全反應時,生成氯化銨,強酸弱堿鹽,水解呈酸性;
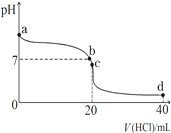
③c點時氨水與鹽酸恰好反應生成氯化銨溶液,根據鹽的水解原理、電荷守恒判斷溶液中各離子濃度大小.
解答 解:(1)明礬水解生成氫氧化鋁膠體,具有吸附性,反應的離子方程式為Al3++3H2O?Al(OH)3(膠體)+3H+,將FeCl3溶液蒸干時,鐵離子水解生成Fe(OH)3和HCl,升高溫度促進HCl揮發,所以蒸干溶液時得到堿,灼燒氫氧化鐵時,氫氧化鐵會分解,反應方程式為2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,所以最終得到的是紅棕色固體Fe2O3,
故答案為:Al3++3H2O?Al(OH)3(膠體)+3H+;Fe2O3;
(2)CH3COONa溶液中,醋酸根離子發生水解生成醋酸和氫氧根離子,溶液顯示堿性,離子方程式為:CH3COO-+H2O?CH3COOH+OH-,
故答案為:堿; CH3COO-+H2O?CH3COOH+OH-;
(3)①根據電荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),和溶液呈中性c(H+)=c(Cl-),所以c(NH4+)=c(Cl-),故答案為:等于;
②恰好完全反應時,生成氯化銨,強酸弱堿鹽,水解呈酸性,水解方程式為:NH4++H2O?NH3?H2O+H+,故答案為:酸;NH4++H2O?NH3?H2O+H+;
③c點時,加入20mL鹽酸,氨水與鹽酸恰好完全反應生成氯化銨溶液,由于銨根離子部分水解,溶液顯示酸性,則c(H+)>c(OH-),根據電荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-)可得:(Cl-)>c(NH4+),溶液中各離子濃度大小為:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案為:c(Cl-)>c(NH4+)>c(H+)>c(OH-);c(Cl-)+c(OH-).
點評 本題考查了鹽的水解原理、酸堿混合的定性判斷、離子濃度大小比較,題目難度中等,注意掌握溶液酸堿性的定性判斷方法,能夠根據電荷守恒、鹽的水解原理判斷溶液中各離子濃度大小.


科目:高中化學 來源: 題型:選擇題
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 使石蕊呈紅色的溶液:NH4+、Ba2+、ClO-、Cl- | |
| C. | 使酚酞呈紅色的溶液:K+、Na+、CH3COO-、Br- | |
| D. | 與鋁反應產生大量氫氣的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴苯(液溴),加四氯化碳、萃取 | |
| B. | 乙烷(乙烯),通入高錳酸鉀溶液、洗氣 | |
| C. | 溴乙烷(乙醇),加水振蕩、分液 | |
| D. | 乙酸乙酯(乙酸),加氫氧化鈉溶液振蕩、分液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①AgNO3;②NaBr;③AgBr | B. | ①AgNO3;②NaCl;③AgCl | ||
| C. | ①AgCl; ②AgNO3;③NaCl | D. | ①AgNO3;②NaCl;③Ag |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
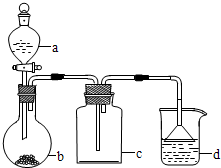
| 選項 | a種物質 | b種物質 | c種物質 | d中收集的氣體 |
| A | 濃氨水 | NaOH | 濃硫酸 | NH3 |
| B | 稀鹽酸 | CaCO3 | 濃硫酸 | CO2 |
| C | 稀硝酸 | Cu | 堿石灰 | NO |
| D | 濃鹽酸 | KMnO4 | 水 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

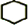 ,B名稱是1,2-二溴環己烷
,B名稱是1,2-二溴環己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$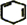 +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Mg2+、NO3-、SO32- | B. | K+、Cl-、NO3-、Fe2+ | ||
| C. | NH4+、Al3+、NO3-、SO42- | D. | K+、Na+、HCO3-、NO3- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com