
【題目】鎳是重要的有色金屬之一,但粗鎳中一般含有Fe、Cu及難與酸、堿溶液反應的不溶性雜質而影響使用.現對粗鎳進行提純,具體的反應流程如下: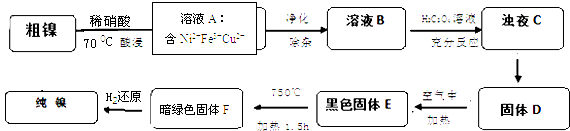
已知:
①2Ni2O3(黑色) ![]() 4NiO(黑色)+O2↑
4NiO(黑色)+O2↑
②
物質 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
Ksp | 8.8×10﹣38 | 2.2×10﹣20 | 5.48×10﹣18 | 3.2×1018 |
根據信息回答:
(1)28Ni在周期表中的第周期;鎳與稀硝酸反應的離子方程式為 . 實驗表明鎳的浸出率與溫度有關,隨著溫度升高鎳的浸出率增大,但當溫度高于70℃時,鎳的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因為;
(2)在溶液A的凈化除雜中,先調節PH=5.5,加熱煮沸5min,靜置一段時間后,過濾出Fe(OH)3 . 為了得到純凈的溶液B還需要加入以下物質進行除雜(填正確答案標號).
A.NaOH
B.Na2S
C.H2S
D.NH3﹒H2O
(3)已知以下三種物質的溶解度關系:NiC2O4>NiC2O4H2O>NiC2O42H2O.由濁液C得到固體D的操作包括過濾、、(填操作名稱); D生成E的化學方程式為
(4)1molE經上述流程得到純鎳,理論上參加反應的氫氣為 mol.
(5)測定樣品中的鎳含量的基本思路是將Ni2+轉化為沉淀,通過測量沉淀的質量進一步推算Ni含量.已知Ni2+能與CO32﹣ , C2O42﹣、S2﹣等離子形成沉淀,但測定時常選用丁二酮肟(C4H8N2O2)作沉淀劑,生成分子式為C8H14N4O4Ni的鮮紅色沉淀.從實驗誤差角度分析主要原因為: .
【答案】
(1)四;3Ni+8H++2NO3﹣=3Ni2++2NO↑+4H2O;溫度升高時,Ni2+的水解程度變大
(2)C
(3)洗滌;干燥;4NiC2O4?2H2O+3 O2=2Ni2O3+8CO2↑+8H2O
(4)2
(5)生成沉淀質量大,稱量誤差小,分析結果準確度高
【解析】解:(1.)28Ni核外有4層電子,是第四周期元素;根據流程圖可知鎳與稀硝酸反應生成硝酸鎳和NO、水,離子方程式為:3Ni+8H++2NO3﹣=3Ni2++2NO↑+4H2O;實驗表明鎳的浸出率與溫度有關,隨著溫度升高鎳的浸出率增大,但當溫度高于70℃時,鎳的浸出率又降低,浸出渣中Ni(OH)2含量增大,Ni(OH)2是由Ni2+水解而得到的,所以溫度過高時Ni2+的水解程度變大,浸出渣中Ni(OH)2含量增大;所以答案是:四;3Ni+8H++2NO3﹣=3Ni2++2NO↑+4H2O;溫度升高時,Ni2+ 的水解程度變大.
(2.)AB選項中含有Na+ , 則溶液B中有Na+雜質,不純凈,錯誤;若選用D,則Cu(OH)2 Ni(OH)2的溶度積相差不大,而且引入NH4+ , 不易的純凈的硝酸鎳溶液,錯誤;C、CuS與NiS的溶度積相差很大,Cu2+沉淀完全而且不會引入新的雜質,正確,
所以答案是:C;
(3.)利用3種物質的溶解度的差異,濁液C中主要得NiC2O42H2O,所以沉淀過濾之后應洗滌、干燥沉淀,則操作Ⅰ、Ⅱ名稱是洗滌、干燥;固體E為黑色,所以應是Ni2O3;則D生成E的化學方程式為:4NiC2O42H2O+3 O2=2Ni2O3+8CO2↑+8H2O;所以答案是:洗滌;干燥;4NiC2O42H2O+3O2=2Ni2O3+8CO2↑+8H2O;
(4.)1mol Ni2O3經上述流程轉化為2molNiO,2molNiO與氫氣發生氧化還原反應,生成單質鎳,需要氫氣的物質的量是2mol;所以答案是:2;
(5.)因為Ni2+與丁二酮肟(C4H8N2O2)生成的C8H14N4O4Ni鮮紅色沉淀的沉淀質量大,稱量誤差小,分析結果準確度高.
所以答案是:生成沉淀質量大,稱量誤差小,分析結果準確度高.


 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案科目:高中化學 來源: 題型:
【題目】下列離子方程式中,屬于水解反應的是( )
A.HCOOH+H2OHCOO﹣+H3O+
B.CO2+H2OHCO3﹣+H+
C.CO32﹣+H2OHCO3﹣+OH﹣
D.HS﹣+H2OS2﹣+H3O+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na2O2是中學化學常用的強氧化劑,除了能與CO2、H2O反應外,還可與其他還原劑如H2、C發生反應,某化學課外興趣小組為探究Na2O2與H2的反應情況,設計了如下圖所示裝置進行有關實驗。

(1)此裝置中,怎樣檢查除啟普發生器之外的裝置的氣密性?_________________________________。
(2)請完成該實驗的有關操作步驟。
①檢查裝置氣密性;
②打開a、b產生氫氣,觀察試管內物質的顏色變化;
③____________________________________________________;
④加熱過氧化鈉,觀察試管內物質的顏色變化;
⑤反應完全后,__________________________________________;
⑥拆卸裝置。
(3)該裝置中,堿石灰的作用是_________________________ 。
(4)實驗過程中觀察到(2)中步驟②無明顯變化,步驟④Na2O2熔化后,黃色粉末立即變成白色,干燥管內硫酸銅未變成藍色。則Na2O2與H2反應的化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應mX(g)+nY(g)qZ(g)的△H<0,m+n>q,在恒容密閉容器中反應達到平衡時,下列說法正確的是( )
A.通入稀有氣體使壓強增大,平衡將正向移動
B.X的正反應速率是Y的逆反應速率的 ![]() 倍
倍
C.降低溫度,混合氣體的平均相對分子質量變小
D.增加X的物質的量,Y的轉化率降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將Na2O2逐漸加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微熱,產生沉淀和氣體的物質的量(mol)與加入的Na2O2物質的量(mol)的關系如圖所示,則原溶液中的Mg2+、Al3+、NH4+物質的量分別( ) 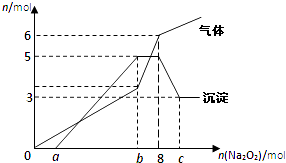
A.2 mol、3 mol、6 mol
B.3 mol、2 mol、6mol
C.2 mol、3 mol、4 mol
D.3 mol、2 mol、2 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請回答下列問題:
(1)純水在T℃時,pH=6,該溫度下1molL﹣1的NaOH溶液中,由水電離出的c(OH﹣)=molL﹣1 .
(2)某一元弱酸溶液(A)與二元強酸(B)的pH相等.若將兩溶液稀釋相同的倍數后,pH(A)pH(B) (填“>”、“=”或“<”).現用上述稀釋溶液中和等濃度等體積的NaOH溶液,則需稀釋溶液的體積V(A)V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的電離方程式是:H2R=H++HR﹣ , HR﹣R2﹣+H+ , 若0.1molL﹣1NaHR溶液的c(H+)=a molL﹣1 , 則0.1molL﹣1H2R溶液中c(H+)(0.1+a) molL﹣1(填“<”、“>”或“=”),理由是 .
(4)電離平衡常數是衡量弱電解質電離程度的物理量.已知:
化學式 | 電離常數(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃時,有等濃度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的順序為(用化學式表示).
②向NaCN溶液中通入少量的CO2 , 發生反應的化學方程式為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)某無色溶液只含有Na+、Ba2+、Al3+、Fe3+、Br-、SO42-、CO32-中兩種或多種離子,取少量逐滴滴入NaOH溶液至過量,先出現白色沉淀后消失的現象;另取少量往其中滴加氯水,溶液為橙黃色;則原溶液一定不存在__________(填離子符號)。寫出原溶液加入過量的NaOH溶液反應的離子方程式_______________。
(2)KClO3和濃鹽酸在一定溫度下的化學方程式為:KClO3+6HCl(濃)=KCl+3Cl2↑+3H2O。濃鹽酸在反應中表現出來的性質是__________(填寫編號)
①只有還原性 ②還原性和酸性 ③只有氧化性 ④氧化性和酸性。
反應中,若氧化產物比還原產物多0.1mol,則電子轉移的物質的量為__________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子中,在無色透明的酸性溶液中,可以大量共存的是( )
A.Al3+、Na+、SO42-、Br-B.Na+、NH4+、NO3-、I-
C.K+、Mg2+、Fe3+、Cl-D.Na+、AlO2-、SO42-、CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,將2.4molA和1.2molB兩種氣體相混合后于容積為2L的某密閉容器中,發生如下反應A(g)+B(g)x C(g)+D(g)△H<0,2min末反應達到平衡狀態,生成了0.8molD,并測得C的濃度為0.4mol/L,請填寫下列空白:
(1)x值等于2min內v(B)= .
(2)A的轉化率為 .
(3)該反應達到平衡時,再向容器中加入1.2molA和0.6molB,再次達到平衡后,A的轉化率(填“增大”、“減小”或“不變”).
(4)該反應的平衡常數的表達式k= , 450℃時平衡常數500℃時平衡常數(填“大于”、“小于”或“等于”).
(5)相同溫度下,若起始時向該容器中充入0.4mol A、0.4mol B、0.2molC和0.2molD,反應達到平衡前,反應速率v正v逆(填“>”或“<”),達到平衡時D的濃度為 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com