
| A. | 需要加熱的反應說明它是吸熱反應 | |
| B. | 已知C(石墨,s)═C(金剛石,s)△H>0,則金剛石比石墨穩定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若將含0.6 mol H2SO4的稀硫酸與含1 mol NaOH的稀溶液混合,放出的熱量等于57.3 kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,則△H1>△H2 |
分析 A.吸熱反應不一定加熱才能進行,有的放熱反應也是需要加熱;
B.能量越高越不穩定;
C.根據熱化學方程式的意義來回答,生成1mol水放出57.3KJ熱量;
D.CO可以繼續燃燒生成二氧化碳,放出熱量.
解答 解:A.需要加熱才能發生的反應不一定為吸熱反應,一些放熱反應也需在加熱條件下才能進行,如鋁熱反應需要高溫下才能發生,是否加熱與反應熱無關,故A錯誤;
B.能量越高越不穩定,C(石墨,s)═C(金剛石,s)△H>0,轉化為金剛石需要吸熱,說明石墨能量較低,則石墨比金剛石穩定,故B錯誤;
C.將含0.6molH2SO4的稀硫酸即H+是1.2mol,與含1molNaOH即OH-是1mol的溶液混合,生成1mol水,放出的熱量等于57.3 kJ,故C正確;
D.放熱△H為負值,CO可以繼續燃燒生成二氧化碳,放出熱量,碳燃燒生成二氧化碳放出的熱量大于生成一氧化碳,所以2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,△H1<△H2,故D錯誤;
故選C.
點評 本題綜合考查化學反應與能量變化,為高頻考點,題目側重考查吸熱反應、放熱反應、反應熱、中和熱的測定等知識,注意把握相關概念的理解,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 若D與鹽酸反應,可生成A和B,則X一定是H2O | |
| B. | 若D是一種強堿,則A、B、C均可與X反應生成D | |
| C. | 若D為NaCl,且A可與C反應生成B,則E可能是CO2 | |
| D. | 若D是一種強酸,則A既可以是單質,也可以是化合物,且D可與銅反應生成B |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在一恒溫恒容密閉容器中充入1mol CO2和3mol H2,一定條件下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol
在一恒溫恒容密閉容器中充入1mol CO2和3mol H2,一定條件下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol| A. | 該密閉容器的體積為1 L | |
| B. | 從反應開始到平衡,氫氣的轉化率為0.75 | |
| C. | 從反應開始到平衡,氫氣的平均反應速率為0.075 mol/(L•min) | |
| D. | 該溫度下,反應的平衡常數的值為$\frac{16}{3}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2個 | B. | 3個 | C. | 4個 | D. | 5個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
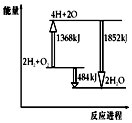
| A. | 拆開2molH2(g)和1molO2(g)中的化學鍵共吸收1368kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共放出1852kJ能量 | |
| C. | 1molH2(g)和$\frac{1}{2}$molO2(g)反應生成1molH2O(l),放出熱量小于242kJ | |
| D. | 2molH2(g)和1molO2(g)反應生成2molH2O(g),共放出484kJ熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HNO3═H++N5++3O2- | B. | Ca(OH)2═Ca2++(OH-)2 | ||
| C. | AlCl3═Al+3+3Cl- | D. | Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 標準狀況下,任何氣體的摩爾體積都約為22.4 L | |
| B. | 1 mol氣體的體積若是22.4 L,它必定處于標準狀況 | |
| C. | 標準狀況下,1molH2和O2混合氣體的體積約為22.4 L | |
| D. | 標準狀況下,11.2L水中含有分子的數目為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 某實驗需要配制460mL1.0mol/L的稀硫酸,應取該硫酸25.0mL | |
| B. | 足量銅和含2mol溶質的該硫酸在加熱條件下反應,標準狀況下生成氣體的體積約為22.4L | |
| C. | 該硫酸與等質量的水混合所得溶液溶質的物質的量濃度小于9.2mol/L | |
| D. | 該硫酸與等體積的水混合所得溶液的溶質質量分數小于49% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com