
【題目】一定溫度下,向容積為2 L的密閉容器中充入一定量的氣體A和氣體B,發生反應: 2A(g)+B(g) ![]() 2C(g),反應過程中測定部分數據見下表(表中t1<t2),下列說法正確的是
2C(g),反應過程中測定部分數據見下表(表中t1<t2),下列說法正確的是
反應時間/min | n(A)/mol | n(B)/mol |
0 | 0.10 | 0.060 |
t1 | 0.012 | |
t2 | 0.016 |
A. 在0~t1 min內的平均反應速率為v(C)=0.088/t1 molL-1min-1
B. 其他條件不變,起始時向容器中充入0.10 mol C和0.010 mol B,平衡時n(A)=0.012 mol
C. 保持其他條件不變,升高溫度,平衡時c(A)=0.0070 molL-1,則反應的ΔH>0
D. 相同溫度下,起始時向容器中充入0.15mol A和0.090mol B,平衡時A轉化率大于88%
【答案】BD
【解析】
經分析,t1時,n(B)=0.016mol,則t1時該反應已經達到平衡狀態,故t2時,n(A)=0.012mol,由此作答。
A. 在0~t1 min內的平均反應速率為v(C)=0.088/2t1 molL-1min-1=0.044/t1 molL-1min1,A錯誤;
B.根據等效平衡,起始充入0.10mol C和0.010mol ,相當于起始充入了0.10mol A和0.060mol B,所以平衡時n(A)=0.012mol,B正確;
C.保持其他條件不變,升高溫度,平衡時c(A)減小,該反應為放熱反應,則反應的ΔH<0;C錯誤;
D. 在原平衡下,參加反應的A的物質的量為0.088mol,則A的轉化率為88%,在新的反應體系中,A、B的物質的量增加了,相當于增大了壓強,平衡向正方反應方向移動,所以該體系中A的轉化率大于88%,D正確;
故合理選項為BD。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】由硫鐵礦“燒渣”(主要成分:Fe3O4、Fe2O3和FeO)制備綠礬(FeSO4·7H2O))的流程如圖:

已知:FeS2(S的化合價為-1)難溶于水。
(1)①中加入的酸為___,濾渣2的主要成分是___。
(2)①中生成Fe3+的離子方程式為Fe3O4+8H+=2Fe3++Fe2++4H2O、___。
(3)檢驗②中Fe3+已經完全轉化成Fe2+的實驗方法:取適量溶液2,___。
(4)通過③得到綠礬晶體的實驗操作:加熱濃縮、冷卻結晶、___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學院科研團隊研究表明,在常溫常壓和可見光下,基于LDH(一種固體催化劑)合成NH3的原理示意圖如下。下列說法不正確的是( )
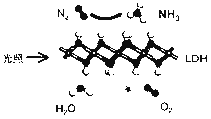
A. 該過程將太陽能轉化成為化學能 B. 該過程中,涉及極性鍵與非極性鍵的斷裂與生成
C. 氧化產物與還原產物的物質的量之比為3∶4 D. 該反應為放熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F、G均為短周期元素,原子序數依次遞增。A元素原子核內無中子,B元素原子最外層電子數是次外層電子數的2倍,D是地殼中含量最多的元素,E是短周期中金屬性最強的元素,F與G位置相鄰,G是同周期元素中原子半徑最小的主族元素。請回答下列問題:
(1)C在元素周期表中的位置為______,G的原子結構示意圖是____。
(2)D與E按原子個數比1:1形成化合物甲,其電子式為____,所含化學鍵類型為____。向甲中滴加足量水時發生反應的化學方程式是______。
(3)E、F、G三種元素所形成的簡單離子,半徑由大到小的順序是_____。(用離子符號表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于各圖像的解釋或結論正確的是

A. 圖①可表示用NaOH溶液滴定等濃度醋酸溶液,溶液導電性隨NaOH的體積變化
B. 圖②可表示25℃時,0.10 molL-1鹽酸滴定20.00mL0.10 molL-1NaOH溶液的滴定曲線
C. 圖③表示水溶液中c(H+)與c(OH-)的變化關系,則水的電離程度(![]() ):
):![]() ;水的離子積:KW(d)=KW(b)
;水的離子積:KW(d)=KW(b)
D. 圖④表示合成氨N2(g)+3H2(g) ![]() 2NH3(g) △H<0的平衡常數與溫度和壓強的關系
2NH3(g) △H<0的平衡常數與溫度和壓強的關系
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列四組實驗,現象和結論均正確的是( )
操作 | 現象 | 結論 | |
A | 滴加稀NaOH溶液,將紅色石蕊試紙置于試管口 | 試紙不變藍 | 原溶液中無NH |
B | 將SO2通入Ba(NO3)2溶液中 | 出現白色沉淀 | 沉淀為BaSO3 |
C | 在Na2S溶液中滴加新制氯水 | 產生淺黃色沉淀 | 非金屬性:C1>S |
D | 將稀硝酸加入過量鐵粉中,充分反應后,滴加KSCN溶液 | 有氣體生成,溶液呈血紅色 | 稀硝酸將Fe氧化成Fe3+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將質量為mg的銅屑完全溶于適量濃硝酸中,反應后得到NO2、NO的混合氣體,將所得氣體通入300mL2molL-1NaOH溶液中,恰好完全反應,生成含NaNO3和NaNO2的鹽溶液,其中NaNO3的物質的量為0.2mol,則m的值為( )
A.12.8B.19.2C.25.6D.51.2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是( )
A. 14 g乙烯和丙烯混合氣體中的氫原子數為2NA
B. 1 mol N2與4 mol H2反應生成的NH3分子數為2NA
C. 1 mol Fe溶于過量硝酸,電子轉移數為2NA
D. 標準狀況下,2.24 L CCl4含有的共價鍵數為0.4NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據要求回答下列問題。
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]()
(1)只含有離子鍵的是______(填序號,下同)
(2)含有共價鍵的離子化合物是______,其中含有非極性共價鍵的物質的電子式為______。
(3)屬于共價化合物的是______。
(4)熔融狀態下能導電的化合物是______。
(5)熔融狀態下和固態時都能導電的物質是______。
(6)用電子式表示![]() 的形成過程:______。
的形成過程:______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com