
| 1mol×[4-(-1)] |
| 1mol×2×[0-(-1)] |


科目:高中化學 來源: 題型:
| A、NaClO3中Cl的化合價是+5 |
| B、被氧化的Cl原子和被還原的Cl原子的物質的量的比為1:5 |
| C、Cl2既是氧化劑又是還原劑 |
| D、每生成1mol的NaClO3轉移6mol的電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:
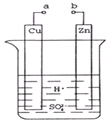 原電池是化學對人類的一項重大貢獻.
原電池是化學對人類的一項重大貢獻. 查看答案和解析>>
科目:高中化學 來源: 題型:

| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 14 |
| 6 |
| 14 |
| 7 |
| 16 |
| 8 |
| 35 |
| 17 |
| 235 |
| 92 |
| 238 |
| 92 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| 葉綠素 |
| 光 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 浙江大學的科研小組成功研制出能在“數分鐘之內”將電量充滿的鋰電池,其成本只有傳統鋰電池的一半.他們把鋰錳氧化物(LMO)浸泡在石墨里面,使其變成一個可以導電的密集網絡的負極材料(如圖),與電解質和正極材料(石墨)構成可充電電池.若電解液為LiAlCl4-SOCl2,電池的總反應為:4LiCl+S+SO2
浙江大學的科研小組成功研制出能在“數分鐘之內”將電量充滿的鋰電池,其成本只有傳統鋰電池的一半.他們把鋰錳氧化物(LMO)浸泡在石墨里面,使其變成一個可以導電的密集網絡的負極材料(如圖),與電解質和正極材料(石墨)構成可充電電池.若電解液為LiAlCl4-SOCl2,電池的總反應為:4LiCl+S+SO2 | 充電 |
| 放電 |
| A、電池的電解液可為LiCl水溶液 |
| B、該電池放電時,負極發生還原反應 |
| C、充電時陽極反應式為:4Cl-+S+SO2-4e-═2SOCl2 |
| D、放電時電子從負極經外電路流向正極,再從正極經電解質流向負極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com