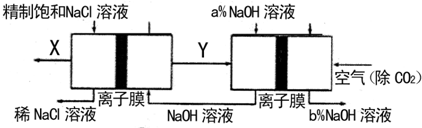
氯堿工業是高耗能產業,為了提高原料的利用率,將電解的Y氣體作為燃料電池的燃料,為電解池供電;X氣體作為鈦的冶煉原料,在這種工藝設計中,相關物料的傳輸與轉化關系如圖所示,其中氯堿工業裝置中的電極未標出,所用的離子膜都只允許陽離子通過.如圖所示:

(1)①圖中的節能型氯堿工業部分,X、Y分別是
Cl2
Cl2
、
H2
H2
(填化學式),分析比較圖示中氫氧化鈉質量分數8%與6%的大小為
a%<b%
a%<b%
;
②分別寫出燃料電池B中正、負極上發生的電極反應,正極:
O2+4e-+2H2O═4OH-
O2+4e-+2H2O═4OH-
,負極:
H2-2e-+2OH-═2H2O
H2-2e-+2OH-═2H2O
;
③這樣設計的主要節(電)能之處在于(寫出兩點):
燃料電池可以為電解池補充電能
燃料電池可以為電解池補充電能
、
提高產品氫氧化鈉的濃度,降低能耗
提高產品氫氧化鈉的濃度,降低能耗
.
(2)寫出鈦鐵礦經氯化法得到四氯化鈦的化學方程式:
2FeTiO
3+6C+7Cl
22FeCl
3+2TiCl
4+6CO
2FeTiO
3+6C+7Cl
22FeCl
3+2TiCl
4+6CO
.
(3)TiCl
4暴露在潮濕空氣中冒白煙,白煙主要為白色的二氧化鈦的水合物H
2TiO
3,寫出該反應的化學方程式:
TiCl4+3H2O═H2TiO3+4HCl
TiCl4+3H2O═H2TiO3+4HCl
.
(4)已知:①
Mg(s)+Cl2(g)MgCl2(s)△H=-641kJ?mol
-1②
Ti(s)+Cl2(g)TiCl4(I)△H=-385kJ?mol
-1寫出Mg與TiCl
4反應的熱化學方程式:
2Mg(s)+TiCl4(s)═2MgCl2(s)+Ti(s)△H-512kJ?mol-1
2Mg(s)+TiCl4(s)═2MgCl2(s)+Ti(s)△H-512kJ?mol-1
,反應在氬氣氛圍中進行的原因是
Mg和Ti都有強還原性,在Ar氣氛中可以防止被氧化
Mg和Ti都有強還原性,在Ar氣氛中可以防止被氧化
.




 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案

 Ⅰ
Ⅰ