
 探究實驗發現,硝酸發生氧化還原反應時,濃度越稀,對應還原產物中氮元素的化合價越低.
探究實驗發現,硝酸發生氧化還原反應時,濃度越稀,對應還原產物中氮元素的化合價越低.

科目:高中化學 來源: 題型:
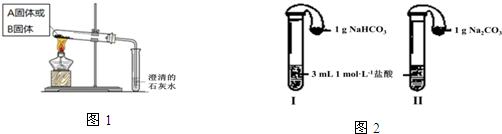
| 實驗方案 | 實驗操作 | 實驗現象 | 結論 |
| 方案1 | 取少量白色物質于試管中,加入適量水,振蕩,樣品全部溶于水,向其中加入無色酚酞試液 | 溶液變成紅色 | 白色物質為Na2O |
| 方案2 | ①取少量白色物質于試管中,加入適量水,振蕩,樣品全部溶于水,向其中加入過量的BaCl2溶液 | 出現白色沉淀 | |
| ②靜置片刻,取上層清液于試管中,滴加無色酚酞試液 | 無明顯現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、12.5% | B、25% |
| C、50% | D、75% |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、c(CO32-)>c(H2CO3) |
| B、c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| D、c(Na+)=c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化學 來源: 題型:
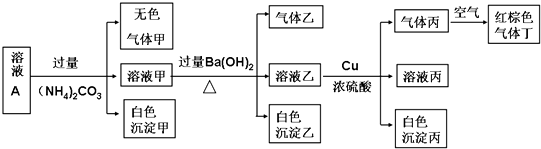
| A、沉淀乙一定有BaCO3,可能有BaSO4 |
| B、實驗消耗Cu 14.4g,則生成氣體丁的體積為3.36L |
| C、該溶液中一定有NO3-、Al3+、SO42-、Cl-四種離子 |
| D、生成的甲、乙、丙氣體均為無色的易溶于水氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、溶液中難以確定Cl-的存在與否 |
| B、原溶液中所含的離子為:Fe2+、K+、NO3-、SO42- |
| C、步驟②中可以確定Fe2+、NO3-的存在,不能確定其它離子是否存在 |
| D、步驟③中的白色沉淀為2種鋇鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.1g | B、0.2g |
| C、0.3g | D、0.4g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com