
A.其主要的作用是給催化劑加熱
B.其作用是把生成的熱量傳遞給需要預熱的混合氣體,并將反應后生成的氣體冷卻
C.為了充分利用廢熱,生產中使冷水經過熱交換器從而得到熱水
D.進行熱量交換時,冷、熱氣體流向相同
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
A.為提高反應速率和原料利用率,硫鐵礦要在“沸騰”狀態下?燃燒??
B.為防止催化劑中毒,氣體在進接觸室前要先凈化?
C.接觸室中熱交換器的主要作用是預熱未反應的氣體和冷卻反應后的氣體?
D.吸收塔中SO3從下而上,水從上而噴下,剩余氣體從上部出來放入空氣?
查看答案和解析>>
科目:高中化學 來源: 題型:
2008年10月14日長江商報報道:湖北監利釩污染致近千人患嚴重皮膚病。監利縣有投產和在建的非法釩冶煉廠達9家,非法釩冶煉廠所造成的污染使得草木枯萎,飲水變咸,清河變濁,人畜奇怪病變,曾經的魚米之鄉正受到前所未有的污染威脅。釩和釩(V)的化合物在工業上有重要用途。如五氧化二釩是工業接觸法制硫酸的催化劑。查閱資料知,利用釩礦石制五氧化二釩和釩的工藝流程圖如下:
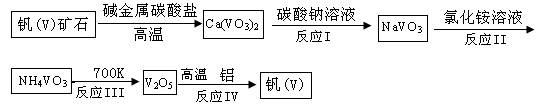
(1)釩(V)的原子序數為23,下列對釩在元素周期表中位置和元素類別判斷正確的是 。
A.它位于第五周期第ⅤB族 B.它位于第四周期第ⅤB族 C.它是過渡元素
D.它位于第五周期第ⅤA族 E.它位于第四周期第ⅤA族 F.它與鐵位于同一周期
(2)工業上,接觸法制硫酸在接觸室里發生反應:2SO2+O2![]() 2SO3,催化劑一般是V2O5??,下列對五氧化二釩作用的描述正確的是 。
2SO3,催化劑一般是V2O5??,下列對五氧化二釩作用的描述正確的是 。
A.能增大該反應所需要的能量 B.能提高二氧化硫的轉化率
C.能改變該反應的反應熱(△H) D.能同程度增大正、逆反應速率
E.能增加SO2和O2分子的能量
(3)寫出下列化學方程式:
反應I: ;反應III: ;反應IV: 。
(4)預測反應II發生的原因是 ;IV的反應類型是 。
查看答案和解析>>
科目:高中化學 來源:09—10年海南中學高二下學期期末考試化學卷 題型:填空題
(12分)硫酸在國民經濟中占有極其重要的地位,下圖是工業接觸法制硫酸的簡單流程圖,試回答下列有關問題.
(1)在實際生產過程中,進入接觸室的氣體中O2的體積分數是SO2體積分數的1.5倍,其原因是
(2)在硫酸工業生產中,為了有利于SO2的轉化,且能充分利用熱能,采用了中間有熱交換器的接觸室。按此密閉體系中氣體的流向,則在B處流出的氣體(除N2外)為 ;
(3)工業上生產硫酸時,利用催化氧化反應將SO2轉化為SO3是一個關鍵步驟。壓強及溫度對SO2轉化率的影響如下表(原料氣各成分的體積分數為:SO2 7%,O2 11%,N2 82%):
| 壓強/MPa 溫度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化學 來源:2011屆吉林省普通中學高三下學期期中教學質量檢測理綜化學部分 題型:填空題
I.目前,我國采用“接觸法”制硫酸,設備如圖所示: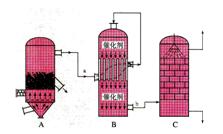
(1)圖中設備A的名稱是_____________ 該設備中主要反應的化學方程式為 。
(2)有關接觸法制硫酸的下列說法中,不正確的是______________。
A.二氧化硫的接觸氧化在接觸室中發生 | B.吸收塔用濃度為98.3%濃硫酸吸收三氧化硫 |
| C.煅燒含硫48%的黃鐵礦時,若FeS2損失了2%,則S損失2% | |
| D.B裝置中反應的條件之一為較高溫度是為了提高SO2的轉化率 |
 氨堿法”中CO2來源于 ;
氨堿法”中CO2來源于 ;查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com