

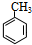
 +Br2$\stackrel{光照}{→}$
+Br2$\stackrel{光照}{→}$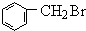 +HBr
+HBr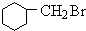 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$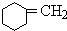 +NaBr+H2O
+NaBr+H2O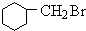 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$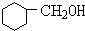 +NaBr.
+NaBr. 分析 A為分子式為C7H8的芳香烴,則A為 ,反應①為甲苯在光照條件下發生甲基上的取代反應,反應②發生苯環與氫氣的加成反應,反應③為醇的消去反應,反應為鹵代烴發生水解反應,可推知B為
,反應①為甲苯在光照條件下發生甲基上的取代反應,反應②發生苯環與氫氣的加成反應,反應③為醇的消去反應,反應為鹵代烴發生水解反應,可推知B為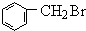 ,C為
,C為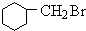 ,D為
,D為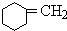 ,E為
,E為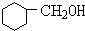 .
.
解答 解:A為分子式為C7H8的芳香烴,則A為 ,反應①為甲苯在光照條件下發生甲基上的取代反應,反應②發生苯環與氫氣的加成反應,反應③為醇的消去反應,反應為鹵代烴發生水解反應,可推知B為
,反應①為甲苯在光照條件下發生甲基上的取代反應,反應②發生苯環與氫氣的加成反應,反應③為醇的消去反應,反應為鹵代烴發生水解反應,可推知B為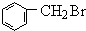 ,C為
,C為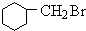 ,D為
,D為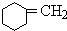 ,E為
,E為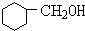 .
.
(1)A的名稱是甲苯,故答案為:甲苯;
(2)①的反應類型是:取代反應.③的反應類型是消去反應,故答案為:取代反應;消去反應;
(3)B(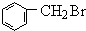 )中鹵素原子的檢驗方法:取少量B溶液于試管中,加NaOH溶液加熱,一段時間后,加入足量HNO3酸化,再加Ag NO3,若產生淡黃色沉淀則為溴元素,
)中鹵素原子的檢驗方法:取少量B溶液于試管中,加NaOH溶液加熱,一段時間后,加入足量HNO3酸化,再加Ag NO3,若產生淡黃色沉淀則為溴元素,
故答案為:取少量B溶液于試管中,加NaOH溶液加熱,一段時間后,加入足量HNO3酸化,再加Ag NO3,若產生淡黃色沉淀則為溴元素;
(4)反應①的化學方程式是: +Br2$\stackrel{光照}{→}$
+Br2$\stackrel{光照}{→}$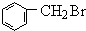 +HBr,
+HBr,
反應③的化學方程式是: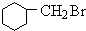 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$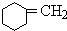 +NaBr+H2O,
+NaBr+H2O,
反應④的化學方程式是: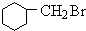 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$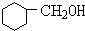 +NaBr,
+NaBr,
故答案為: +Br2$\stackrel{光照}{→}$
+Br2$\stackrel{光照}{→}$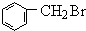 +HBr;
+HBr;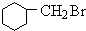 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$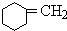 +NaBr+H2O;
+NaBr+H2O;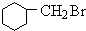 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$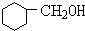 +NaBr.
+NaBr.
點評 本題考查有機物的推斷,涉及芳香烴、鹵代烴的性質與轉化,注意根據反應條件判斷發生的反應,熟練掌握官能團的性質與轉化.


 新思維小冠軍100分作業本系列答案
新思維小冠軍100分作業本系列答案 名師指導一卷通系列答案
名師指導一卷通系列答案科目:高中化學 來源: 題型:選擇題
| A. | 將純水加熱到950C時,Kw變大,pH不變,水仍呈中性 | |
| B. | 向純水中加入稀氨水,平衡逆向移動,c(OH-)增大,Kw變小 | |
| C. | 向水中加入少量固體硫酸氫鈉,c(H+)增大,平衡逆向移動,KW不變 | |
| D. | 向水中通入HCl氣體,平衡逆向移動,溶液導電能力減弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18.6g | B. | 20g | C. | 19.4g | D. | 24g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “冰十六”的密度比液態水小 | B. | “冰十六”與干冰由不同分子構成 | ||
| C. | “冰十六”可以包合氣體分子 | D. | 液態水轉變成“冰十六”是化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(OH-)/c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、Cl-不能大量共存 | |
| B. | 通入過量SO2氣體的溶液中:HSO3-、NO3-、Ba2+不能大量共存 | |
| C. | 向足量NaHSO4溶液中逐漸滴入Ba(HCO3)2溶液的離子方程式為:HCO3-+Ba2++H++SO42-═BaSO4↓+H2O+CO2↑ | |
| D. | 向Fe(NO3)3溶液中加入HI溶液的離子方程式為:2Fe3++2I-═2Fe2++2I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅和濃硝酸反應 | |
| B. | 銅和稀硝酸反應 | |
| C. | 銅與空氣中氧氣反應得氧化銅,然后氧化銅和硝酸反應 | |
| D. | 銅和硝酸銀反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
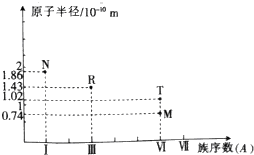
| A. | 常壓下,單質R的熔點高于單質M的熔點 | |
| B. | R、T的簡單離子都會破壞水的電離平衡 | |
| C. | N2M2與R2M3中所含化學鍵的類型完全相同 | |
| D. | N、R、T的最高價氧化物對應的水化物之間能相互反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室用乙酸和正丁醇制備乙酸正丁酯.有關物質的相關數據如下表:
實驗室用乙酸和正丁醇制備乙酸正丁酯.有關物質的相關數據如下表:| 化合物 | 相對分子質量 | 密度/g•cm-3 | 沸點/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com