
| 方案 | 操作 | 判斷 |
| A | 分別加入澄清石灰水 | 產生沉淀者為Na2CO3 |
| B | 分別加入等濃度的稀鹽酸 | 反應較劇烈者為Na2CO3 |
| C | 分別加入CaCl2溶液 | 產生沉淀者為Na2CO3 |
| D | 逐漸加入等濃度的鹽酸 | 立即產生氣泡者為Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 NaHCO3不穩定,加熱易分解,但加熱溶液不分解,都可與堿發生反應,與氫氧化鈣溶液反應都可生成沉淀,且都能與酸反應生成氣體,以此解答該題.
解答 解:A.碳酸鈉和碳酸氫鈉均與Ca(OH)2反應產生沉淀,故Ca(OH)2溶液比較是否有沉淀生成的方法不能鑒別二者,故A錯誤;
B.向Na2CO3中逐滴加入鹽酸時,先無氣體產生,當鹽酸加入較多時,可產生氣體,而向NaHCO3中加入同濃度鹽酸,則迅速產生氣體,產生氣體較為劇烈的為碳酸氫鈉,故B錯誤;
C.碳酸鈉與氯化鈣反應產生碳酸鈣沉淀,碳酸氫鈉與氯化鈣不反應,故氯化鈣溶液可以區分兩物質,故C正確;
D.向Na2CO3中逐滴加入鹽酸時,先無氣體產生,當鹽酸加入較多時,可產生氣體,而向NaHCO3中加入同濃度鹽酸,則迅速產生氣體,故D錯誤.
故選C.
點評 本題考查Na2CO3和NaHCO3的鑒別,側重于學生的分析能力和實驗能力的考查,題目難度不大,注意把握二者性質的差異,學習中注意相關知識的積累.


科目:高中化學 來源: 題型:多選題
| A. | m=2 | |
| B. | 達平衡時,Z的體積分數為10% | |
| C. | 達平衡后,保持容器體積不變,加熱,容器內壓強將增大 | |
| D. | 將平衡后的容器體積壓縮至1L,X的濃度為0.45mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內壓強不隨時間變化 | B. | 化學反應速率關系是:2υ正(X)=υ正(Y) | ||
| C. | 容器內氣體密度不隨時間變化 | D. | 容器內X、Y、Z的濃度之比為l:2:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | υ(A)=0.5mol/(L•min) | B. | υ(B)=1.2mol/(L•s) | C. | υ(C)=0.1mol/(L•s) | D. | υ(D)=0.4mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
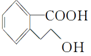 ,下列有關M的說法正確的是( )
,下列有關M的說法正確的是( )| A. | 該分子中存在一個手性碳原子 | |
| B. | M的分子式為C9H10O3 | |
| C. | 1 mol M能與足量Na反應生成0.5 mol H2 | |
| D. | 1 mol M完全燃燒消耗10 mol O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 容器編號 | 溫度(℃) | 起始物質的量(mol) | 平衡物質的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | x | |
| Ⅱ | 387 | 0.40 | y | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
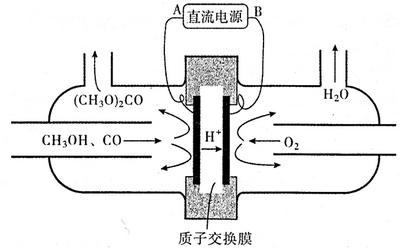
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com