
 計算物質的量;
計算物質的量;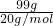 =4.95mol,含有的電子數為4.95mol×10=49.5NA,故A錯誤;
=4.95mol,含有的電子數為4.95mol×10=49.5NA,故A錯誤; =
=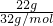 =
=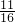 mol,含有氧原子的物質的量為
mol,含有氧原子的物質的量為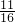 ×2mol=
×2mol=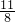 mol,26g臭氧的物質的量為n=
mol,26g臭氧的物質的量為n= =
=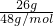 ,含有氧原子的物質的量為
,含有氧原子的物質的量為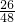 ×3mol,兩者所含氧原子總數為3NA個氧原子,故C正確;
×3mol,兩者所含氧原子總數為3NA個氧原子,故C正確; 2FeCl3,反應后鐵過量,轉移的電子數依據氯氣全部反應計算為0.2NA,故D錯誤;
2FeCl3,反應后鐵過量,轉移的電子數依據氯氣全部反應計算為0.2NA,故D錯誤;

 黃岡創優卷系列答案
黃岡創優卷系列答案湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com