
【題目】下列說法不正確的是( )
A.加入正催化劑,活化分子百分數增大,化學反應速率一定增大
B.熵增加且放熱的反應一定是自發反應
C.任何條件下,化學反應的焓變都等于化學反應的反應熱
D.常溫下硝酸銨能夠溶于水,因為其溶于水是一個熵增大過程
科目:高中化學 來源: 題型:
【題目】某原電池裝置如圖所示,電池總反應為2Ag+Cl2===2AgCl。下列說法正確的是( )
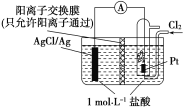
A. 負極反應為Ag-e-===Ag+
B. 放電時,交換膜右側溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替鹽酸,則電池總反應隨之改變
D. 當電路中轉移0.01 mol e-時,交換膜左側溶液中約減少0.02 mol離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金、銀、鋁、鎂、鈦,均是人類大量生產和使用的金屬。試回答下列問題:
(1)一個原子有多級電離能,從電子排布特點判斷第三電離能大小:Mg______Al(填大于或等于或小于)。
(2)鈦被稱為繼鐵、鋁之后的第三金屬。第四周期元素中,未成對電子數目與基態鈦原子未成對電子數目相同元素還有__________種。
(3)基態金原子的外圍電子排布式為5d106s1,試判斷金在元素周期表中的位置_______。
(4)Ag+與氨水形成的二氨合銀離子空間構型是直線形,其中配位原子的雜化類型是______。
(5)四氯化鈦是生產金屬鈦及其化合物的重要中間體。室溫下,四氯化鈦為無色液體,能與水蒸氣反應發煙,生成二氧化鈦固體,可以做煙幕劑。四氯化鈦中存在的化學鍵類型是_______,寫出上述反應的化學方程式____________________。
(6)工業用電解氯化鎂制得鎂,而不用氧化鎂的原因___________________________。
(7)金單質的晶胞是面心立方結構,已知金相對原子質量為M,晶胞邊長為d cm,則一個該晶胞占有的原子總質量為________克。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.加熱才能發生的反應一定是吸熱反應
B.化學反應的熱效應的大小與參加反應的物質的多少無關
C.反應物的總能量大于生成物的總能量的反應一定是放熱反應
D.同溫同壓下,反應H2(g)+Cl2(g)=2HCl(g)在光照和點燃條件下的△H不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為研究銅與濃硫酸的反應,某化學興趣小組進行如下實驗. 實驗I:反應產物的定性探究,按如圖裝置(固定裝置已略去)進行實驗
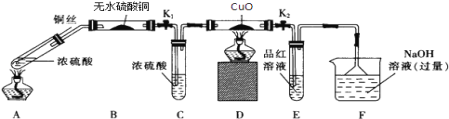
(1)A裝置的試管中發生反應的化學方程式是________________________________;F裝置的作用是______________________;B裝置中的現象是_________________________。
(2)實驗過程中,能證明濃硫酸中硫元素的氧化性強于氫元素的現象是:D裝置中____________,E裝置中_________________________。
(3)實驗結束時,應先_________,再關閉K1 , K2,然后撤去所有酒精燈。
(4)實驗結束后,證明A裝置試管中反應所得產物是否含有銅離子,需將溶液稀釋,操作方法是___________________________________________。
實驗Ⅱ:反應產物的定量探究
(5)在銅與濃硫酸反應的過程中,發現有黑色物質出現,且黑色物質為Cu2S。產生Cu2S的反應為a H2SO4+bCu ![]() cCu2S+dCuSO4+e H2O,則a:b=_________________。
cCu2S+dCuSO4+e H2O,則a:b=_________________。
(6)為測定硫酸銅的產率,將該反應所得溶液中和后配制成250.00mL溶液,取該溶液25.00mL加入足量KI溶液中振蕩,生成的I2恰好與20.00mL 0.30molL﹣1的Na2S2O3溶液反應,若反應消耗銅的質量為9.6g,則硫酸銅的產率為_____________。(已知2Cu2++4I﹣=2CuI+I2, 2S2O32﹣+I2=S4O62﹣+2I﹣)(注:硫酸銅的產率指的是硫酸銅的實際產量與理論產量的比值)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對化學反應的認識正確的是( )
A.化學反應過程中,斷鍵吸熱,成鍵放熱
B.如果某化學反應的△H和△S均小于0,則反應一定能自發進行
C.對于同一個化學反應,一步完成和分幾步完成,其反應的焓變不相同
D.反應物的總焓大于反應產物的總焓時,△H>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中正確的是( )
A. 液溴易揮發,在存放液溴的試劑瓶中應加水封
B. 能使潤濕的淀粉KI試紙變成藍色的物質一定是Cl2
C. 某溶液加入CCl4,CCl4層顯紫色,證明原溶液中存在I-
D. 某溶液加入BaCl2溶液,產生不溶于稀硝酸的白色沉淀,該溶液一定含有Ag+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗操作、現象和解釋或結論都正確的是
選項 | 實驗操作 | 現象 | 解釋或結論 |
A | 過量的Fe粉中加入HNO3, | 溶液呈紅色 | 稀HNO3將Fe氧化為 |
B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出現 | AgCl比AgI更難溶 |
C | Al箔插入稀HNO3中 | 無現象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
D | 用玻璃棒蘸取濃氨水點到紅色石蕊試紙上 | 試紙變藍色 | 濃氨水呈堿性 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究人員從木耳菜中提取過氧化物酶(POD),分別與四種不同酚類物質及H2O2進行催化反應,結果如圖所示。下列相關說法正確的是
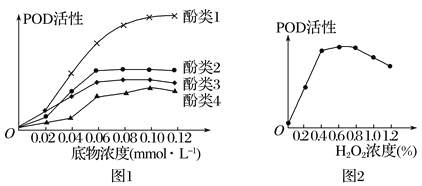
A. 圖1所示的實驗目的是探究不同酚類物質的濃度對POD活性的影響
B. 當底物濃度為0.08 mmolL-1時,POD催化酚類2的反應速率一定大于酚類3
C. 由圖2可知,H2O2濃度過高會抑制POD的活性,降低濃度后POD的活性一定會恢復
D. H2O2對POD活性的影響與溫度和pH對POD活性的影響相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com