

 2CO2的平衡常數為K1;反應4Fe+3O2
2CO2的平衡常數為K1;反應4Fe+3O2 2Fe2O3的平衡常數K2,則反應
2Fe2O3的平衡常數K2,則反應 2Fe+3CO2的平衡常數K與K1、K2的關系式___________。
2Fe+3CO2的平衡常數K與K1、K2的關系式___________。 2Fe+3CO ② Fe2O3+3CO
2Fe+3CO ② Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2  的取值范圍是_________________。
的取值范圍是_________________。 2AlCl3(g)+3CO(g) △H>0,欲提高金屬鋁的氯化效果,不可采取的措施是______(填序號):
2AlCl3(g)+3CO(g) △H>0,欲提高金屬鋁的氯化效果,不可采取的措施是______(填序號): 科目:高中化學 來源: 題型:

| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| 1 |
| 2 |
| 3 |
| 2 |
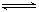 2CO2的平衡常數為K1;反應4Fe+3O2
2CO2的平衡常數為K1;反應4Fe+3O2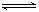 2Fe2O3的平衡常數K2,則反應3CO+Fe2O3
2Fe2O3的平衡常數K2,則反應3CO+Fe2O3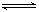 2Fe+3CO2的平衡常數K與K1、K2的關系式
2Fe+3CO2的平衡常數K與K1、K2的關系式
|
|
| ||
| ||
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
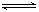 HSO3-+OH-
HSO3-+OH-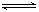 HSO3-+OH-
HSO3-+OH-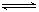 2AlCl3(g)+3CO(g)△H>0,欲提高金屬鋁的氯化效果,不可采取的措施是
2AlCl3(g)+3CO(g)△H>0,欲提高金屬鋁的氯化效果,不可采取的措施是查看答案和解析>>
科目:高中化學 來源: 題型:

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
無水AlCl3可用作有機合成的催化劑、食品膨松劑等。工業制備無水AlCl3的流程如下:

(1)已知:C(s)+O2(g)=CO(g) ; △H=-110.5kJ·mol-1 ①
2Fe(s)+O2(g)=Fe2O3(s) ;△H=-822.1kJ·mol-1 ②
請寫出C還原Fe2O3生成CO的熱化學方程式:
。
(2)氯化爐中通入O2的目的是 。
(3)氯化爐中Al2O3、C12和C反應的化學方程式是 。
(4)氯化爐中導出的氣體,通常用亞硫酸鈉溶液來吸收,請寫出用Na2SO3溶液處理尾氣時發生反應的離子方程式 。
(5)在升華器中加入鋁粉的目的是 。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年江蘇省鎮江市高三上學期期末考試化學試卷(解析版) 題型:填空題
無水AlCl3可用作有機合成的催化劑、食品膨松劑等。工業上由鋁土礦(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下圖所示流程進行一系列反應來制備無水AlCl3。

(1)氯化鋁在加熱條件下易升華,氣態氯化鋁的化學式為Al2Cl6,每種元素的原子最外層均達到8電子穩定結構,則AlCl3是: 晶體,其結構式為: 。
(2)氯化爐中Al2O3、Cl2和C反應的化學方程式是 。
(3)冷卻器排出的尾氣中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反應的離子方程式為: 。
(4)升華器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是: 。
(5)AlCl3產品中Fe元素含量直接影響其品質,為測定產品中Fe元素的含量,現稱取16.25g無水AlCl3產品,溶于過量的NaOH溶液,過濾出沉淀物,沉淀物經洗滌、灼燒、冷卻、稱重殘留固體質量為0.32g。則產品中Fe元素的含量為: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com