
 2SO3(g)在一密閉容器中進行。已知初始濃度 c0(SO2)=0.4mol?L-1、c0(O2)=1mol?L-1,如達到平衡時有80%的SO2轉化為SO3,求平衡時三種氣體的濃度和平衡常數。
2SO3(g)在一密閉容器中進行。已知初始濃度 c0(SO2)=0.4mol?L-1、c0(O2)=1mol?L-1,如達到平衡時有80%的SO2轉化為SO3,求平衡時三種氣體的濃度和平衡常數。  期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案 陽光考場單元測試卷系列答案
陽光考場單元測試卷系列答案 名校聯盟沖刺卷系列答案
名校聯盟沖刺卷系列答案科目:高中化學 來源: 題型:
 (2009?丹東模擬)請根據工業制硫酸的有關知識回答下列問題:
(2009?丹東模擬)請根據工業制硫酸的有關知識回答下列問題:
| ||
| ||
| ||
| △ |


查看答案和解析>>
科目:高中化學 來源: 題型:
 2SO3(g)測得某一時刻SO2、O2、SO3物質的量濃度分別為0.2mol/L、0.1mol/L、0.2mol/L.當反應達到平衡時,下列數據可能存在的是( )
2SO3(g)測得某一時刻SO2、O2、SO3物質的量濃度分別為0.2mol/L、0.1mol/L、0.2mol/L.當反應達到平衡時,下列數據可能存在的是( )查看答案和解析>>
科目:高中化學 來源: 題型:
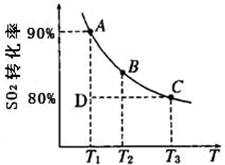 硫及其化合物在國民生產中占有重要的地位.
硫及其化合物在國民生產中占有重要的地位.| 1 | 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
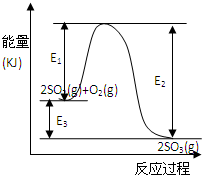 利用催化氧化反應將SO2轉化為SO3是工業上生產硫酸的關鍵步驟.T℃時反應2SO2(g)+O2(g)?2SO3(g)過程中的能量變化如圖所示,回答下列問題.
利用催化氧化反應將SO2轉化為SO3是工業上生產硫酸的關鍵步驟.T℃時反應2SO2(g)+O2(g)?2SO3(g)過程中的能量變化如圖所示,回答下列問題.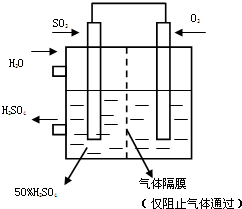
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com