
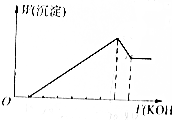
 把鎂鋁合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的體積與生成沉淀的質量關系如圖所示,則合金中鎂與鋁的質量比是( )
把鎂鋁合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的體積與生成沉淀的質量關系如圖所示,則合金中鎂與鋁的質量比是( )| A. | 1:1 | B. | 8:9 | C. | 4:3 | D. | 4:9 |
分析 由圖象可知,金屬與酸反應時酸過量,利用7~8體積發生的反應為Al(OH)3+KOH═KAlO2+2H2O來計算Al的量,由1~7體積發生Al3++3OH-═Al(OH)3↓、Mg2++2OH-═Mg(OH)2↓來計算Mg的量,然后計算合金中鎂和鋁的質量比.
解答 解:設KOH的濃度為cmol/L,合金中Al的物質的量為x,Mg的物質的量為y,
由7~8體積發生的反應為Al(OH)3+KOH═KAlO2+2H2O,則
Al~Al(OH)3~NaOH
1 1
x (8-7)×0.001L×c
x=0.001cmol,
由1~7體積發生Al3++3OH-═Al(OH)3↓、Mg2++2OH-═Mg(OH)2↓,則
Al3++3OH-═Al(OH)3↓
1 3
0.001cmol 0.003cmol
Mg2++2OH-═Mg(OH)2↓
1 2
y (0.006c-0.003c)mol
y=0.0015cmol,
則合金中鎂和鋁的質量比為0.0015cmol×24g/mol:0.001cmol×27g/mol=4:3,
故選C.
點評 本題考查鎂、鋁及其化合物的性質,明確發生的化學反應及反應與圖象的關系是解答本題的關鍵,難度不大.


 新課標階梯閱讀訓練系列答案
新課標階梯閱讀訓練系列答案科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
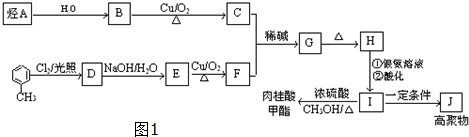
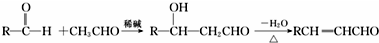
 $→_{△}^{硫酸}$
$→_{△}^{硫酸}$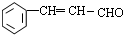 +H2O.
+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在酒精燈加熱條件下,Na2CO3、NaHCO3固定都能發生分解 | |
| B. | 不可用元素周期律解釋熱穩定性:Na2CO3>NaHCO3 | |
| C. | 分別加熱Na2CO3和NaHCO3固體,試管內壁均有水珠,則兩種物質均受熱分解 | |
| D. | 1L0.1mol•L-1NaHCO3溶液中HCO3-和CO32-離子數之和為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉-鉀合金可在核反應堆中用作熱交換液 | |
| B. | 過氧化鈉可用作潛水艇中的供氧劑 | |
| C. | 純堿可用作治療胃酸過多的藥劑 | |
| D. | 碳酸氫鈉溶液用于制泡沫滅火劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在蒸發食鹽水時,邊加熱邊用玻璃棒攪拌直至液體蒸干 | |
| B. | 鑒別Na2CO3與NaHCO3固體可用加熱的方法 | |
| C. | 實驗室制備氫氧化鐵膠體時,向飽和氯化鐵溶液中滴加氫氧化鈉溶液 | |
| D. | 配制一定物質的量濃度的NaOH溶液,將NaOH固體放在容量瓶中加水溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NaBr+Cl2=2CaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2=2H2O+3S↓ | |
| D. | 2CO+O2=2CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com