
生物質能是一種潔凈、可再生能源。生物質氣(主要成分為 CO、CO2、H2 等)與H2混合,催化合成甲醇和二甲醚(CH3OCH3)及許多烴類物質等,是生物質能利用的方法之一.
(1)已知碳的氣化反應在不同溫度下平衡常數的對數值(lgK)如下表:

反應:CO(g)+H2O(g)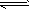 CO2(g)+H2(g),該反應的△H________0(選填:“>”、“<”、“=”);在900K時,該反應平衡常數的對數值(lgK)=_____________.
CO2(g)+H2(g),該反應的△H________0(選填:“>”、“<”、“=”);在900K時,該反應平衡常數的對數值(lgK)=_____________.
(2)甲醇是一種重要的能源和化工原料,工業上合成甲醇的反應為:CO+2H2⇌CH3OH.現已知:H2(g)、CO(g)、CH3OH(l)的燃燒熱ΔH分別為-285.8KJ/mol、-283.0KJ/mol和-726.5KJ/mol。則:CH3OH不完全燃燒生成CO和液態H2O的熱化學反應方程式 .
(3)在一定溫度、壓強和催化條件下,工業上用CO和H2反應生成二甲醚,同時產生一種參與大氣循環的無機物。則該反應的化學反應方程式為: .
(4)下圖左為綠色電源“二甲醚燃料電池”的工作原理示意圖.a電極上發生反應的電極反應式為 .
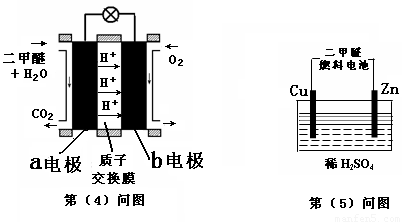
(5)連接下圖右裝置的電源為(4)問中的二甲醚燃料電池。接通電源一段時間后,觀察到裝置中電解質溶液顏色由無色變為藍色,并逐漸加深。則該裝置中的Cu電極應與二甲醚燃料電池中 電極(填a或b)相連。通電時發生反應的總的離子反應方程式為: .
(1)<; 0.36 (2)CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5KJ/mol
(3)3CO+3H2 =(CH3)2O+CO2或者2CO+4H2 =(CH3)2O+ H2O,
(4)(CH3)2O-12e-+3H2O=2CO2+12H+(5)b Cu+2H+ Cu2++H2↑
Cu2++H2↑
【解析】
試題分析:K1={ C(CO)·C(H2)} /C(H2O);K2=
{ C(CO2)·C2(H2)} /C2(H2O)
②-①整理得:CO(g)+H2O(g)  CO2(g)+H2(g),它的平衡常數為:K={ C(CO2)·C(H2)} /{
C(CO) ·C(H2O)}.=K2/K1. K越大,lgK就越大。升高溫度K減小,說明升高溫度化學平衡向逆反應方向移動。根據化學平衡移動原理:升高溫度,化學平衡向吸熱反應方向移動。逆反應是吸熱反應。所以正反應為放熱反應。所以△H<0.在900K時,該反應平衡常數的對數值lgK =lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36. (2)由題意可寫出CO、CH3OH燃燒的熱化學方程式①CO(g)+(1/2)O2(g)=CO2(g)
△H=-283.0KJ/mol;②CH3OH(l)+(3/2)O2(g)=CO2(g)+2H2O. ②-①得:CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5KJ/mol。(3)根據題意可得反應的化學方程式:3CO+3H2 =(CH3)2O+CO2或者2CO+4H2 =(CH3)2O+
H2O。(4)在燃料電池中,通入燃料的電極作負極,通入氧氣的電極作正極。a電極及負極上發生反應的電極反應式是:(CH3)2O-12e-+3H2O=2CO2+12H+。(5)在電解池中觀察到裝置中電解質溶液顏色由無色變為藍色,并逐漸加深。說明Cu失去了電子。Cu電極作陽極。二甲醚燃料電池中b電極(即正極)相連。通電時發生反應的總的離子反應方程式為:Cu+2H+
CO2(g)+H2(g),它的平衡常數為:K={ C(CO2)·C(H2)} /{
C(CO) ·C(H2O)}.=K2/K1. K越大,lgK就越大。升高溫度K減小,說明升高溫度化學平衡向逆反應方向移動。根據化學平衡移動原理:升高溫度,化學平衡向吸熱反應方向移動。逆反應是吸熱反應。所以正反應為放熱反應。所以△H<0.在900K時,該反應平衡常數的對數值lgK =lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36. (2)由題意可寫出CO、CH3OH燃燒的熱化學方程式①CO(g)+(1/2)O2(g)=CO2(g)
△H=-283.0KJ/mol;②CH3OH(l)+(3/2)O2(g)=CO2(g)+2H2O. ②-①得:CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5KJ/mol。(3)根據題意可得反應的化學方程式:3CO+3H2 =(CH3)2O+CO2或者2CO+4H2 =(CH3)2O+
H2O。(4)在燃料電池中,通入燃料的電極作負極,通入氧氣的電極作正極。a電極及負極上發生反應的電極反應式是:(CH3)2O-12e-+3H2O=2CO2+12H+。(5)在電解池中觀察到裝置中電解質溶液顏色由無色變為藍色,并逐漸加深。說明Cu失去了電子。Cu電極作陽極。二甲醚燃料電池中b電極(即正極)相連。通電時發生反應的總的離子反應方程式為:Cu+2H+ Cu2++H2↑。
Cu2++H2↑。
考點:考查原電池、電解池的反應原理及化學平衡常數的計算、熱化學方程式的書寫等知識。


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 生物質能是一種潔凈、可再生的能源.生物質氣(主要成分為CO、CO2、H2等)與H2混合,催化合成甲醇是生物質能利用的方法之一.
生物質能是一種潔凈、可再生的能源.生物質氣(主要成分為CO、CO2、H2等)與H2混合,催化合成甲醇是生物質能利用的方法之一.查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省德陽市“一診”考試化學試卷(解析版) 題型:填空題
生物質能是一種潔凈、可再生能源。生物質氣(主要成分為CO、CO2、H2等)與混合,在含有Zn、Cu等元素的催化劑條件下能合成一種生物質能——甲醇。
(1) 與CO互為等電子體的物質的化學式是 。
(2) CO2分子中碳原子的雜化類型是 雜化。
(3) 按電子排布Zn在元素周期表中屬于 區,
其晶體屬于六方最密堆積,它的配位數是 。
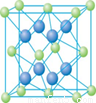
(4) Cu的一種氯化物晶體的晶胞結構如圖所示。(空心球代表氯離子),則一個晶胞中所含的數目是 。
查看答案和解析>>
科目:高中化學 來源:2014屆四川省高二10月階段性考試化學試卷(解析版) 題型:填空題
(5分)生物質能是一種潔凈、可再生能源。生物質氣(主要成分為 CO、CO2、H2 等)與 H2 混合,催化合成甲醇是生物質能利用的方法之一。
(1)上述反應的催化劑含有 Cu、Zn、Al 等元素。寫出基態 Cu2+離子的核外電子排布式_______________________________________;
(2)根據等電子原理,寫出 CO 分子的結構式______________________;
(3)甲醇催化氧化可得到甲醛,甲醛與新制 Cu(OH)2 的堿性溶液反應生成 Cu2O 沉淀。
①甲醛分子中碳原子軌道的雜化類型為_____________________;
②甲醛分子的空間構型是__________________;
③ 1 mol 甲醛分子中 σ 鍵的數目為__________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com