
實驗室常用二氧化錳和濃鹽酸共熱的方法制取氯氣,反應中二氧化錳被還原為MnCl2。根據要求回答下列問題:
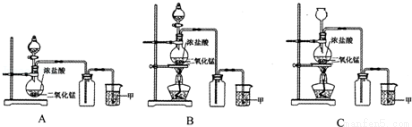
(1)A、B、C三套裝置中,應選用的裝置是 (選填“A”、“B”、“C”)。
(2)寫出實驗室用上述方法制取氯氣的化學方程式 。
(3)為了防止氯氣污染環境,圖中所示的溶液甲為 ,在該溶液中發生反應的化學方程式 。
(4)利用該原理和裝置進行實驗,制得的氯氣中往往含有的雜質有 ,可依次通入到 除去。
科目:高中化學 來源:2016-2017學年內蒙古高二上學期期中化學試卷(解析版) 題型:實驗題
1、某學生用0.1 mol·L-1的KOH標準溶液滴定未知濃度的鹽酸,其操作分解為如下幾步:
A.移取20mL待測鹽酸注入潔凈的錐形瓶中,并加入2~3滴酚酞; |
B.用標準溶液潤洗滴定管2~3次; |
C.把盛有標準溶液的堿式滴定管固定好,調節滴定管尖嘴使之充滿溶液; |
D.取標準KOH溶液注入堿式滴定管至刻度“0”以上1~2cm 處; |
E.調節液面至“0”或“0”以下刻度,記下讀數;
F.把錐形瓶放在滴定管的下面,用標準KOH溶液滴定至終點并記下滴定管液面的刻度.
就此實驗完成填空:
(1)正確操作步驟的順序是(用序號字母填寫)__________AF。
(2)上述B步驟操作的目的是_____________。
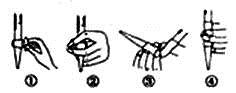
(3)在進行C步操作滴定前排氣泡時,應選擇下圖2中的 (填序號),若用25mL滴定管進行實驗,當滴定管中的液面在“10”處,則管內液體的體積(填序號)____________(①=10mL,②=15mL,③<10mL,④>15mL)。
(4)判斷以下操作,對測定結果鹽酸濃度的影響(填“偏高”、“偏低”或““無 影響”)
①上述A步驟操作之前,若先用待測溶液潤洗錐形瓶,則對滴定結果的影響是__________。
②若稱取一定量的KOH固體(含少量NaOH)配制標準溶液并用來滴定上述鹽酸,則對滴定結果產生的影響是____________。
③如果滴定前裝有待測溶液的酸式滴定管尖嘴部分有氣泡,而滴定結束后氣泡消失,則測定結果將__________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省高二上期中化學試卷(解析版) 題型:選擇題
歸納法是高中化學學習常用的方法之一,某化學研究性學習小組在學習了《化學反應原理》后作出了如下的歸納總結:歸納正確的是
①向0.1 mol·L-1 CH3COOH溶液中加入少量冰醋酸,平衡向正反應方向移動,電離程度增大;
②常溫下,pH=3的醋酸溶液與pH=11的NaOH溶液等體積混合,則有c(Na+) +c(H+)=c(OH-)+c(CH3COO-)
+c(H+)=c(OH-)+c(CH3COO-)
③常溫下,AgCl在同物質的量濃度的CaCl2和NaCl溶液中的溶解度相同;
④常溫下,已知醋酸電離平衡常數為Ka;醋酸根水解平衡常數為Kh;水的離子積
A.①②④ B.②④ C.②③ D.①②③④
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二上期中化學卷(解析版) 題型:選擇題
某溫度下,在固定容積的密閉容器中,可逆反應A(氣)+3B(氣) 2C(氣)達到平衡時,各物質的物質的量之比為n(A)∶n(B)∶n(C)=2∶2∶1,保持溫度不變,以2∶2∶1的物質的量之比再充入A、B、C ,則下列說法正確的是( )
2C(氣)達到平衡時,各物質的物質的量之比為n(A)∶n(B)∶n(C)=2∶2∶1,保持溫度不變,以2∶2∶1的物質的量之比再充入A、B、C ,則下列說法正確的是( )
A.平衡不移動
B.再達平衡時,n(A)∶n(B)∶n(C)仍為2∶2∶1
C.再達平衡時,B的體積分數減小
D.再達平衡時,正反應速率增大,逆反應速率減小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二上期中化學卷(解析版) 題型:選擇題
已知強酸與強堿的稀溶液發生中和反應的熱化學方程式為 H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,又知電解質的電離是吸熱過程。向1 L 0.5 mol·L-1的NaOH溶液中加入下列物質:①稀醋酸;②濃硫酸;③稀硝酸,恰好完全反應。則其焓變ΔH1、ΔH2、ΔH3的關系是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH3<ΔH2
C.ΔH1=ΔH3>ΔH2 D.ΔH1>ΔH3>ΔH2
D.ΔH1>ΔH3>ΔH2
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省嘉興市七校高一上期中化學試卷(解析版) 題型:選擇題
能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶無色溶液加以區別的一種試劑是(必要時可以加熱)( )
A.BaCl2 B.NaOH C.Ba(OH)2 D.AgNO3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省嘉興市七校高一上期中化學試卷(解析版) 題型:選擇題
在標準狀況下,448 mL 某氣體的質量為1.28 g,該氣體的摩爾質量約為( )
A.46 g B.44 C.64 g·mol-1 D.32 g·mol-1
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市武清區等五區縣高二上期中化學卷(解析版) 題型:填空題
在一定體積的密閉容器中,進行如下化學反應:CO2(g)+H2(g) CO(g)+H2O(g),其化學平衡常數K與溫度t的關系如下:
CO(g)+H2O(g),其化學平衡常數K與溫度t的關系如下:
T/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
請回答下列問題:
(1)該反應為___________反應。(填“吸熱”或“放熱”)
(2)830℃,c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, C(H2)=0.05mol/L,該反應__________(填“是”或“否”)達到的化學平衡狀態。
(3)800℃時,固定容積的密閉容器中,放入混合物,起始濃度為c(CO)=0.01 mol/L,c(H2O)=0.03 mol/L,c(CO2)=0.01 mol/L,c(H2)=0.05 mol/L,則反應開始時,H2O的消耗速率比生成速率___________(填“大”、“小”或“不能確定”)
(4)830℃時,在1L的固定容積的密閉容器中放入2mol CO2和1mol H2,平衡后CO2的轉化率為___________,H2的轉化率為___________(用分數表示)。若再充入1mol H2則H2的轉化率為___________(增大,減少,不變)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年天津市紅橋區高一上學期期中化學試卷(解析版) 題型:選擇題
已知:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,則下列說法不正確的是( )
A.還原劑是HCl,氧化劑是KMnO4
B.每生成1mol Cl2轉移電子的物質的量為2mol
C.氧化劑與還原劑的物質的量之比為1:8
D.氧化產物與還原產物的物質的量之比為5:2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com