
【題目】25 ℃時,水的電離達到平衡:H2O![]() H++OH- △H>0,下列敘述正確的是 ( )
H++OH- △H>0,下列敘述正確的是 ( )
A.向水中加入稀氨水,平衡逆向移動,c(OH-)降低
B.向水中加入少量固體硫酸氫鈉,c(H+)增大,Kw不變
C.由水電離出的c(H+)=1×10-12mol/L的溶液pH一定為12
D.將水加熱,Kw增大,pH不變
 激活思維優加課堂系列答案
激活思維優加課堂系列答案 活力試卷系列答案
活力試卷系列答案 課課優能力培優100分系列答案
課課優能力培優100分系列答案科目:高中化學 來源: 題型:
【題目】實驗室需配制0.2000molL﹣1Na2S2O3標準溶液450mL,并利用該溶液對某濃度的NaClO溶液進行標定.
(1)若用Na2S2O3固體來配制標準溶液,在如圖所示的儀器中,不必要用到的儀器是_________(填字母),還缺少的玻璃儀器是_________(填儀器名稱)。
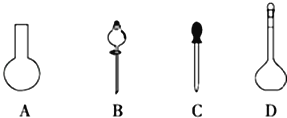
(2)根據計算需用天平稱取Na2S2O3固體的質量是_________g。在實驗中其他操作均正確,若容量瓶用蒸餾水洗滌后未干燥,則所得溶液濃度_________(填“>”“<”或“=”,下同)0.2000molL﹣1.若還未等溶液冷卻就定容了,則所得溶液濃度_________0.2000molL﹣1。
(3)用滴定法標定的具體方法:量取20.00mL NaClO溶液于錐形瓶中,加入適量稀鹽酸和足量KI固體,用0.2000molL﹣1Na2S2O3標準溶液滴定至終點(淀粉溶液作指示劑),四次平行實驗測定的V(Na2S2O3)數據如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
測定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
V(Na2S2O3)/mL | 21.90 | 18.80 | 22.10 | 22.00 |
①NaClO溶液中加入適量稀鹽酸和足量KI固體時發生反應的離子方程式為_________。
②NaClO溶液的物質的量濃度是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積一定的密閉容器中,置入一定量的一氧化氮和足量碳發生化學反應:C(s)+2NO(g)![]() CO2(g)+N2(g),平衡時c(NO)與溫度T的關系如圖所示,則下列說法正確的是( )
CO2(g)+N2(g),平衡時c(NO)與溫度T的關系如圖所示,則下列說法正確的是( )
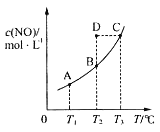
A.該反應的ΔH>0
B.若該反應在T1、T2℃時的平衡常數分別為K1、K2,則K1<K2
C.在T2℃時,若反應體系處于狀態D,則此時v正>v逆
D.若狀態B、C、D的壓強分別為p(B)、p(C)、p(D),則p(C)=p(D)>p(B)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:A 是石油裂解氣的主要產物之一,其產量常用于衡量一個國家石油化工發展水平的標志。下列是有機物 A~G 之間的轉化關系:
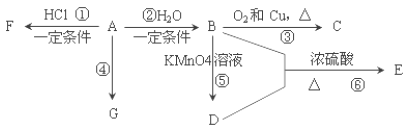
請回答下列問題:
(1)A 的官能團的名稱是___________; C 的結構簡式是________;
(2)E 是一種具有香味的液體, 由 B+D→E 的反應方程式為___________, 該反應類型是______________;
(3)G 是一種高分子化合物,其結構簡式是______________;
(4)比賽中,當運動員肌肉挫傷或扭傷時,隨隊醫生即對準受傷部位噴射物質 F(沸點 12.27°C)進行應急處理.寫出由A 制 F 的化學反應方程式______________。
(5)E 的同分異構體能與 NaHCO3溶液反應,寫出該同分異構體的結構簡式_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對滴有酚酞試液的下列溶液,操作后顏色變深的是
A. 明礬溶液加熱 B. CH3COONa溶液加熱
C. 氨水中加入少量NH4Cl固體 D. 小蘇打溶液中加入少量NaCl固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】網絡趣味圖片“一臉辛酸”,是在臉上重復畫滿了辛酸的鍵線式結構。下列有關辛酸的敘述正確的是
A. 辛酸的同分異構體(CH3)3CCH (CH3) CH2COOH的名稱為 2,2,3-三甲基戊酸
B. 辛酸的羧酸類同分異構體中,含有3個“一CH3”結構,且存在乙基支鏈的共有7種(不考慮立體異構)
C. 辛酸的同分異構體中能水解生成相對分子質量為74的有機物的共有8種(不考慮立體異構)
D. 正辛酸常溫下呈液態,而軟脂酸常溫下呈固態,故二者不符合同一通式
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T1時,在三個容積均為1L的恒容密閉容器中僅發生反應: 2NO2(g)![]() 2NO(g)+O2(g) (正反應吸熱)。實驗測得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆為速率常數,受溫度影響。
2NO(g)+O2(g) (正反應吸熱)。實驗測得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆為速率常數,受溫度影響。
下列說法正確的是
容器 編號 | 物質的起始濃度(mol·L-1) | 物質的平衡濃度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 設k為該反應的化學平衡常數,則有k=k逆:k正
B. 達平衡時,容器Ⅱ與容器Ⅲ中的總壓強之比為20∶17
C. 容器Ⅱ中起始平衡正向移動,達平衡時,容器Ⅱ中NO2的轉化率比容器Ⅰ中的小
D. 若改變溫度為T2,且T2>T1,則k正:k逆<0.8
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學按右圖所示的裝置進行實驗。 A、B為兩種常見金屬,它們的硫酸鹽可溶于水。當 K 閉合時,在交換膜處 SO42-從右向左移動。下列分析正確的是

A.溶液中A2+濃度減小
B.B 的電極反應: B-2eˉ=B2+
C.y 電極上有 H2產生,發生還原反應
D.反應初期,x電極周圍出現白色膠狀沉淀,不久沉淀溶解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學院深圳先進技術研究院研發出一種新型鋁一石墨烯雙離子電池(AGDIB電池),該電池以溶有六氟磷酸鋰![]() 的碳酸酯類溶劑為電解液放電時合金
的碳酸酯類溶劑為電解液放電時合金![]() 發生去合金化反應陰離子
發生去合金化反應陰離子![]() 從石墨烯C中脫嵌進入電解質溶液。放電時其工作原理如圖所示,下列說法錯誤的是( )
從石墨烯C中脫嵌進入電解質溶液。放電時其工作原理如圖所示,下列說法錯誤的是( )

A.該電池不能用水作為電解質溶液
B.放電時,a電極的電極反應式為Li-e-=Li+
C.廢舊AGDIB電池進行“放電處理”時,若轉移1mole-,則可回收7gLi
D.充電時,b電極的電極反應式為PF6--e-+Cx=CxPF6
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com