
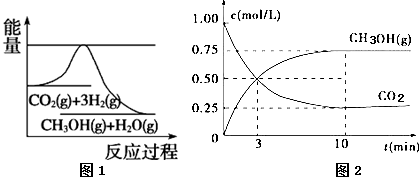
| A. | 該反應在高溫下才能自發進行 | |
| B. | 再加入一定量CO2,則$\frac{n({CH}_{3}OH)}{n({CO}_{2})}$增大 | |
| C. | 溫度降低,CH3OH(g)+H2O(g)?CO2(g)+3H2(g)的平衡常數K增大 | |
| D. | 從反應開始到平衡,用氫氣表示的平均反應速率為0.225 mol/(L•min) |
分析 A、反應物的總能量大于生成物的總能量時,反應放熱;氣體分子數減少的反應為熵減的反應,根據△G=△H-T△S判斷;
B、再加入一定量CO2,平衡右移,以二氧化碳的量增加為主;
C、此反應為放熱反應,逆反應是吸熱反應,降低溫度,平衡左移;
D、根據反應速率V=$\frac{△C}{△t}$和反應速率之比等于計量數之比來計算.
解答 解:A、反應物的總能量大于生成物的總能量時,反應放熱,即△H<0;正反應方向的氣體分子數減少,氣體分子數減少的反應為熵減的反應,即△S<0,所以在低溫下能自發,故A錯誤;
B、再加入一定量CO2,平衡右移,以二氧化碳的量增加為主,則$\frac{n({CH}_{3}OH)}{n({CO}_{2})}$減小,故B錯誤;
C、此反應為放熱反應,逆反應是吸熱反應,降低溫度,平衡左移,K減小,故C錯誤;
D、從反應開始到平衡,用CH3OH表示的平均反應速率V(CH3OH)=$\frac{△C}{△t}$=$\frac{0.75mol/L}{10min}$=0.075mol/(L•min),而化學反應速率之比等于計量數之比,故V(H2)=3V(CH3OH)=0.225mol/(L•min),故D正確;
故選D.
點評 本題考查了根據圖象判斷反應吸放熱以及溫度的改變對K的影響,應注意的是K只受溫度的影響,其它因素的改變所引起的平衡的移動,K不變.


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案 優翼小幫手同步口算系列答案
優翼小幫手同步口算系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 甲基橙呈紅色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 無色透明的溶液中:MnO4-、SO42-、Na+、H+ | |
| D. | $\frac{KW}{c(H+)}$=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
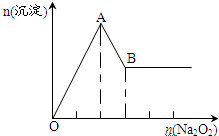 有一透明溶液,可能含有較大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一種或幾種,取此溶液做下列試驗
有一透明溶液,可能含有較大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一種或幾種,取此溶液做下列試驗查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 30mL | B. | 55mL | C. | 65mL | D. | 175mL |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時,負極反應為2n-2e-+20H一═Zn(OH)2 | |
| B. | 充電時,陰極pH增大 | |
| C. | 放電時,若有6mol電子轉移,則正極有10 mol OH一移向負極 | |
| D. | 充電時,陽極反應為Fe(OH)3+50H一+3e一=Fe042-+4H20 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 小蘇打和鹽酸反應:CO32-+2H+═CO2↑+H2O | |
| B. | 氫氧化鋁溶于強堿:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | 氫氧化鋇溶液與硫酸溶液反應:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸鈣與醋酸反應:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com