
分析 ①在酸性條件下,雙氧水氧化Cu,生成Cu2+,溶液變藍;
②此溫度下無水硫酸銅的溶解度為40g,可知140g硫酸銅溶液中有40g硫酸銅;則8.4g濾液含有硫酸銅為2.4g,有6g水;原本有水15g,則有15g-6g=9g水進入硫酸銅晶體中,可以計算出晶體中硫酸銅為16g,共含有硫酸銅為2.4g+16g=18.4g,進而求其物質的量.
解答 解:①在酸性條件下,雙氧水氧化Cu,生成Cu2+,溶液變藍,離子方程式為:Cu+H2O2+2H+=Cu2++2H2O;
故答案為:Cu+H2O2+2H+=Cu2++2H2O;
②此溫度下無水硫酸銅的溶解度為40g,可知140g硫酸銅溶液中有40g硫酸銅;則8.4g濾液含有硫酸銅為:$\frac{40g}{140g}=\frac{m}{8.4g}$,m=2.4g,有6g水;原本有水15g,則有15g-6g=9g水進入硫酸銅晶體中,可以計算出晶體中硫酸銅為16g,共含有硫酸銅為2.4g+16g=18.4g,其物質的量為0.115mol;
故答案為:0.115mol.
點評 本題以氧化還原反應為載體考查離子方程式的書寫,溶解度的相關計算,注意硫酸銅分為兩部分,一部分存在于藍色晶體中,一部分存在于濾液中.


 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:選擇題
| A. | ≥1.68L | B. | >1.68L | C. | ≤1.68L | D. | <1.68L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
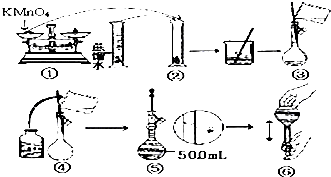 人體血液里Ca2+離子的濃度一般采用g/cm3來表示.抽取一定體積的血樣,加適量的草酸銨[(NH4)2C2O4]溶液,可析出草酸鈣(CaC2O4)沉淀,將此草酸鈣沉淀洗滌后溶于強酸可得一種弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可測定血液樣品中Ca2+的濃度.某研究性學習小組設計如下實驗步驟測定血液樣品中Ca2+的濃度:
人體血液里Ca2+離子的濃度一般采用g/cm3來表示.抽取一定體積的血樣,加適量的草酸銨[(NH4)2C2O4]溶液,可析出草酸鈣(CaC2O4)沉淀,將此草酸鈣沉淀洗滌后溶于強酸可得一種弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可測定血液樣品中Ca2+的濃度.某研究性學習小組設計如下實驗步驟測定血液樣品中Ca2+的濃度:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2X2+3Y2?2X2Y3 | B. | 3X2+2Y2?2X3Y2 | C. | X2+2Y22?XY2 | D. | 2X2+Y2?2X2Y |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液中c(H+)和c(OH-)都減小 | B. | 溶液中c(H+)增大 | ||
| C. | 醋酸電離平衡向左移動 | D. | 溶液的pH增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸化學式 | CH3COOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | 1mol•L-1的溶液中,pH(HCN)>pH(H2CO3)>pH(CH3COOH) | |
| B. | 升高溫度,HCN溶液中HCN的電離平衡正向移動,電離平衡常數增大 | |
| C. | 0.2mol/L醋酸溶液與0.1mol/L醋酸溶液中c(H+)之比小于2:1 | |
| D. | 飽和H2CO3溶液中c(H+)與c(CO32-)的比值小于2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上用二氧化硅在高溫下與焦炭反應,生成單質硅和二氧化碳的原理,制取粗硅 | |
| B. | 手指不慎被玻璃劃傷流血,可向傷口上涂FeCl3溶液,是因為FeCl3溶液可殺菌消毒 | |
| C. | 2014年山東萊蕪共出現284天霧霾天氣,對煤進行液化和氣化等物理變化的處理,可減少霧霾天氣的發生 | |
| D. | 白酒放置一定時間香味更濃,是因為白酒中乙醇與少量的有機酸反應生成有香味的酯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
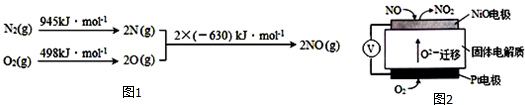
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com