
| A. | 原子半徑A>B>C>D | |
| B. | 原子序數d>c>b>a | |
| C. | 離子半徑C>D>B>A | |
| D. | 單質的還原性A>B離子的還原性C2?>D? |
分析 短周期元素的離子:aA2+、bB+、cC2-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+2=d+1,且A、B在周期表中C、D的下一周期,原子序數:a>b>d>c,結合元素周期律遞變規律解答該題.
解答 解:短周期元素的離子:aA2+、bB+、cC2-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+2=d+1,且A、B在周期表中C、D的下一周期,原子序數:a>b>d>c,
A、A、B在周期表中C、D的下一周期,并且原子序數:a>b>d>c,原子核外電子層數越多,半徑越大,同周期元素原子序數越大,半徑越小,則有原子半徑:B>A>C>D,故A錯誤;
B、aA2+、bB+、cC2-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+2=d+1,所以原子序數為a>b>d>c故B錯誤;
C、aA2+、bB+、cC2-、dD-都具有相同的電子層結構,核電荷數越大,離子半徑越小,核電荷數a>b>d>c,所以離子半徑C2->D->B+>A2+,故C正確;
D、同周期自左而右元素金屬性減弱,單質還原性減弱,則單質的還原性:B>A,同周期自左而右元素非金屬性增強,陰離子的還原性減弱,則還原性為C2?>D?,故D錯誤;
故選C.
點評 本題考查位置結構性質的相互關系及應用,根據核外電子排布確定元素所在周期表中的位置,清楚元素周期律的遞變規律是解答該題的關鍵,難度不大.


 課時訓練江蘇人民出版社系列答案
課時訓練江蘇人民出版社系列答案科目:高中化學 來源: 題型:選擇題
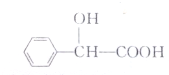 某有機物的結構如下所示,有關該物質的說法錯誤的是( )
某有機物的結構如下所示,有關該物質的說法錯誤的是( )| A. | 該物質的分子式為C8H8O3 | |
| B. | 該物質分子中的8個碳原子都在同一個平面上 | |
| C. | 該物質既可以發生酯化反應又可以發生縮聚反應 | |
| D. | 1mol該物質可以與2mol金屬Na反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 時間/min | 0 | 20 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.020 | 0.020 | 0.020 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②⑤⑦ | B. | ②③④⑤⑥ | C. | ③④⑥ | D. | ②③④⑥⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X、Y、Z的濃度相等 | B. | X、Y、Z在容器中共存 | ||
| C. | 正、逆反應速率都等于零 | D. | X、Y、Z的濃度均不再改變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2CH3 | B. | (CH3)3CCH2CH2CH3 | C. | CH3CH2OH | D. | CH3OCH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 配位體是Cl-和H2O,配位數是9 | |
| B. | 中心離子是Ti4+,配離子是[TiCl(H2O)5]2+ | |
| C. | 內界和外界中的Cl-的數目比是1:2 | |
| D. | 加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氨水能跟氯化亞鐵溶液反應生成氫氧化亞鐵 | |
| B. | 0.1mol/L氯化銨溶液的pH約為5 | |
| C. | 0.1mol/L氨水可以使酚酞試液變紅 | |
| D. | 銨鹽受熱易分解 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com