
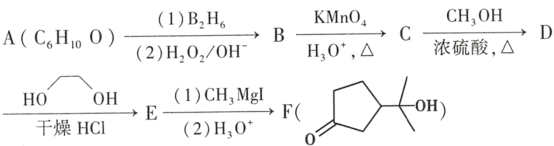
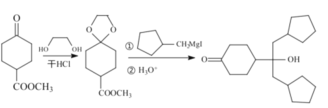
【題目】酯類化合物與格氏試劑(RMgX,X=Cl、Br、I)的反應是合成叔醇類化合物的重要方法,可用于制備含氧多官能團化合物。化合物F的合成路線如圖:
已知:
① RCH=CH2 ![]() RCH2CH2OH
RCH2CH2OH
②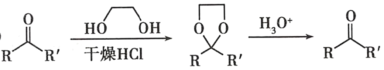
③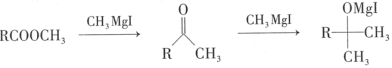
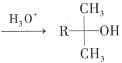
(1)A的結構簡式為_____。
(2)B→C的反應類型為_____。
(3)C中官能團的名稱為_____。
(4)C→D的化學方程式為_____。
(5)寫出符合下列條件的D的同分異構體_____(填結構簡式,不考慮立體異構)。
①含有五元環(huán)碳環(huán)結構;
②能與NaHCO3溶液反應放出CO2氣體;
③能發(fā)生銀鏡反應。
(6)D→E的目的是_____。
(7)已知羥基能與格氏試劑發(fā)生反應。寫出以 ![]() 、CH3OH 和格氏試劑為原料制備
、CH3OH 和格氏試劑為原料制備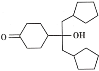 的合成路線(其他試劑任選)_____。
的合成路線(其他試劑任選)_____。
【答案】![]() 氧化反應 羰基和羧基
氧化反應 羰基和羧基 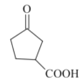 +CH3OH
+CH3OH![]()
 +H2O
+H2O 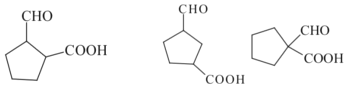 保護D中酮羰基,使其在E→F的轉化過程中不參與反應
保護D中酮羰基,使其在E→F的轉化過程中不參與反應 
![]()
![]()
【解析】
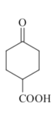
根據(jù)反應條件可知A發(fā)生信息①中的反應生成B,可知A中含有碳碳雙鍵,B含有羥基。B中羥基被酸性高錳酸鉀氧化后酸化生成C,C與甲醇發(fā)生酯化反應生成D,說明C中含有羧基,D發(fā)生信息②中的第一步反應生成E,E先發(fā)生信息③中反應,再發(fā)生信息②中第二步反應重新引入羰基生成F,由F的結構結合A的分子式逆推可得A為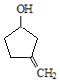 ,故B為
,故B為 、C為
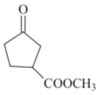
、C為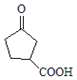 、D為
、D為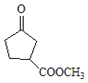 、E為
、E為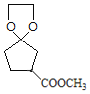 。
。
(1)根據(jù)分析可知A的結構簡式為![]() ;
;
(2)B到C羥基轉化為羧基,屬于氧化反應;
(3)C為 ,其官能團為羰基、羧基;
,其官能團為羰基、羧基;
(4)C到D為酯化反應,化學方程式為 +CH3OH
+CH3OH![]()
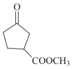 +H2O;
+H2O;
(5)D為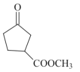 ,其同分異構體滿足::①含有五元環(huán)碳環(huán)結構;②能與NaHCO3溶液反應放出CO2氣體,說明含有羧基,③能發(fā)生銀鏡反應,說明含有醛基,則符合條件的同分異構體為:
,其同分異構體滿足::①含有五元環(huán)碳環(huán)結構;②能與NaHCO3溶液反應放出CO2氣體,說明含有羧基,③能發(fā)生銀鏡反應,說明含有醛基,則符合條件的同分異構體為: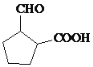 、
、 、
、![]() ;
;
(6)根據(jù)信息③可知酮羰基也可以需CH3MgI反應,而目標產(chǎn)物含有酮羰基,所以D→E的目的是保護D中酮羰基,使其在E→F的轉化過程中不參與反應;
(7)參考生成F的轉化,![]() 用酸性高錳酸鉀溶液氧化生成
用酸性高錳酸鉀溶液氧化生成![]() ,然后與乙醇反應生成
,然后與乙醇反應生成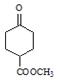 ,再與乙二醇生成
,再與乙二醇生成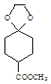 ,最后與
,最后與![]() 反應后酸性水解生成目標物,所以合成路線流程圖為:
反應后酸性水解生成目標物,所以合成路線流程圖為:
![]()

![]()
 。
。


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業(yè)考試導與練系列答案
初中學業(yè)考試導與練系列答案科目:高中化學 來源: 題型:
【題目】下列說法錯誤的是( )
A.用惰性電極電解 Na2SO4 溶液,當 2 mol 電子轉移時,可加入 18 g 水恢復
B.用惰性電極電解 1 L 1 mol/L CuSO4 溶液,當加入 1 mol Cu(OH)2 恢復電解前濃度時, 電路中轉移了 4 mol e-
C.用惰性電極電解 1 mol CuSO4 和 1 mol NaCl 的混合溶液,溶液的 pH 先減小后增大
D.要想實現(xiàn) Cu+H2SO4(稀) ═ CuSO4+H2↑的反應,需在電解池中進行,且 Cu 為陽極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,甲、乙兩個裝置的燒杯中分別盛有足量的CuCl2溶液。
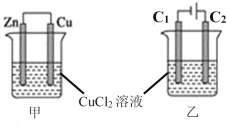
(1)甲裝置中,Zn電極發(fā)生______反應(填“氧化”或“還原”),溶液中Cl-向_____極(填“Zn”或“Cu”)移動,Zn電極反應式為_______,若反應過程中有0.1mol電子發(fā)生轉移,則Cu極質量增加__________。
(2)乙裝置中,石墨電極C1是_______極,現(xiàn)象是______,C2極電極反應式為_______,若反應過程中陰極析出12.8g的Cu,則陽極產(chǎn)生的氣體在標準狀況下的體積為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組中兩個變化所發(fā)生的反應,屬于同一類型的是
A.由苯制硝基苯、由乙醇制取乙酸乙酯
B.乙烯使溴的CCl4溶液褪色、甲苯使酸性高錳酸鉀水溶液褪色
C.由HO-CH2-COOH制![]() 、由氯乙烯制聚氯乙烯
、由氯乙烯制聚氯乙烯
D.由氯乙烷制乙烯、由溴乙烷制乙醇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗內(nèi)容能達到實驗目的的是
實驗目的 | 實驗內(nèi)容 | |
A | 鑒別乙醇與乙醛 |
|
B | 比較乙酸、碳酸、苯酚的酸性 |
|
C | 說明烴基對羥基上氫原子活性的影響 | |
D | 說明苯環(huán)對取代基上氫原子活性的影響 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有X、Y、Z三種短周期元素,X的氣態(tài)氫化物化學式為H2X,此氫化物的式量與X最最高價氧化物的式量之比為17∶ 40,X原子核內(nèi)質子數(shù)與中子數(shù)相等,Y與X可以形成離子化合物Y2X,Y的陽離子電子層結構與Ne相同,乙與X同周期,其氣態(tài)單質是雙原子分子,兩原子共用1對電子。試回答:
(1)寫出各元素符號:X__________、Y_________、Z__________。
(2)X離子的結構簡圖為____________________。X與Y形成的離子化合物的化學式為___________________,Z和氫形成的化合物的化學式為________________。
(3)Y單質在空氣中燃燒的化學方程式為 __________________________________,生成物與水反應的化學方程式為_________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鄰羥基桂皮酸(IV)是合成香精的重要原料,下列為合成鄰羥基桂皮酸(IV)的路線之一。
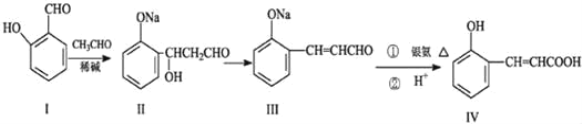
試回答:
(1)Ⅰ中官能團的名稱______。
(2)Ⅱ→Ⅲ的反應類型______。
(3)①IV與乙醇在濃硫酸作用下發(fā)生酯化反應的方程式______。
②Ⅳ與過量NaOH溶液反應的化學方程式______。
(4)有機物X與IV互為同分異構體,且X有如下特點:
①是苯的對位取代物,②能與NaHCO3反應放出氣體,③能發(fā)生銀鏡反應。請寫出X的兩種結構簡式_______;
(5)下列說法正確的是_______。
A.Ⅰ的化學式為C7H8O2
B.Ⅰ遇氯化鐵溶液呈紫色
C.Ⅱ能與NaHCO3溶液反應
D.1mol有機物IV最多能與4molH2加成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】制燒堿所用鹽水需兩次精制。第一次精制主要是用沉淀法除去粗鹽水中Ca2+、Mg2+、Fe3+、SO![]() 等離子,過程如下:
等離子,過程如下:
Ⅰ. 向粗鹽水中加入過量BaCl2溶液,過濾;
Ⅱ. 向所得濾液中加入過量Na2CO3溶液,過濾;
Ⅲ. 濾液用鹽酸調節(jié)pH,獲得一次精制鹽水。
(1)過程Ⅰ除去的離子是______。
(2)過程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
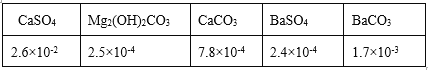
①檢測Fe3+是否除盡的方法是______。
②過程Ⅰ選用BaCl2而不選用CaCl2,運用表中數(shù)據(jù)解釋原因______。
③除去Mg2+的離子方程式是______。
④檢測Ca2+、Mg2+、Ba2+是否除盡時,只需檢測Ba2+即可,原因是_____。
(3)第二次精制要除去微量的I-、IO![]() 、NH
、NH![]() 、Ca2+、Mg2+,流程示意如下:
、Ca2+、Mg2+,流程示意如下:
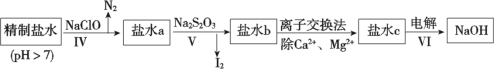
① 過程Ⅳ除去的離子是______。
② 鹽水b中含有SO![]() 。Na2S2O3將IO
。Na2S2O3將IO![]() 還原為I2的離子方程式是________ 。
還原為I2的離子方程式是________ 。
③ 過程VI中,在電解槽的陽極發(fā)生反應的電極方程式是:_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組用如圖裝置研究氣體X的性質,氣體X的主要成分是Cl2,其中含有少量水蒸氣。請回答下列問題:

(1)分別描述B、C裝置中的現(xiàn)象____;結合化學方程式及物質性質說明B、C裝置中現(xiàn)象不同的原因____。
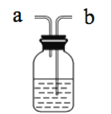
(2)Cl2是有毒氣體,為了防止多余Cl2污染空氣,可以在D處用如圖裝置進行尾氣處理,用化學方程式表示該原理____。氣體應該由____(填“a”或“b”)管通入。若要吸收224mLCl2(標況下),至少需要1mol/L的上述溶液____mL。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com