


| 實驗內容 | 實驗現象 | |
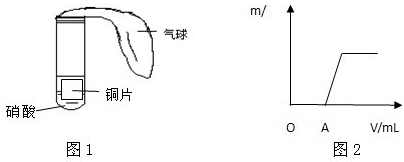
| A | 收集一集氣瓶氣體,觀察顏色,然后向瓶內倒入約占瓶容積1/5的蒸餾水,充分振蕩. | 蒸餾水呈淺黃綠色,瓶內氣體仍呈黃綠色. |
| B | 取出瓶內部分溶液,滴入紫色石蕊試液中直至過量. | 紫色石蕊試液先變紅色,后紅色褪色. |
| C | 取出瓶內剩下的部分溶液,滴入硝酸銀溶液中. | 產生大量白色沉淀 |
| D | 最后向瓶內倒入少量濃氫氧化鈉溶液,振蕩. | 瓶內黃綠色氣體立即消失. |
| ||

| ||
 ;
;

 寒假樂園北京教育出版社系列答案
寒假樂園北京教育出版社系列答案科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
(21分)
(1)在上面元素周期表中全部是金屬元素的區域為 。
(a)A (b)B (c)C (d)D
(2)現有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,乙元素原子核外M電子層與K電子層上的電子數相等。
①用元素符號將甲、乙兩元素填寫在上面元素周期表中對應的位置。
②甲、乙兩元素相比較,金屬性較強的是 (填名稱),可以驗證該結論的實
驗是 。
(a)將在空氣中放置已久的這兩種元素的塊狀單質分別放入熱水中
(b)將這兩種元素的單質粉末分別和同濃度的鹽酸反應
(c)將這兩種元素的單質粉末分別和熱水作用,并滴入酚酞溶液
(d)比較這兩種元素的氣態氫化物的穩定性
③寫出甲的氧化物及氧化物對應水化物分別與強堿反應的離子方程式
、 。
(3)表中所列小寫字母分別代表一種化學元素:
①m、f、j的單質熔點由高到低的順序___________________________(填元素符號)。
②以上元素形成的金屬單質中,熔點最低的是____________________(填元素符號)。
③f、m、n、g所形成的氫化物的穩定性還性由強到弱的順序為
____________________________________________________________(填化學式);
④甲、乙、c、d、e形成的簡單離子的半徑由小到大的順序為
___________________________________________________________。
⑤f元素單質是在生產中用量很大,試寫出工業上制備f元素單質的化學方程式
_____________________________________________________________________。
⑥c元素的單質用途_______________________________________________(填一條)。
查看答案和解析>>
科目:高中化學 來源:09—10年成都石室中學高一下期期末考試化學卷 題型:填空題
(21分)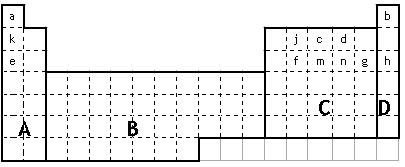
(1)在上面元素周期表中全部是金屬元素的區域為 。


(a)A (b)B (c)C (d)D
(2)現有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,乙元素原子核外M電子層與K電子層上的電子數相等。
①用元素符號將甲、乙兩元素填寫在上面元素周期表中對應的位置。
②甲、乙兩元素相比較,金屬性較強的是 (填名稱),可以驗證該結論的實
驗是 。
(a)將在空氣中放置已久的這兩種元素的塊狀單質分別放入熱水中
(b)將這兩種元素的單質粉末分別和同濃度的鹽酸反應
(c)將這兩種元素的單質粉末分別和熱水作用,并滴入酚酞溶液
(d)比較這兩種元素的氣態氫化物的穩定性
③寫出甲的氧化物及氧化物對應水化物分別與強堿反應的離子方程式
、 。


(3)表中所列小寫字母分別代表一種化學元素:
①m、f、j的單質熔點由高到低的順序___________________________(填元素符號)。
②以上元素形成的金屬單質中,熔點最低的是____________________(填元素符號)。
③f、m、n、g所形成的氫化物的穩定性還性由強到弱的順序為
____________________________________________________________(填化學式);
④甲、乙、c、d、e形成的簡單離子的半徑由小到大的順序為
___________________________________________________________。
⑤f元素單質是在生產中用量很大,試寫出工業上制備f元素單質的化學方程式
_____________________________________________________________________。
⑥c元素的單質用途_______________________________________________(填一條)。
查看答案和解析>>
科目:高中化學 來源:09-10年成都石室中學高一下期期末考試化學卷 題型:填空題
(21分)
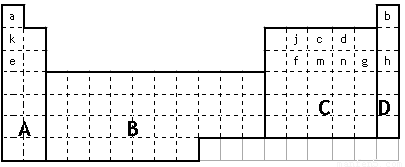
(1)在上面元素周期表中全部是金屬元素的區域為
。

(a)A (b)B (c)C (d)D
(2)現有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,乙元素原子核外M電子層與K電子層上的電子數相等。
①用元素符號將甲、乙兩元素填寫在上面元素周期表中對應的位置。
②甲、乙兩元素相比較,金屬性較強的是 (填名稱),可以驗證該結論的實
驗是 。
(a)將在空氣中放置已久的這兩種元素的塊狀單質分別放入熱水中
(b)將這兩種元素的單質粉末分別和同濃度的鹽酸反應
(c)將這兩種元素的單質粉末分別和熱水作用,并滴入酚酞溶液
(d)比較這兩種元素的氣態氫化物的穩定性
③寫出甲的氧化物及氧化物對應水化物分別與強堿反應的離子方程式
、
。
(3)表中所列小寫字母分別代表一種化學元素:
①m、f、j的單質熔點由高到低的順序___________________________(填元素符號)。
②以上元素形成的金屬單質中,熔點最低的是____________________(填元素符號)。
③f、m、n、g所形成的氫化物的穩定性還性由強到弱的順序為
____________________________________________________________(填化學式);
④甲、乙、c、d、e形成的簡單離子的半徑由小到大的順序為
___________________________________________________________。
⑤f元素單質是在生產中用量很大,試寫出工業上制備f元素單質的化學方程式
_____________________________________________________________________。
⑥c元素的單質用途_______________________________________________(填一條)。
查看答案和解析>>
科目:高中化學 來源: 題型:

(1)在上面元素周期表中全部是金屬元素的區域為 。
(a)A (b)B (c)C (d)D
(2)現有甲、乙兩種短周期元素,室溫下,甲元素單質在冷的濃硫酸或濃硝酸中,表面都生成致密的氧化膜,乙元素原子核外M電子層與K電子層上的電子數相等。
①用元素符號將甲、乙兩元素填寫在上面元素周期表中對應的位置。
②甲、乙兩元素相比較,金屬性較強的是 (填名稱),可以驗證該結論的實
驗是 。
(a)將在空氣中放置已久的這兩種元素的塊狀單質分別放入熱水中
(b)將這兩種元素的單質粉末分別和同濃度的鹽酸反應
(c)將這兩種元素的單質粉末分別和熱水作用,并滴入酚酞溶液
(d)比較這兩種元素的氣態氫化物的穩定性
③寫出甲的氧化物及氧化物對應水化物分別與強堿反應的離子方程式
、 。
(3)表中所列小寫字母分別代表一種化學元素:
①m、f、j的單質熔點由高到低的順序___________________________(填元素符號)。
②以上元素形成的金屬單質中,熔點最低的是____________________(填元素符號)。
③f、m、n、g所形成的氫化物的穩定性還性由強到弱的順序為
____________________________________________________________(填化學式);
④甲、乙、c、d、e形成的簡單離子的半徑由小到大的順序為
___________________________________________________________。
⑤f元素單質是在生產中用量很大,試寫出工業上制備f元素單質的化學方程式
_____________________________________________________________________。
⑥c元素的單質用途_______________________________________________(填一條)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com