
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
分析 混合物26g與足量稀硫酸反應,產生標況下H211.2L,氫氣物質的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,26g金屬提供電子物質的量為0.5mol×2=1mol,故提供1mol電子需要金屬的平均質量為26g,計算各金屬提供1mol電子需要的質量,結合平均量進行解答.
解答 解:混合物26g與足量稀硫酸反應,產生標況下H211.2L,氫氣物質的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,26g金屬提供電子物質的量為0.5mol×2=1mol,故提供1mol電子需要金屬的平均質量為26g,
Fe在反應中表現+2價,提供1mol電子需要Fe的質量為56g×$\frac{1mol}{2}$=28g,
Mg在反應中表現+2價,提供1mol電子需要Mg的質量為24g×$\frac{1mol}{2}$=12g,
Al在反應中表現+3價,提供1mol電子需要Al的質量為27g×$\frac{1mol}{3}$=9g,
Cu不稀硫酸反應產生氫氣,提供1mol電子需要Cu的質量為無窮大,
故兩兩混合,可能的組合為:Cu與Mg、Cu與Al、Fe與Mg、Fe與Al,共4種,
故選C.
點評 本題考查混合物的有關計算,題目難度中等,注意平均值與極限法相結合的利用,從而簡化計算,注意若有不反應的金屬應視作需金屬質量無窮大,試題培養了學生的化學計算能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C |
| D |
| A. | C的非金屬性最強,可與E元素形成共價化合物 | |
| B. | 元素D可形成三種價態的酸,且酸根離子均能促進水的電離 | |
| C. | 原子半徑由大到小的排列順序為:E>D>B>A>C | |
| D. | C、D元素形成的最簡單的氫化物的熱穩定性:D<C |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 煤的干餾是煤氣化的重要方法,也是煤綜合利用最“古老”的、最簡單的方法.某實驗小組根據教材習題設計了煤干餾實驗,裝置如圖所示.實驗時,取約2-3g的煤粒,在研體中研磨至粉末狀態;用藥匙將煤粉放入試管中,在具支試管中加入2mL水,按照如圖所示安裝好裝置;點燃酒精燈,對試管預熱后再集中受熱,待具支試管中氣泡產生的速度均勻后,在具支試管口收集氣體,并用明火靠近具支試管口,可以觀察到產生的氣體能夠燃燒.根據上述實驗回答下列問題:
煤的干餾是煤氣化的重要方法,也是煤綜合利用最“古老”的、最簡單的方法.某實驗小組根據教材習題設計了煤干餾實驗,裝置如圖所示.實驗時,取約2-3g的煤粒,在研體中研磨至粉末狀態;用藥匙將煤粉放入試管中,在具支試管中加入2mL水,按照如圖所示安裝好裝置;點燃酒精燈,對試管預熱后再集中受熱,待具支試管中氣泡產生的速度均勻后,在具支試管口收集氣體,并用明火靠近具支試管口,可以觀察到產生的氣體能夠燃燒.根據上述實驗回答下列問題: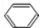 +HNO3$→_{△}^{濃硫酸}$
+HNO3$→_{△}^{濃硫酸}$ +H2O;
+H2O;
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
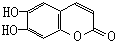 )具有抗癌作用.下列關于七葉樹內酯的敘述中不正確的是( )
)具有抗癌作用.下列關于七葉樹內酯的敘述中不正確的是( )| A. | 能被KMnO4酸性溶液氧化 | |
| B. | 既可以看成酚類化合物又可看成酯類化合物 | |
| C. | 能與銀氨溶液發生銀鏡反應 | |
| D. | 1 mol該物質最多與3 mol Br2 發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相對分子質量最小的化合物分子式是CH2O | |
| B. | 相對分子質量最小的化合物分子式是C2H2O | |
| C. | 含相同碳原子數的各化合物,其相對分子質量之差是16的整數倍 | |
| D. | 含相同碳原子數的各化合物,其相對分子質量之差是18的整數倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,0.1molC8H18所含有的共價鍵數目為2.5NA | |
| B. | 1L 1 mol•L-1 FeCl3溶液完全水解產生的Fe(OH)3膠體粒子數為NA | |
| C. | 氫氧燃料電池正極消耗22.4L氣體時,電路中通過的電子數目為4NA | |
| D. | 28.6gNa2CO3•10H2O溶于水配成1L溶液,該溶液中陰離子數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | 密度(g/ml-3) | 沸點(℃) | 水溶性 | 溶解性 |
| 甲 | 0.7893 | 78.5 | 溶 | 溶于乙 |
| 乙 | 1.220 | 100.7 | 溶 | 溶于甲 |
| A. | 分液 | B. | 蒸餾 | C. | 干餾 | D. | 萃取 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com