
【題目】下列敘述正確的是
A.在酒精燈加熱條件下,Na2CO3、NaHCO3固體都能發生分解
B.Cl2是一種有毒氣體,不可用于自來水的殺菌消毒
C.SiO2既能和NaOH溶液反應又能和氫氟酸反應,所以是兩性氧化物
D.Na2SiO3水溶液俗稱水玻璃,是制備硅膠和木材防火劑等的原料
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】A、B、C、D是原子序數依次增大的四種短周期元素,甲、乙、丙、丁、戊是由其中的兩種或三種元素組成的化合物,己是由C元素形成的單質,已知甲+乙=丁+己,甲+丙=戊+己,0.1mol·L-1丁溶液的pH為13(25℃)。下列說法正確的是
A. 原子半徑:D>C >B>A
B. B元素只能形成一種二元含氧酸,且B元素的含氧酸對應的酸酐一定是氧化物
C. 1mol甲與足量乙反應轉移電子的數目為NA
D. 1.0L 0.1mol·L-1戊溶液中陰離子總的物質的量小于0.1mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向一定量的 Fe、FeO、![]() 的混合物中,加入 100mL1mol/L 的鹽酸,恰好使混合物完全溶解,放出224mL(標準狀況)的氣體,所得溶液中,加入 KSCN 溶液無血紅色出現。若用足量的 CO 在高溫下還原 相同質量的混合物,能得到鐵的質量為( )
的混合物中,加入 100mL1mol/L 的鹽酸,恰好使混合物完全溶解,放出224mL(標準狀況)的氣體,所得溶液中,加入 KSCN 溶液無血紅色出現。若用足量的 CO 在高溫下還原 相同質量的混合物,能得到鐵的質量為( )
A.2.8gB.5.6gC.11.2gD.無法計算
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家研發了一種室溫下“可呼吸”的Na—CO2二次電池。將NaClO4溶于有機溶劑作為電解液,鈉和負載碳納米管的鎳網分別作為電極材料,電池的總反應為:3CO2+4Na![]() 2Na2CO3+C。下列說法錯誤的是
2Na2CO3+C。下列說法錯誤的是

A. 放電時,ClO4-向負極移動
B. 充電時釋放CO2,放電時吸收CO2
C. 放電時,正極反應為:3CO2+4e =2CO32-+C
D. 充電時,正極反應為:Na++e=Na
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某鋁土礦中主要含有Al2O3、Al(OH)3還含有Fe2O3等雜質。利用拜耳法生產氧化鋁的流程如圖所示:
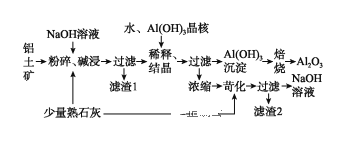
請回答下列問題:
(1)粉碎后的鋁土礦堿浸時應在較高溫度下進行,其目的是____________________。濾渣1的主要成分為________________。
(2)Al2O3與NaOH溶液反應的離子方程式為____________________________________。
(3)加Al(OH)3晶核的目的是促進Al(OH)3的析出。上述“稀釋、結晶”工藝,也可用通入足量的_________氣體的方法來代替。(已知:通入該氣體后,其產物之一可用來做發酵粉)。
(4)焙燒過程中發生的化學方程式為_________________________________。
(5)濃縮所得的NaOH溶液由于吸收了空氣中的CO2而含有雜質,該雜質可通過苛化(即與少量熟石灰反應)反應除去,寫出苛化反應的化學方程式:_________________________________________________。
(6)該生產流程能實現____________________(填化學式)的循環利用。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電子工業常用30%的FeCl3溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。
(1)寫出FeCl3溶液與金屬銅發生反應的化學方程式:______________________。
(2)某工程師為了從使用過的腐蝕廢液(主要含CuCl2、FeCl3溶液等)中回收銅,并重新獲得純凈的FeCl3溶液,準備采用如圖所示流程:(已知:加過量①為Fe;加過量④為稀鹽酸;通入⑥為Cl2)
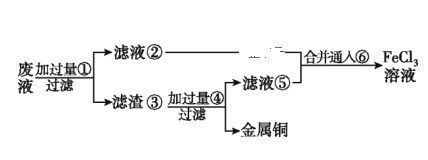
①上述實驗中濾渣③的主要物質為___________________(填化學式),寫出向②⑤的合并液中通入⑥的離子方程式:______________________________。
②配制并保存FeCl2溶液時,需加入鐵屑,其目的是_______________________________。
③要證明FeCl3溶液是否含有Fe2+,可選擇下列選項中的______________(已知:加入該物質后,生成藍色沉淀)。
A.加入 K3[Fe(CN)6]溶液 B.加入NaOH溶液 C.加入KSCN溶液
(3)現有1.2 L含3 mol FeCl2的酸性溶液恰好與0.6 mol HIO3完全反應,還原產物為_______(填化學式,已知該物質遇淀粉溶液變藍),該反應離子方程式為___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】明礬可用于制取鉀肥和冶煉鋁,具體工藝流程如下圖所示:
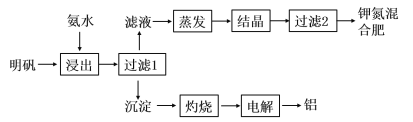
(1)“浸出”反應的離子方程式為__________________________________。“浸出”所用稀氨水濃度為6mol/L,則配制100mL該氨水需12mol/L的濃氨水的體積為______mL,若量取該濃氨水時俯視刻度線,會導致配制的稀氨水濃度________(填“偏高”、“偏低”或“無影響”)。
(2)檢驗“過濾1”所得沉淀是否洗凈的實驗方法是_______________________________。
(3)請寫出“電解”熔融氧化鋁制取金屬鋁的化學方程式________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳及其化合物廣泛存在于自然界中。回答下列問題:
(1)基態碳原子核外有________種能量不同的電子, 其核外電子運動狀態由_____ 種因素決定。
(2)CH4分子間不能形成氫鍵, 主要原因是CH4 分子中的碳原子不含孤對電子、_____ 、 _____________。
(3)碳酸的非羥基氧的個數和磷酸的非羥基氧的個數都是1, 從結構上分析,它們的強度 相近,均為中強酸。然而事實上二氧化碳水溶液的酸性卻很弱,原因是__________。
(4)乙二胺(H2NCH2CH2NH2)是 一種有機化合物, N 原子的雜化軌道類型為______,乙二胺通過配位鍵能與Cu2+ 形成穩定的環狀配離子,其結構可表示為__________。
(5)金剛石是碳的一種同素異形體,屬于_______ 晶體。已知金屬鈉的晶胞(體心立方堆積)沿其體對角線垂直在紙平面上的投影圖如圖A 所示,則金剛石晶胞沿其體對角線垂直在紙平面上的投影圖應該是下圖 ___________(從 A~D 圖中選填).
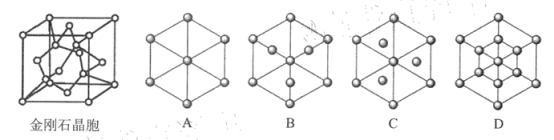
若碳原子半徑為r ,金剛石晶胞中碳原子的空間占有率為_____________( 用含π 的代數.式表示).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】石油是工業的血液,與我們的生產、生活息息相關。
(1)乙烯是石油化工重要的基礎原料。 寫出乙烯的電子式____________
(2)分子式為C5H12的某烴,分子中含有4個甲基,該烴的結構簡式為_______________________。
(3)與乙烯互為同系物的是_______ 。(選填編號)
a. CH3CH=CH2 b. CH2=CHCH=CH2
c. CH≡CH d. CH3CH3
(4)聚乙烯安全無毒,可用于制食品包裝袋。聚乙烯的結構簡式為 ________________ 。
(5)乙炔三聚可得到苯或二乙烯基乙炔 (CH2=CH-C-C-CH=CH2) 。鑒別苯和二乙烯基乙炔可用的試劑是__________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com