
【題目】對于數以千萬計的化學物質和為數眾多的化學反應,分類法的作用幾乎是無可代替的。
Ⅰ.現有以下物質:①H2O ②Cu ③BaCO3 ④Fe(OH)3膠體 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物質中屬于混合物的是________(填序號,下同),屬于電解質的是________。
(2)向④中逐滴滴加⑦,可觀察到的現象是_____________________。
Ⅱ.雖然分類的方法不同,但四種基本反應類型和離子反應、氧化還原反應之間也存在著一定的關系。
(3)下圖為離子反應、氧化還原反應和置換反應三者之間的關系,其中表示離子反應的是________(填字母)。
![]()
(4)有同學認為所有酸堿中和反應均可表示為H++OH-=H2O。請舉個例子反駁上述觀點(用離子方程式表示)_____________。
【答案】④⑦ ①① 先出現紅褐色沉淀,后沉淀溶解,得到黃色溶液 C Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
【解析】
I.(1)由多種物質組成的是混合物;在水溶液中或熔融狀態下能導電的化合物為電解質;
(2)電解質溶液能使膠體發生聚沉;
II.(3)所有的置換反應全是氧化還原反應,置換反應中有部分是離子反應,部分是非離子反應,氧化還原反應中,有部分是離子反應,部分是非離子反應;
(4)該離子反應表示強酸、強堿混合生成弱電解質水且不生成其它沉淀的反應。
I.(1)由多種物質組成的是混合物,④⑦是混合物;在水溶液中或熔融狀態下能導電的化合物為電解質,①③為電解質;②Cu是金屬單質,不屬于電解質,也不是非電解質;⑤酒精和⑥CO2都是化合物,二者都屬于非電解質;故屬于混合物的是④⑦;屬于電解質的是①③;
(2)電解質溶液能使膠體發生聚沉,故向氫氧化鐵膠體中加入稀硫酸能發生膠體聚沉產生氫氧化鐵紅褐色沉淀;繼續滴加稀硫酸,則氫氧化鐵沉淀與硫酸發生酸堿中和反應產生可溶性的Fe2(SO4)3而使沉淀溶解,得到黃色溶液,故反應現象是先出現紅褐色沉淀,后沉淀溶解,得到黃色溶液;
Ⅱ.(3)所有的置換反應全是氧化還原反應,與氧化還原反應的關系是被包含和包含的關系,所以A是氧化還原反應,B是置換反應,離子反應有的是氧化還原反應,有的是置換反應,所以C是離子反應;
(4)離子反應H++OH-=H2O表示強酸、強堿混合生成可溶性強電解質和弱電解質水的反應,若是弱酸、弱堿發生的中和反應,或者酸堿中和反應生成的鹽是難溶性的沉淀,則不能用此離子方程式來表示,例如H2SO4、Ba(OH)2發生的中和反應的離子方程式為Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O。


科目:高中化學 來源: 題型:
【題目】下列離子方程式中書寫正確的是( )
A.用小蘇打治療胃酸過多:![]()
B.氫氧化鋇溶液與稀硫酸反應:![]()
C.碳酸氫鈣溶液和氫氧化鈉溶液混合:![]()
D.銅片插入硝酸銀溶液中:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:將Cl2通入適量KOH溶液中,產物中可能含有KCl、KClO、KClO3,且![]() 的值與溫度高低有關。當n(KOH)=a mol時,下列說法不正確的是
的值與溫度高低有關。當n(KOH)=a mol時,下列說法不正確的是
A.參加反應的氯氣的物質的量等于![]() a mol
a mol
B.改變溫度,產物中KClO3的最大理論產量為![]() a mol
a mol
C.改變溫度,反應中轉移電子的物質的量n(e-)的范圍為![]() a mol≤n(e-)≤
a mol≤n(e-)≤![]() a mol
a mol
D.若某溫度下,反應后![]() =11,則溶液中
=11,則溶液中![]() =
=![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了探究幾種氣態氧化物的性質,某同學設計了以下實驗:用三只集氣瓶收集二氧化硫、二氧化氮氣體,倒置在水槽中。然后,分別緩慢通入適量氧氣或氯氣,如圖所示。一段時間后,A、B裝置中集氣瓶充滿溶液,C裝置中集氣瓶里還有氣體。

(1)如果裝置A中通入的氧氣恰好使液體充滿集氣瓶,假設瓶內液體不擴散。
①寫出A中總反應的化學方程式:________;該實驗對工業上生產硝酸的啟示是________。
②假設該實驗條件下,氣體摩爾體積為aL·mol-1,集氣瓶中溶液的物質的量濃度為________。
(2)實驗前在C水槽里滴加幾滴紫色石蕊試液,通入氧氣前后,實驗現象變化可能為___________;寫出化學方程式:________,溶液充滿集氣瓶后,在B水槽里滴加硝酸鋇溶液,可能觀察到的現象為___________;寫出所有反應的離子方程式:_________;證明B水槽反應后溶液里有氯離子的操作方法是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表隱含著許多信息和規律。以下所涉及的元素均為中學化學中常見的短周期元素,其原子半徑及主要化合價列表如下,其中R2Q2用于呼吸面具或潛水艇中作為氧氣來源。

下列說法正確的是
A. T、Z的最高價氧化物對應水化物的酸性T<Z
B. R、X、Y的單質失去電子能力最強的是X
C. M與Q形成的是離子化合物
D. M、Q、Z都在第2周期
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若 m g Na在足量氯氣中燃燒,生成固體的質量為(m+3.55)g,則 m g Na與氧氣反應,生成的固體的質量為:①2.7g、②3.1g、③3.55g、④3.9g、⑤4.0g( )
A.①②③B.②③④C.③④⑤D.①③⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將0.1mol的KCl和0.1mol的AlCl3溶于水配成100mL混合溶液,下列溶液中Cl-濃度與該混合溶液中Cl-濃度相等的是
A. 3mol/L的NaCl溶液 B. 2mol/L的FeCl3溶液
C. 2mol/L的MgCl2溶液 D. 2mol/L的NaCl溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知圖一表示的是可逆反應 CO(g)+H2(g)![]() C(s)+H2O(g)-Q(Q>0)的化學反應速率(v)與時間(t)的關系,圖二表示的是可逆反應2NO2(g)
C(s)+H2O(g)-Q(Q>0)的化學反應速率(v)與時間(t)的關系,圖二表示的是可逆反應2NO2(g)![]() N2O4(g)+Q(Q>0)的濃度(c)隨時間 t 的變化情況,下列 說法中正確的是
N2O4(g)+Q(Q>0)的濃度(c)隨時間 t 的變化情況,下列 說法中正確的是
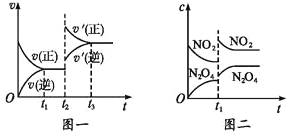
A.圖一 t2 時刻改變的條件可能是升高了溫度或增大了壓強
B.圖一 t2 時刻改變的條件可能是通入了 CO 氣體
C.圖二 t1 時刻改變的條件可能是升高了溫度或增大了壓強
D.圖二 t1 時刻改變的條件是增大壓強,則混合氣體的平均相對分子質量將減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(15分)“套管實驗”是將一支較小的試管裝入另一試管中,經組裝來完成原來需要兩只或更多試管進行的實驗。因其有許多優點,近年來被廣泛開發并應用于化學實驗中。下面這個實驗為“套管實驗”,實驗裝置如下圖,小試管中部有沾上無水硫酸銅粉末的脫脂棉。請觀察實驗裝置,分析實驗原理,并回答下列問題:
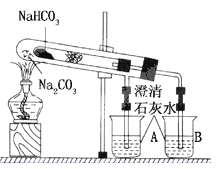
(1)整個實驗過程中,能觀察到的現象為
①燒杯A中________;②小試管中________;
③燒杯B中____________________________;
(2)實驗結束時,在操作上要特別注意的問題是
____________________________________________________________________
(3)寫出實驗過程中發生反應的化學方程式
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com