
科目:高中化學 來源:廣西南寧沛鴻民族中學2010-2011學年高二下學期期中考試化學文科試題 題型:013
|
往2 L密閉容器中充入8.0 mol氣態反應物A,2 min后,測得A還剩余2.0 mol,則2 min內A的化學反應速率為 | |
| [ ] | |
A. |
1.0 mol/(L·min) |
B. |
1.5 mol/(L·min) |
C. |
2.0 mol/(L·min) |
D. |
3.0 mol/(L·min) |
查看答案和解析>>
科目:高中化學 來源:浙江省余姚中學2011-2012學年高二下學期第一次質檢化學試題 題型:022
工業合成氨與制備硝酸一般可連續生產,流程如下:
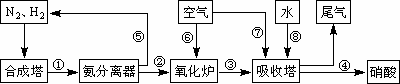
(1)工業生產時,制取氫氣的一個反應為:CO+H2O(g)![]() CO2+H2.t℃時,往1 L密閉容器中充入0.2 mol CO和0.3 mol水蒸氣.反應建立平衡后,體系中c(H2)=0.12 mol·L-1.該溫度下此反應的平衡常數K=________(填計算結果).
CO2+H2.t℃時,往1 L密閉容器中充入0.2 mol CO和0.3 mol水蒸氣.反應建立平衡后,體系中c(H2)=0.12 mol·L-1.該溫度下此反應的平衡常數K=________(填計算結果).
(2)合成塔中發生反應N2(g)+3H2(g)![]() 2NH3(g) ΔH<0.下表為不同溫度下該反應的平衡常數.由此可推知,表中T1________300℃(填“>”、“<”或“=”).
2NH3(g) ΔH<0.下表為不同溫度下該反應的平衡常數.由此可推知,表中T1________300℃(填“>”、“<”或“=”).
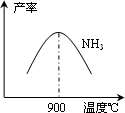
(3)N2和H2在鐵作催化劑作用下從145℃就開始反應,不同溫度下NH3產率如圖所示.溫度高于900℃時,NH3產率下降的原因________.
(4)在上述流程圖中,氧化爐中發生反應的化學方程式為________.
(5)硝酸廠的尾氣直接排放將污染空氣.目前科學家探索利用燃料氣體中的甲烷等將氮的氧化物還原為氮氣和水,反應機理為:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
則甲烷直接將NO2還原為N2的熱化學方程式為:________.
(6)氨氣在純氧中燃燒,生成一種單質和水,試寫出該反應的化學方程式________,科學家利用此原理,設計成氨氣-氧氣燃料電池,則通入氨氣的電極是________(填“正極”或“負極”);堿性條件下,該電極發生反應的電極反應式為________.
查看答案和解析>>
科目:高中化學 來源:福建省廈門六中2011-2012學年高二下學期期中考試化學試題 題型:022
工業合成氨與制備硝酸一般可連續生產,流程如下:
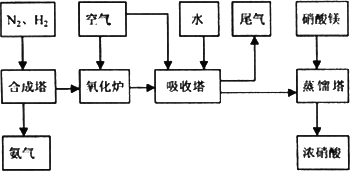
(1)工業生產時,制取氫氣的一個反應為:CO+H2O![]() CO2+H2,
CO2+H2,
①t℃時,往1 L密閉容器中充人0.2 mol CO和0.3 mol水蒸氣,反應建立平衡后,體系中c(H2)=0.12 mol·L-1,該溫度下此反應的平衡常數K=________;(請填數字不必帶單位)
②保持溫度不變,向上述平衡體系中再加入0.1 mol CO,當反應重新建立平衡時,水蒸氣的總轉化率α(H2O)=________.
(2)合成塔中發生反應為:
N2(g)+3H2(g)![]() 2NH3(g);ΔH<0
2NH3(g);ΔH<0
下表為不同溫度下該反應的平衡常數.由此可推知,表中T1________573K(填“>”、“<”或“=”).
在生產中,若要增大H2的轉化率,在其他條件不變的情況下可以采取的措施為________(填字母).
A.加入一定量H2
B.加入一定量N2
C.將生成的氣體NH3液化分離
D.升高溫度
(3)NH3和O2在鉑系催化劑作用下從145℃就開始反應:
4NH3+5O2![]() 4NO+6H2O;△H=-905 kJ·mol-1,不同溫度下NO產率如圖所示,溫度高于900℃時,NO產率下降的原因________.
4NO+6H2O;△H=-905 kJ·mol-1,不同溫度下NO產率如圖所示,溫度高于900℃時,NO產率下降的原因________.

(4)吸收塔中反應為:3NO2+H2O![]() 2HNO3+NO.從生產流程看,吸收塔中需要補充空氣,其原因是________
2HNO3+NO.從生產流程看,吸收塔中需要補充空氣,其原因是________
查看答案和解析>>
科目:高中化學 來源: 題型:
(15分)工來合成氨與制備硝酸一般可連續生產,流程如下:
(1)工來生產時,制取氫氣的一個反應為:![]() ,
,
①t℃時,往l L密閉容器中充人0.2 mol CO和0.3 mol水蒸氣,反應建立平衡后,體系中c(H2)=0.12 mol?L-1,該溫度下此反應的平衡常數K= ;
②保持溫度不變,向上述平衡體系中再加入0.1 mol CO,當反應重新建立平衡時,水蒸氣的總轉化率![]() (H2O)= 。
(H2O)= 。
T(K) | T1 | 573 | T2 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
(2)合成塔中發生反應為:
![]()
![]()
 右表為不同溫度下該反應的平衡常數。由此可推知,表中T1 573K(填“>”、“<”或“=”)。
右表為不同溫度下該反應的平衡常數。由此可推知,表中T1 573K(填“>”、“<”或“=”)。
(3)NH3和O2在鉑系催化劑作用下從145℃就開始反應:
![]() 4NH3+5O2
4NH3+5O2![]() NO+6H2O AH=-905kJ?mol-1,不同溫度下NO產率如圖所示,溫度高于900℃時,NO產率下降的原因 。
NO+6H2O AH=-905kJ?mol-1,不同溫度下NO產率如圖所示,溫度高于900℃時,NO產率下降的原因 。
![]() (4)吸收塔中反應為:3NO2+H2O
(4)吸收塔中反應為:3NO2+H2O![]() 2HNO3+NO。從生產流程看,吸收塔中需要補充空氣,其原因是
2HNO3+NO。從生產流程看,吸收塔中需要補充空氣,其原因是
![]() (5)硝酸廠的尾氣含有氮氧化物,不經處理直接排放將污染空氣。目前科學家探索利用燃料氣體中的甲烷將氮氧化物還原為氮氣和水,其反應機理為:
(5)硝酸廠的尾氣含有氮氧化物,不經處理直接排放將污染空氣。目前科學家探索利用燃料氣體中的甲烷將氮氧化物還原為氮氣和水,其反應機理為:
![]() CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ![]() H=-574kJ?mol-1。;
H=-574kJ?mol-1。;
![]() CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ![]() H=-1160 kJ?mol-1;
H=-1160 kJ?mol-1;
則甲烷直接將NO2還原為N2的熱化學方程式為: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com