
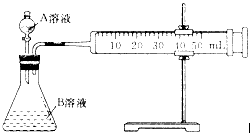

 H2C2O4溶液,另取兩支試管各加入
H2C2O4溶液,另取兩支試管各加入 KMnO4溶液。將四支試管分成兩組(各有一支盛有H2C2O4溶液和KMnO4溶液的試管),一組放入冷水中,另一組放入熱水中,經過一段時間后,分別混合并振蕩,記錄溶液褪色所需時間。該實驗試圖探究__________對化學反應速率的影響,但該組同學始終沒有看到溶液褪色,其原因是_____________________________________。
KMnO4溶液。將四支試管分成兩組(各有一支盛有H2C2O4溶液和KMnO4溶液的試管),一組放入冷水中,另一組放入熱水中,經過一段時間后,分別混合并振蕩,記錄溶液褪色所需時間。該實驗試圖探究__________對化學反應速率的影響,但該組同學始終沒有看到溶液褪色,其原因是_____________________________________。 科目:高中化學 來源: 題型:

| 氫氧化物開始沉淀時的pH | 氫氧化物沉淀完全時的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
 Fe2+(aq)+3OH-(aq)
Fe2+(aq)+3OH-(aq) Fe2+(aq)+3OH-(aq)
Fe2+(aq)+3OH-(aq)| 物質 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
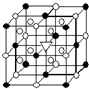 A.(1)右圖所示為冰晶石(化學式為Na3AlF6)的晶胞.圖中●位于大立方體頂點和面心,○位于大立方體的12條棱的中點和8個小立方體的體心,▽圖中●、○中的一種.圖中●、○分別指代哪種粒子
A.(1)右圖所示為冰晶石(化學式為Na3AlF6)的晶胞.圖中●位于大立方體頂點和面心,○位于大立方體的12條棱的中點和8個小立方體的體心,▽圖中●、○中的一種.圖中●、○分別指代哪種粒子| 熔點/K | 沸點/K | 標準狀況時在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
查看答案和解析>>
科目:高中化學 來源: 題型:
 和
和 ;“雙烯合成反應”又稱為“Diels-Alder反應”,如:
;“雙烯合成反應”又稱為“Diels-Alder反應”,如: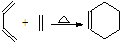 .
. ,則物質A的結構式為:
,則物質A的結構式為: 或CH2=CH-COOH
或CH2=CH-COOH 或CH2=CH-COOH
或CH2=CH-COOH

 中,D物質可發生反應生成一種生活中常用高分子,其化學方程式為:
中,D物質可發生反應生成一種生活中常用高分子,其化學方程式為:



 和
和 都是無色液體,下列物質中可以用來鑒別這兩種物質的是
都是無色液體,下列物質中可以用來鑒別這兩種物質的是查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 綠礬晶體(FeSO4?7H2O)在醫藥上作補血劑.某同學用KMnO4溶液滴定綠礬晶體(FeSO4?7H2O)樣品(雜質不與 KMnO4反應),對鐵元素含量進行測定.
綠礬晶體(FeSO4?7H2O)在醫藥上作補血劑.某同學用KMnO4溶液滴定綠礬晶體(FeSO4?7H2O)樣品(雜質不與 KMnO4反應),對鐵元素含量進行測定.查看答案和解析>>
科目:高中化學 來源:2013-2014學年福建省莆田市高三3月質量檢測化學試卷(解析版) 題型:填空題
(13分)鐵和鐵的化合物在工業生產和日常生活中都有廣泛的用途。
(1)在定向爆破中,常利用氧化鐵與鋁反應放出的熱量來切割鋼筋,該反應的化學方程式為__。
(2)已知:2Fe2O3(s)+3C(s)=3CO2(g)+4Fe(s)? △H=+468.2 kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1。
則Fe(s)與O2 (g)反應生成Fe2 O3 (s)的熱化學方程式為______________________。
(3)可用KMnO4溶液滴定Fe2+的濃度,反應的離子方程式如下:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①KMnO4溶液應盛放在_____滴定管中;
②判斷達到滴定終點的現象是_____;
③用硫酸酸化的0.020 00 mol·L-1。KMnO4溶液滴定某FeSO4溶液至終點,實驗數據記錄如下表:
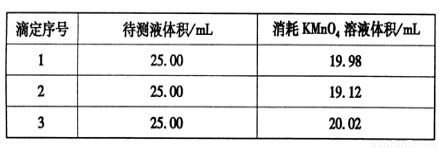
請分析數據并計算,該FeSO4溶液的物質的量濃度為_____。
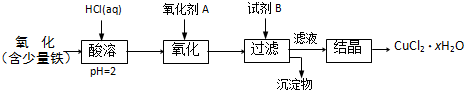
(4)新型納米材料ZnFe2Ox,可用于除去工業廢氣中的某些氧化物。制取新材料和除去廢氣的轉化關系如下圖:
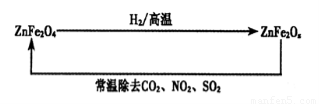
①已知ZnFe2O4與H2反應的物質的量之比為2:1,則ZnFe2Ox中x=_____;
②用ZnFe2Ox除去SO2的過程中,氧化劑是_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com