
【題目】下列說法不正確的是( )
A.已知冰的熔化熱為![]()
![]() ,冰中氫鍵鍵能為20
,冰中氫鍵鍵能為20![]() ,假設1mol冰中有2mol氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中
,假設1mol冰中有2mol氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中![]() 的氫鍵
的氫鍵
B.已知:![]() 石墨
石墨![]() ,
,![]()
![]() .
.![]() ,
,![]()
![]() .
.![]() 石墨
石墨![]() ,
,![]()
![]() .則
.則![]() ,
,![]()
![]()
C.實驗測得環己烷![]() 、環己烯
、環己烯![]() 和苯
和苯![]() 的標準燃燒熱分別為
的標準燃燒熱分別為![]()
![]() 、
、![]()
![]() 和
和![]()
![]() ,可以證明在苯分子中不存在獨立的碳碳雙鍵
,可以證明在苯分子中不存在獨立的碳碳雙鍵
D.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為![]() ,
,![]() 若加入少量醋酸鈉固體,則
若加入少量醋酸鈉固體,則![]() 向左移動,
向左移動,![]() 減小,Ka變小
減小,Ka變小
【答案】D
【解析】
![]() 冰是由水分子通過氫鍵形成的分子晶體,冰的熔化熱為
冰是由水分子通過氫鍵形成的分子晶體,冰的熔化熱為![]() ,1mol冰變成
,1mol冰變成![]() 的液態水所需吸收的熱量為
的液態水所需吸收的熱量為![]() ,全用于打破冰的氫鍵,冰中氫鍵鍵能為
,全用于打破冰的氫鍵,冰中氫鍵鍵能為![]() ,1mol冰中含有2mol氫鍵,需吸收
,1mol冰中含有2mol氫鍵,需吸收![]() 的熱量,
的熱量,![]() 由計算可知,最多只能打破1mol冰中全部氫鍵的
由計算可知,最多只能打破1mol冰中全部氫鍵的![]() ,故A正確;
,故A正確;
B.![]() 石墨
石墨![]() ;
;![]()
![]()
![]() ;
;![]()
![]()
![]() 石墨
石墨![]() ;
;![]()
![]()
![]() ;
;![]()
![]()
根據蓋斯定律,方程式![]() 可由
可由![]() 可得,
可得, ![]()
![]()
![]()
![]()
![]() ,故B正確;
,故B正確;
C.實驗測得環己烷![]() 和環己烯
和環己烯![]() 的標準燃燒熱分別為
的標準燃燒熱分別為![]() 和
和![]() ,1mol環己烯
,1mol環己烯![]() 與環己烷
與環己烷![]() 相比,形成1mol碳碳雙鍵,能量降低169kJ,假如苯分子中有獨立的碳碳雙鍵,苯
相比,形成1mol碳碳雙鍵,能量降低169kJ,假如苯分子中有獨立的碳碳雙鍵,苯![]() 與環己烷
與環己烷![]() 相比,形成三個碳碳雙鍵,則能量應降低
相比,形成三個碳碳雙鍵,則能量應降低![]() ,而實際測得苯的燃燒熱僅為3265
,而實際測得苯的燃燒熱僅為3265![]() ,能量降低了3916
,能量降低了3916![]()
![]() ,遠大于
,遠大于![]() ,充分說明苯分子不是環己三烯的結構,可以證明在苯分子中不存在獨立的碳碳雙鍵,故C正確;
,充分說明苯分子不是環己三烯的結構,可以證明在苯分子中不存在獨立的碳碳雙鍵,故C正確;
D.Ka是電離常數,是弱電解質達電離平衡時的平衡常數,在一定溫度下,與濃度無關.Ka的計算用溶液中電離出來的各離子濃度乘積與溶液中未電離的電解質分子濃度的比值,一定溫度下,醋酸溶液的物質的量濃度為c,電離度為![]() ,
,![]() 醋酸電離出的
醋酸電離出的![]() 和
和![]() 濃度均為
濃度均為![]() ,溶液中未電離的電解質分子濃度為
,溶液中未電離的電解質分子濃度為![]() ,故題中
,故題中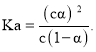 若加入少量醋酸鈉固體,
若加入少量醋酸鈉固體,![]() 增大了
增大了![]() 的濃度,
的濃度,![]() 向左移動,
向左移動,![]() 減小,但是溫度不變,則Ka不變,故D錯誤。
減小,但是溫度不變,則Ka不變,故D錯誤。
答案:D。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是
A. 水、乙醇、乙酸都屬于弱電解質
B. 苯與氯氣生成 的反應屬于取代反應
的反應屬于取代反應
C. 分子式為C9H12的芳香烴共有8種
D. 淀粉、油脂、蛋白質都屬于高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸溶液中存在電離平衡CH3COOH![]() H++CH3COO-,下列敘述不正確的是( )
H++CH3COO-,下列敘述不正確的是( )
A.升高溫度,平衡正向移動,醋酸的電離常數Ka值增大
B.0.10mol/L的CH3COOH溶液中加水稀釋,溶液中c(OH-)增大
C.CH3COOH溶液中加少量的CH3COONa固體,平衡逆向移動
D.25℃時,欲使醋酸溶液pH、電離常數Ka和電離程度都減小,可加入少量冰醋酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,甲池的總反應式為:N2H4+O2=N2+H2O,下列關于該電池工作時的說法正確的是( )

A. 該裝置工作時,Ag電極上有氣體生成
B. 甲池中負極反應為N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均減小
D. 當甲池中消耗0.1molN2H4時,乙池中理論上最多產生6.4g固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列反應的熱化學方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
則反應4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H為
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁是應用廣泛的金屬。以鋁土礦(主要成分為Al2O3,含SiO2和Fe2O3等雜質)為原料制備鋁的一種工藝流程如下:

注:SiO2在“堿溶”時轉化為鋁硅酸鈉沉淀。
(1)“堿溶”時生成偏鋁酸鈉的離子方程式為_____________________。
(2)向“過濾Ⅰ”所得濾液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不變”或“減小”)。
(3)“電解Ⅰ”是電解熔融Al2O3,電解過程中作陽極的石墨易消耗,原因是___________。
(4)“電解Ⅱ”是電解Na2CO3溶液,原理如圖所示。陽極的電極反應式為_____________________,陰極產生的物質A的化學式為____________。

(5)鋁粉在1000℃時可與N2反應制備AlN。在鋁粉中添加少量NH4Cl固體并充分混合,有利于AlN的制備,其主要原因是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,某同學設計了一個甲醚(CH3OCH3)燃料電池并探究氯堿工業原理和粗銅的精煉原理,乙裝置中X為陽離子交換膜。根據要求回答下列相關問題:
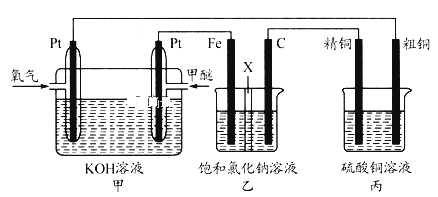
(1)寫出甲中負極的電極反應式__。
(2)反應一段時間后,乙裝置中生成NaOH主要在___(填“鐵極”或“石墨極”)區。
(3)如果粗銅中含有鋅、銀等雜質,丙裝置中陽極上電極反應式為___,反應一段時間,硫酸銅溶液濃度將___(填“增大”“減小”或“不變”)。
(4)若在標準狀況下,有2.24L氧氣參加反應,則乙裝置中鐵電極上生成的氣體在標準狀況下的體積為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列各圖的敘述不正確的是( )
化學方程式 | 平衡常數K |
F2 + H2 = 2HF | 6.5×1095 |
Cl2 + H2 = 2HCl | 2.6×1033 |
Br2 + H2 = 2HBr | 1.9×1019 |
I2 + H2 = 2HI | 8.7×102 |
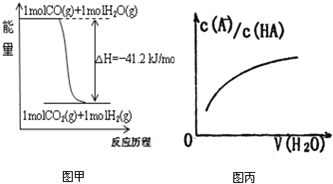
A.已知CO的燃燒熱283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,則圖甲表示CO和H2O(g)生成CO2和H2的能量變化
B.某溫度下,pH =11的NH3H2O和pH =1的鹽酸等體積混合后(不考慮混合后溶液體積的變化)恰好完全反應,反應后的溶液中NH4+、NH3H2O與NH3三種微粒的平衡濃度之和為0.05molL-1
C.在常溫下,X2(g) 和 H2反應生成HX的平衡常數如表乙所示,僅依據K的變化,就可以說明在相同條件下,平衡時X2(從F2到I2)的轉化率逐漸降低,且X2與H2反應的劇烈程度逐漸減弱
D.圖丙中曲線表示常溫下向弱酸HA的稀溶液中加水稀釋過程中,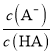 的變化情況
的變化情況
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是部分短周期元素原子半徑與原子序數的關系,則下列說法正確的是( )

A.M在周期表中的位置為:第三周期,IV族
B.Y、Z、M、N四種元素形成的原子半徑最大的是Y
C.X、N兩種元素的氣態氫化物的沸點相比,前者較低
D.Y元素和X元素可以形成Y2X2型化合物,陰、陽離子物質的量之比為1:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com