
將7 mol N2和11 mol H2在適宜條件下按下式進行反應N2+3H2![]() 2NH3,當在某一溫度下達到化學平衡狀態,試解答:
2NH3,當在某一溫度下達到化學平衡狀態,試解答:
(1)若測得平衡混合氣體對空氣的相對密度為0.6時,求N2的轉化率.
(2)若測得平衡混合氣體對空氣的相對密度為0.47時,求N2的轉化率.
 每課必練系列答案
每課必練系列答案科目:高中化學 來源:四川省成都外國語學校2011屆高三10月月考化學試題 題型:022
在一定溫度下
,把2 mol N2和6 mol H2通入一個體積不變的密閉容器中(如圖)發生以下的反應: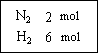
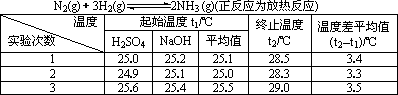
若反應達到平衡后,測得混和氣體為7 mol,據此回答下列問題:保持上述反應溫度不變,使a、b、c分別代表初始加入的N2、H2和NH3的物質的量,如果反應達到平衡后混和氣體中各物質的物質的量分數仍與上述平衡時完全相同,那么:
(1)若a=1 mol,c=2 mol,則b=________mol,在此情況下,反應起始時將向________方向進行(填“正”或“逆”)
(2)若規定起始時反應向逆反應方向進行,則c的范圍是________.
(3)在上述裝置中,若需控制平衡后的混和氣體的物質的量為6.5 mol,則可采取的措施是________.
查看答案和解析>>
科目:高中化學 來源:山東省臨沂高新區實驗中學2008-2009學年高三12月月考化學試題 人教版 人教版 題型:022
合成氨工業對化學工業和國防工業具有重要意義.
(1)常溫下氨氣極易溶于水,其水溶液可以導電.
①用方程式表示氨氣溶于水的過程中存在的可逆過程__________________
②氨水中水電離出的c(OH-)________10-7 mol/L(填寫“>”、“<”或“=”)
③將相同體積、相同物質的量濃度的氨水和鹽酸混合后,溶液中離子濃度由大到依次為________.
(2)氨氣具有還原性,在銅的催化作用下,氨氣和氟氣反應生成A和B.A為銨鹽,B在標準狀況下為氣態.在此反應中,若每反應1體積氨氣,同時反應0.75體積氟氣;若每反應8.96 L氨氣(標準狀況),同時生成0.3 mol A.
①寫出氨氣和氟氣反應的化學方程式________;
②在標準狀況下,每生成1 mol B,轉移電子的物質的量為________mol.
(3)Ⅰ在某壓強恒定的密閉容器中加入2 mol N2和4 mol H2,發生如下反應:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
達到平衡時,體積為反應前的三分之二.求:
①達到平衡時,N2的轉化率為________.
②若向該容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均>0,在相同條件下達到平衡時,混合物中各組分的物質的量與上述平衡相同.試比較反應放出的能量:①________②(填“>”、“<”或“=”)
Ⅱ若將2 mol N2和4 mol H2放入起始體積相同的恒容容器中,在與Ⅰ相同的溫度下達到平衡.
③試比較平衡時NH3的濃度:Ⅰ________Ⅱ(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化學 來源:江西省白鷺洲中學2012屆高三上學期期中考試化學試題 題型:022
硝酸是一種重要的化工原料,工業上生產硝酸的主要過程如下:
(1)以N2和H2為原料合成氨氣.反應為:N2(g)+3H2(g)![]() 2NH3(g);ΔH<0.
2NH3(g);ΔH<0.
①下列措施可以提高H2的轉化率的是(填選項序號)________.
a.選擇適當的催化劑
b.增大壓強
c.及時分離生成的NH3
d.升高溫度
②一定溫度下,在密閉容器中充入1 mol N2和3 mol H2發生反應.若容器容積恒定,達到平衡狀態時,氣體的總物質的量是原來的![]() ,則N2的轉化率α1=________;若容器壓強恒定,達到平衡狀態時,N2的轉化率為α2,則α2________α1(填“>”、“<”或“=”).
,則N2的轉化率α1=________;若容器壓強恒定,達到平衡狀態時,N2的轉化率為α2,則α2________α1(填“>”、“<”或“=”).
(2)以氨氣、空氣為主要原料制硝酸.
在容積恒定的密閉容器中進行反應2NO(g)+O2(g)![]() 2NO2(g);ΔH>0.
2NO2(g);ΔH>0.
該反應的反應速率(v)隨時間(t)變化的關系如圖所示.若t2,t4時刻只改變一個條件,下列說法正確的是(填選項序號)________.

a.在t1~t2時,可依據容器內氣體的壓強保持不變判斷反應已達到平衡狀態
b.在t2時,采取的措施可以是升高溫度
c.在t3~t4時,可依據容器內氣體的密度保持不變判斷反應已達到平衡狀態
d.在t5時,容器內NO2的體積分數是整個過程中的最大值
(3)硝酸廠常用如下2種方法處理尾氣.
①催化還原法:催化劑存在時用H2將NO2還原為N2.
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-483.6 kJ/mol
N2(g)+2O2(g)=2NO2(g);ΔH=+67.7 kJ/mol
則H2還原NO2生成水蒸氣反應的熱化學方程式是________.
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2.若9.2 g NO2和Na2CO3溶液完全反應時轉移電子0.1 mol,則反應的離子方程式是________.
查看答案和解析>>
科目:高中化學 來源:山西省太原市五中2009屆高三第二學期2月月考化學試題 題型:022
合成氨對工.農業生產和國防都有重要意義.
已知:N2(g)+H2(g)![]() 2NH3(g);ΔH=-92.4 kJ/mol請回答:
2NH3(g);ΔH=-92.4 kJ/mol請回答:
(1)合成氨對工業中采取的下列措施可以用勒夏特列原理解釋的是________(填字母).
a.用鐵觸媒加快化學反應速率
b.采用較高壓強(20M Pa-50M Pa)
c.將原料氣中的少量CO等氣體凈化出來
d.將生成的氨液化并及時從體系中分離出來
(2)一定溫度下,在密閉容器中充入1 mol N2和3 mol H2并發生反應.
①若容器容積恒定,達到平衡時,氣體的壓強為原來的7/8,則N2的轉化率α1=________,此時反應放出的熱量________kJ;
②若容器壓強恒定,則達到平衡時,容器中N2的轉化率=α2________α1(填“<”“>”或“=”)
(3)隨著對合成氨研究的發展,希臘科學家采用高質子導電性的SCY陶瓷(能傳遞H+)為介質,用吸附在它內外表面上的金屬鈀多晶薄膜做電極,實現了常壓.570℃條件下高轉化率的電解法合成氨(裝置如圖).鈀電極A是電解池的________極(填“陽”或“陰”),該極上的電極反應式是________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com