
【題目】已知Y、Z是金屬單質,F、M是極易溶于水的氣體,I元素是地殼中含量僅次于氧的非金屬元素,化合物L是一種可用于制造發動機的新型無機非金屬材料,其相對分子質量為140,其中I元素的質量分數為60%。這些物質間的相互轉化關系如框圖所示(部分產物已略去),根據框圖及提示的信息回答下列問題。

(1)寫出I元素在元素周期表中的位置_________________________________。
(2)K和F反應生成L和M的化學方程式_________________________________________。
(3)將5.2 g 金屬Z與足量的X的稀溶液充分反應無氣體放出,再向溶液中加入過量的NaOH溶液并加熱,收集到0.448L氣體F(標準狀況),則整個過程中轉移的電子數為_________。
(4)C是空氣質量報告中的一種氣體污染物,易形成酸雨;P氣體是形成另一類型酸雨的主要污染物。實驗室中若想用酸性高錳酸鉀溶液除盡P氣體,觀察到的現象應是____________________,寫出相應的離子方程式______________________________ 。
(5)已知向B的溶液中加入NaOH溶液時,先產生白色沉淀,迅速變為灰綠色,最后變為紅褐色,請寫出過量金屬Y與X的稀溶液充分反應的離子方程式 ______________,該反應中被還原的X與未被還原的X的物質的量之比為___________________
【答案】第三周期第IVA族 3SiCl4+4NH3=Si3N4+12HCl 0.16NA或9.632×1022 高錳酸鉀溶液紫色變淺 5 SO2+2 MnO![]() +2H2O=5 SO
+2H2O=5 SO![]() +2 Mn2++4H+ 3Fe+8H++2NO
+2 Mn2++4H+ 3Fe+8H++2NO![]() =3Fe2++2NO↑+4H2O 1:3
=3Fe2++2NO↑+4H2O 1:3
【解析】
I元素是地殼中僅次于O的非金屬元素,則I為Si元素;物質G與焦炭反應生成Si,說明物質G含有Si元素,物質G為SiO2,物質H為CO;Si與Cl2在加熱條件下生成物質K為SiCl4,SiCl4與物質F反應生成物質L和M,F為極易溶于水的氣體,可以有物質D與NaOH溶液在加熱條件下反應,說明物質F為NH3;化合物L是一種可用于制造發動機的新型無機非金屬材料,其相對分子質量為140,其中I元素的質量分數為60%,其另一種元素為N元素,則物質L為Si3N4,物質M為HCl;物質D含有銨根,X的稀溶液與金屬反應生成三種物質,說明X為硝酸,D為NH4NO3,物質Z與物質Y均可以與稀硝酸反應生成物質A,則物質A為水,物質E為Z的硝酸鹽,據此分析。
(1)根據分析,I為Si元素,其在元素周期表中的位置為第三周期第ⅣA族;
(2)根據分析,物質K與物質F反應生成物質L和物質M的化學方程式為3SiCl4+4NH3=Si3N4+12HCl;
(3)將5.2g金屬Z與足量的X的稀溶液充分反應無氣體放出,再向溶液中加入過量的NaOH溶液并加熱,收集到0.448L氣體F(標準狀況),物質F為![]() =0.02mol,0.02mol氨氣全部由硝酸根得電子發生還原反應而來,一個硝酸根得8個電子生成一個銨根,故反應過程中轉移電子8×0.02=0.16mol,為0.16NA個;
=0.02mol,0.02mol氨氣全部由硝酸根得電子發生還原反應而來,一個硝酸根得8個電子生成一個銨根,故反應過程中轉移電子8×0.02=0.16mol,為0.16NA個;
(4)C為空氣質量報告中的一種氣體污染物,易形成酸雨,則C為NO,則另一種氣體P為SO2,利用酸性高錳酸鉀除去SO2,反應方程式為5SO2+2![]() +2H2O=5
+2H2O=5![]() +2Mn2++4H+;反應現象為:高錳酸鉀溶液紫色變淺;
+2Mn2++4H+;反應現象為:高錳酸鉀溶液紫色變淺;
(6)向B的溶液中加入NaOH溶液時,先產生白色沉淀,迅速變為灰綠色,最后變為紅褐色,說明B中含有Fe2+,結合物質X,物質B為Fe(NO3)2,則過量金屬Y與X的稀溶液充分反應的離子方程式為3Fe+8H++2![]() =3Fe2++2NO↑+4H2O,反應過程中共有8mol
=3Fe2++2NO↑+4H2O,反應過程中共有8mol![]() 參加反應,反應生成2mol NO,有6mol硝酸根沒有被還原,故被還原的X與為被還原的X的物質的量的比為2:6=1:3。
參加反應,反應生成2mol NO,有6mol硝酸根沒有被還原,故被還原的X與為被還原的X的物質的量的比為2:6=1:3。


 輕松課堂單元期中期末專題沖刺100分系列答案
輕松課堂單元期中期末專題沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】有a、b、c、d四個金屬電極,有關的反應裝置及部分反應現象如下:
實驗裝置 |
|
|
|
|
部分實驗現象 | a極質量減小b極質量增加 | 溶液中的 | d極溶解c極有氣體產生 | 電子從d極流向a極 |
由此可判斷這四種金屬的活動性順序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作、現象和所得結論錯誤的是 ( )
選項 | 操作 | 現象 | 結論 |
A | 向蔗糖中加入濃硫酸 | 蔗糖變成疏松多孔的海綿狀炭,并放出有刺激性氣味的氣體 | 濃硫酸具有脫水性和強氧化性 |
B | 向久置的Na2SO3溶液中加入足量Ba(NO3)2溶液,再加入足量稀鹽酸 | 先出現白色沉淀,然后部分沉淀溶解 | 部分Na2SO3被氧化 |
C | 某溶液中滴加K3[Fe(CN)6]溶液 | 產生藍色沉淀 | 原溶液中有Fe2+,可能有Fe3+ |
D | 向等濃度的KCl、KI混合液中逐滴滴加AgNO3溶液 | 先出現黃色沉淀 | Ksp(AgCl)>Ksp(AgI) |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.甲醛在木材加工、醫藥等方面有重要用途。甲醇直接脫氫是工業上合成甲醛的新方法,制備過程涉及的主要反應如下:
反應I:CH3OH(g)![]() HCHO(g)+H2(g) ΔH1=+85.2kJ/mol
HCHO(g)+H2(g) ΔH1=+85.2kJ/mol
反應II:CH3OH(g)+![]() O2(g)
O2(g)![]() HCHO(g)+H2O(g) ΔH2
HCHO(g)+H2O(g) ΔH2
反應III:2H2(g)+O2(g)![]() 2H2O(g) ΔH3=—483.6kJ/mol
2H2O(g) ΔH3=—483.6kJ/mol
(1)計算反應Ⅱ的反應熱ΔH2=__________________。
(2)肌肉中的肌紅蛋白(Mb)可與O2結合生成MbO2:Mb(aq)+O2(g)![]() MbO2(aq),其中k正和k逆分別表示正反應和逆反應的速率常數,即υ正=k正·c(Mb)·P(O2),υ逆=k逆·c(MbO2)。37℃時測得肌紅蛋白的結合度(α)與P(O2)的關系如下表[結合度(α)指已與O2結合的肌紅蛋白占總肌紅蛋白的百分比]:
MbO2(aq),其中k正和k逆分別表示正反應和逆反應的速率常數,即υ正=k正·c(Mb)·P(O2),υ逆=k逆·c(MbO2)。37℃時測得肌紅蛋白的結合度(α)與P(O2)的關系如下表[結合度(α)指已與O2結合的肌紅蛋白占總肌紅蛋白的百分比]:
①計算37℃、P(O2)為2.00kPa時,上述反應的平衡常數K=_______。
P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
②導出平衡時肌紅蛋白與O2的結合度(α)與O2的壓強[P(O2)]之間的關系式α=_______(用含有k正、k逆的式子表示)。
II.CO2既是溫室氣體,也是重要的化工原料,以CO2為原料可合成多種有機物。
(3)CO2用于生產乙烯,已知:2CO2(g)+6H2(g)![]() CH2=CH2(g) + 4H2O(g) ΔH=QkJ/mol。一定條件下, 按不同的投料比X[X=
CH2=CH2(g) + 4H2O(g) ΔH=QkJ/mol。一定條件下, 按不同的投料比X[X=![]() ]向某容積可變的恒壓密閉容器中充入CO2、H2,測得不同投料比時CO2的轉化率與溫度的關系如圖所示。
]向某容積可變的恒壓密閉容器中充入CO2、H2,測得不同投料比時CO2的轉化率與溫度的關系如圖所示。

①X1______X2(填“>”或“<”,后同),Q______0。
②圖中A、B、C三點對應的平衡常數KA、KB、KC的大小關系為______。
(4)常溫下,用NaOH溶液作CO2捕捉劑不僅可以降低碳排放,而且可得到重要的化工產品Na2CO3和NaHCO3。
①已知25℃時0.1mol / L的NaHCO3溶液的pH=8.3,試通過計算確定溶液中各離子濃度由大到小的順序為_____[已知:常溫下H2CO3的電離常數Ka1= 4.4×107、Ka2 = 5×1011 ]。
②欲用5LNa2CO3溶液將23.3gBaSO4固體全都轉化為BaCO3,則所用的Na2CO3溶液的物質的量濃度至少為____。
[已知:常溫下Ksp(BaSO4)=1×107、Ksp(BaCO3)=2.5×106 ]。(忽略溶液體積的變化)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組設計如下實驗方案研究Cu與濃H2SO4的反應(裝置中的固定儀器和酒精燈均未畫出):
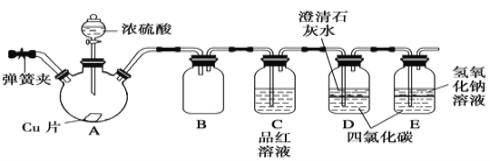
請回答下列問題:
(1)儀器A的名稱_________。Cu與濃H2SO4的反應的化學方程式為________________。
(2)D、E中CCl4的作用是___________________。
(3)加熱過程中,隨著反應的進行,A容器下有少量白色沉淀生成,你認為該沉淀物是_________,分析可能的原因是________________________________________。
(4)實驗結束,打開A容器上的彈簧夾,通入一段時間空氣,目的是______________。
(5)以下提供了三種制取CuSO4溶液的方法,你認為最合理的是____________(填序號),并且寫出該方法對應的化學方程式_____________________________。
① 用銅與濃硫酸制備硫酸銅溶液。
② 將銅片在空氣中加熱,再溶解在稀硫酸中即可得到硫酸銅溶液。
③ 在硫酸和銅的混合容器中滴加 H2O2 溶液,過濾得硫酸銅溶液。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用惰性電極電解足量下列溶液一段時間后,再加入一定量括號內的純凈物,能使溶液恢復到原來的成分和濃度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨電極為惰性電極,溶液中陽離子在陰極放電,陰離子在陽極放電。A、電解AgNO3溶液,Ag+在陰極放電生成Ag,OH-在陽極放電生成O2,且n(Ag)∶n(O2)=2∶1,則應加入Ag2O恢復濃度,故A錯誤;B、電解NaOH溶液,H+在陰極放電生成H2,OH-在陽極放電生成O2,且n(H2)∶n(O2)=2∶1,則應加入一定量的H2O恢復原樣,故B錯誤;C、電解KCl溶液,H+在陰極放電生成H2,Cl-在陽極放電生成Cl2,且n(H2)∶n(Cl2)=1∶1,則應加入一定量HCl恢復原樣,故C錯誤;D、電解CuSO4溶液,Cu2+在陰極放電生成Cu,OH-在陽極放電生成O2,且n(Cu)∶n(O2)=2∶1,則應加入一定量CuO恢復原樣,故D正確。故選D。
點睛:分析電解反應的原理,在兩極析出什么物質(固體或氣體),相當于什么物質脫離反應體系,根據元素守恒和原子比例,加入對應的物質,即可使溶液完全復原。
【題型】單選題
【結束】
28
【題目】工業上用電解法處理含鎳酸性廢水并得到單質Ni的原理如圖所示。下列說法不正確的是
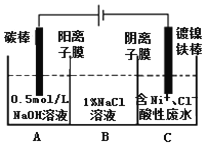
已知:①Ni2+在弱酸性溶液中發生水解
②氧化性:Ni2+(高濃度)>H+>Ni2+(低濃度)
A. 碳棒上發生的電極反應:4OH--4e-=O2↑+2H2O
B. 電解過程中,B中NaCl溶液的物質的量濃度將不斷減少
C. 為了提高Ni的產率,電解過程中需要控制廢水pH
D. 若將圖中陽離子膜去掉,將A、B兩室合并,則電解反應總方程式發生改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關有機物的敘述正確的是 ( )
A. C4H10有3種同分異構體
B. 葡萄糖、果糖的分子式均為C6H12O6,兩者互為同分異構體
C. 戊烷(C5H12)有4種同分異構體
D. 主鏈含5個碳原子,有3個甲基支鏈的烷烴有5種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NO2、O2和熔融KNO3可制作燃料電池,其原理如圖,該電池在使用過程中石墨I電極上生成氧化物Y,Y可循環使用。下列說法正確的是( )

A.O2在石墨Ⅱ附近發生氧化反應
B.該電池放電時NO3-向石墨Ⅱ電極遷移
C.石墨Ⅰ附近發生的反應:3NO2 +2e-=NO+ 2NO3-
D.相同條件下,放電過程中消耗的NO2和O2的體積比為4∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇既是重要的化工原料,又可作為燃料。利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主要反應如下:
①CO(g)+2H2(g)CH3OH(g)△H1
②CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)CO(g)+H2O(g)△H3
回答下列問題:
(1)已知△H1=﹣99kJ·mol﹣1,已知△H2=﹣58kJ·mol﹣1,則△H3=______kJ·mol﹣1。
(2)反應①的化學平衡常數K的表達式為______;圖1中能正確反映平衡常數K隨溫度變化關系的曲線為________(填曲線標記字母)。
(3)合成氣的組成n(H2)/n(CO+CO2)=2.60時體系中的CO平衡轉化率(a)與溫度和壓強的關系如圖2所示。a(CO)值隨溫度升高而________(填“增大”或“減小”)圖2中的壓強由大到小為________。
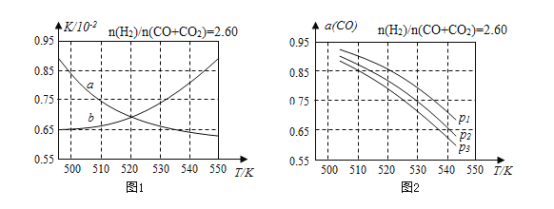
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com