
【題目】某學生以鐵絲和Cl2為原料進行下列三個實驗.從分類角度分析,下列選項正確的是( ) 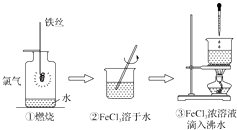
A.實驗①、②所涉及的物質均為電解質
B.實驗②、③均為放熱反應實驗
C.②、③均未發生氧化還原反應
D.實驗①、③反應制得的物質均為純凈物
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式: H2O(g)=H2(g)+ ![]() O2(g);△H=+241.8kJ/mol
O2(g);△H=+241.8kJ/mol
H2(g)+ ![]() O2(g)=H2O(l);△H=﹣285.8kJ/mol
O2(g)=H2O(l);△H=﹣285.8kJ/mol
當1g液態水變為水蒸氣時,其熱量變化是( )
A.吸熱88 kJ
B.吸熱44 kJ
C.放熱44 kJ
D.吸熱2.44 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液可能含有Na+、K+、Mg2+、Cu2+等陽離子及MnO﹣4、SiO2﹣4、AlO﹣2、CO2﹣3、HCO﹣3、SO2﹣4、Cl﹣等陰離子,已知:①該溶液呈無色②經測定溶液的pH=12③取少量溶液,加入稀鹽酸[100mL、2molL﹣1]進行酸化,有白色沉淀生成,還得到一種無色無味的氣體,該氣體使澄清石灰水(足量)變渾濁.對酸化后的溶液過濾,得到濾液甲.
(1)由①、②、③可判斷:原溶液中一定不存在的離子是 , 一定存在的離子是 .
(2)將濾液甲分成兩等份,一份中逐滴加入氨水,最終有白色膠狀沉淀,說明原溶液中一定有(填離子符號),剛開始加入氨水時,沒有沉淀產生,原因是 . (用離子方程式表示);另一份中加入足量的Ba(NO3)2溶液,有白色沉淀生成,說明原溶液中一定有(填離子符號),過濾得到濾液乙.
(3)往濾液乙中加入足量的AgNO3溶液,過濾、洗滌、干燥得固體26.5g,則原溶液中是否有Cl﹣(填“是”或“否”).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴單質具有廣泛的工業價值,查閱資料知:Br2的沸點為59℃,微溶于水,有毒性.某化學小組模擬工業流程從濃縮的海水中提取液溴,主要實驗裝置(夾持裝置略去)及操作步驟如下: 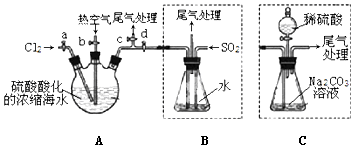
①連接A與B,關閉活塞b、d,打開活塞a、c,向A中緩慢通入Cl2至反應結束;
②關閉a、c,打開b、d,向A中鼓入足量熱空氣;
③進行步驟②的同時,向B中通入足量SO2;
④關閉b,打開a,再通過A向B中緩慢通入足量Cl2;
⑤將B中所得液體進行蒸餾,收集液溴.
請回答:
(1)判斷步驟①中反應已經結束的最簡單方法為 .
(2)步驟②中鼓入熱空氣的作用為; 步驟③B中發生的主要反應的離子方程式為 .
(3)綜合分析步驟①、②、③和④,這四步操作的最終目的為 .
(4)此實驗中尾氣可用(填選項字母)吸收處理. a.水 b.濃硫酸 c.NaOH溶液 d.飽和NaCl溶液
(5)步驟⑤中,蒸餾用到的玻璃儀器除酒精燈、溫度計、尾接管、錐形瓶外,還有和;要達到提純溴的目的,操作中應控制的關鍵條件為 .
(6)若直接連接A與C,進行步驟①和②,充分反應后,向錐形瓶中滴加稀硫酸,再經步驟⑤,也能制得液溴.滴加稀硫酸之前,C中反應生成了NaBr、NaBrO3等,該反應的化學方程式為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】檢驗銨根離子的實驗所依據的是:①氨氣極易溶于水;②銨根離子與OH- 間發生反應產生氨氣;③NH3·H2O電離出NH4+和OH -;④石蕊在堿性條件下變為藍色。
A. ②④B. ①②③④C. ①②③D. ②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知20℃時,飽和NaCl溶液的密度為ρg/cm3 , 物質的量濃度為c mol/L,則下列說法中不正確的是( )
A.溫度低于20℃時,飽和NaCl溶液的濃度小于c mol/L
B.此溶液中NaCl的質量分數為 ![]()
C.20℃時,密度小于ρg/cm3的NaCl溶液是不飽和溶液
D.20℃時,飽和NaCl溶液的溶解度 ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】14C是C的一種放射性核素,在高層大氣中由宇宙射線產生的中子或核爆炸產生的中子轟擊14N可使它轉變為14C.下列說法正確的是
A. 14C原子最外層有6個電子B. 14C核素的中子數為8
C. 14C和14N互為同位素D. 14C16O2的質子數為46
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com