
分析 二氧化硫和氯氣在水溶液中反應生成硫酸和鹽酸,硫酸根和鋇離子反應生成硫酸鋇沉淀;二氧化硫和氨水反應生成亞硫酸銨,亞硫酸根和鋇離子反應生成亞硫酸鋇沉淀;
解答 解:二氧化硫和氨水反應生成亞硫酸銨,反應的離子方程式為:SO2+2NH3•H2O=2NH4++SO32-+H2O,亞硫酸根和鋇離子反應生成亞硫酸鋇沉淀,反應的離子方程式為:SO32-+Ba2+═BaSO3↓,離子方程式可以寫成:Ba2++2NH3•H2O+SO2=BaSO3↓+2NH4++H2O,二氧化硫和氯氣在水溶液中反應生成硫酸和鹽酸,反應的離子方程式為:SO2+Cl2+2H2O═4H++2Cl-+SO42-,硫酸根和鋇離子反應生成硫酸鋇沉淀,SO42-+Ba2+═BaSO4↓,離子方程式可以寫成:Ba2++Cl2+SO2+2H2O=BaSO4↓+4H++2Cl-,該沉淀的成分分別為BaSO3,BaSO4,
故答案為:BaSO3,BaSO4,Ba2++2NH3•H2O+SO2=BaSO3↓+2NH4++H2O,Ba2++Cl2+SO2+2H2O=BaSO4↓+4H++2Cl-;
點評 本題考查了二氧化硫的性質分析,主要是二氧化硫的還原性和酸性氧化物性質的理解應用和離子方程式書寫方法,題目較簡單.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 100℃時,pH=10的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 | |
| B. | 25℃時,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等體積混合,所得溶液的pH=7 | |
| C. | 25℃時,0.2 mol/L NaOH溶液與0.2 mol/L H2SO4恰好中和,所得溶液的pH<7 | |
| D. | 25℃時,pH=12的氨水和pH=2的H2SO4等體積混合,所得溶液的pH>7 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | KClO3和SO2溶于水后的溶液均可導電,故KClO3和SO2均為電解質 | |
| B. | CH3COOH溶液加水稀釋后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值增大 | |
| C. | 反應NH3(g)+HCl(g)=NH4Cl(s)在室溫下自發進行,則該反應的△H<0 | |
| D. | 向濃度均為0.1mol•L-1KI和NaCl混合溶液中,滴加幾滴硝酸鎳溶液,只得到AgI沉淀說明Ksp(Agl)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
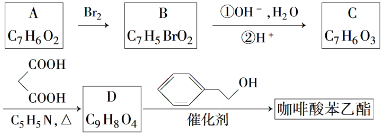
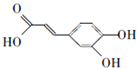 ;
;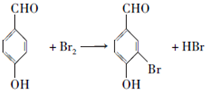 ;
;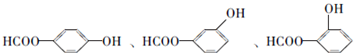 .a.屬于酯類 b.能發生銀鏡反應 c.與FeCl3溶液發生顯色反應①
.a.屬于酯類 b.能發生銀鏡反應 c.與FeCl3溶液發生顯色反應①查看答案和解析>>
科目:高中化學 來源: 題型:解答題
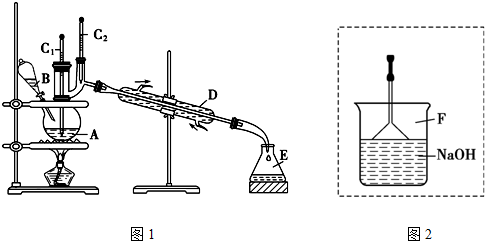
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸點/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鈉浮在水面上 | B. | 金屬鈉形成小球狀 | ||
| C. | 金屬鈉在水面上迅速游動 | D. | 反應后的溶液呈現紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 四氯化碳分子的比例模型: | B. | 如圖所示一定代表丙烯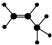 | ||
| C. | 12C32S2比12C34S2更易揮發 | D. | O${\;}_{2}^{2-}$電子式為: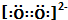 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.6 | B. | 1.6 | C. | 3.2 | D. | 3.6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com