
I.氫能的存儲是氫能應用的主要瓶頸,配位氫化物、富氫載體化合韌是目前所采用的主要儲氫材料。
(1)Ti(BH4)2是一種過渡元素硼氫化物儲氫材料。在基態(tài)Ti2+中,電子占據(jù)的最高能層符號為 ,該能層具有的原子軌道數(shù)為 ;
(2)液氨是富氫物質,是氫能的理想載體,利用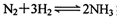 實現(xiàn)儲氫和輸氫。下列說法正確的是
;
實現(xiàn)儲氫和輸氫。下列說法正確的是
;
a.NH3分子中氮原子的軌道雜化方式為sp2雜化
b.NH+4與PH+4、CH4、BH-4、ClO—4互為等電子體
c.相同壓強時,NH3的沸點比PH3的沸點高
d.[Cu(NH3)4]2+離子中,N原子是配位原子
(3)已知NF3與NH3的空間構型相同,但NF3不易與Cu2+形成配離子,其原因是 ;
II.氯化鈉是生活中的常用調味品,也是結構化學中研究離子晶體時常用的代表物,其晶胞結構如圖所示。
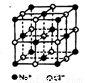
(1)設氯化鈉晶體中Na+與跟它最近鄰的Cl—之間的距離為r,則該Na+與跟它次近鄰的C1—個數(shù)為 ,該Na+與跟它次近鄰的Cl—之間的距離為 ;
(2)已知在氯化鈉晶體中Na+的半徑為以a pm,Cl—的半徑為b pm,它們在晶
體中是緊密接觸的,則在氯化鈉晶體中離子的空間利用率為 ;(用含a、b的式子袁示)
(3)納米材料的表面原子占總原子數(shù)的比例很大,這是它有許多特殊性質的原因。假設某氯化鈉顆粒形狀為立方體,邊長為氯化鈉晶胞的10倍,則該氯化鈉顆粒中表面原子占總原子數(shù)的百分比為 。
Ⅰ.(1)M(1分) 9(2分)
(2)cd(2分)
(3)N、F、H三種元素的電負性為F > N >H,在NF3中,共用電子對偏向F,偏離N原子,使得氮原子上的孤電子對難于與Cu2+形成配位鍵(2分)
Ⅱ.(1)8(2分)
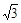 r(2分)
r(2分)
(2)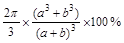 (2分)
(2分)
(3)26% 或 (2分)
(2分)
【解析】
試題分析:Ⅰ.(1)Ti原子核外有22個電子,其基態(tài)原子的核外電子排布式為1s22s22p63s23p63d24s2,在基態(tài)Ti2+中,核外電子排布式為1s22s22p63s23p63d2,對應能層分別別為K、L、M,其中能量最高的是最外層M層,該能層有s、p、d三個能級,s能級有1個軌道,p能級有3個軌道,d能級有5個軌道,所以共有9個原子軌道。
(2)a.NH3分子中N原子含有3個共用電子對和一個孤電子對,所以其價層電子對是4,采用sp3雜化,故錯誤。
b.等電子體是指具有相同電子數(shù)目和原子數(shù)目的分子或離子,NH4+與PH4+、CH4、BH4-、ClO4—原子數(shù)目相同,電子數(shù)目不同,所以不能互為等電子體,故錯誤。
c.相同壓強時,氨氣中含有氫鍵,PH3中不含氫鍵,所以NH3沸點比PH3高,故正確;
d..[Cu(NH3)4]2+離子中,N原子提供孤電子對,所以N原子是配位原子,故正確。
所以選cd 。
(3)N、F、H三種元素的電負性:F>N>H,所以NH3中共用電子對偏向N,而在NF3中,共用電子對偏向F,偏離N原子,故答案為:F的電負性比N大,N-F成鍵電子對向F偏移,導致NF3中N原子核對其孤對電子的吸引能力增強,難以形成配位鍵,故NF3不易與Cu2+形成配離子(或者N、F、H三種元素的電負性:F>N>H,在NF3中,共用電子對偏向F,偏離N原子使得氮原子上的孤對電子難于與Cu2+形成配位鍵.);
Ⅱ.(1)氯化鈉晶體中,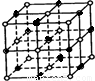 ,從圖中可以看出,鈉離子在體心和棱心位置,氯離子在頂點和面心位置,Na+與跟它次近鄰的C1—(也就是圖中晶胞大立方體中的8個頂點小白圈 )個數(shù)為8個,該Na+與跟它次近鄰的Cl—之間的距離也就是邊長為r的小立方體的體對角線,也就是
,從圖中可以看出,鈉離子在體心和棱心位置,氯離子在頂點和面心位置,Na+與跟它次近鄰的C1—(也就是圖中晶胞大立方體中的8個頂點小白圈 )個數(shù)為8個,該Na+與跟它次近鄰的Cl—之間的距離也就是邊長為r的小立方體的體對角線,也就是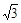 r 。
r 。
(2)晶胞為面心立方,一個氯化鈉晶胞中有4個Na+和Cl-,這個正方體的邊長是2(a+b)pm,體積是8(a+b)3pm3,一個Na+體積是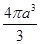 pm3,一個Cl-體積是
pm3,一個Cl-體積是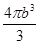 pm3,4個Na+和Cl-體積是
pm3,4個Na+和Cl-體積是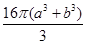 pm3,氯化鈉晶體中離子的空間利用率為
pm3,氯化鈉晶體中離子的空間利用率為 ×100%=
×100%=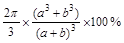 。
。
(3)由NaCl的晶胞圖可知,NaCl的晶胞為正立方體結構,立方體的體心只有一個Na+,而其它的離子都處在立方體的面上,邊長為氯化鈉晶胞邊長的10倍的氯化鈉顆粒中總原子數(shù)為21的立方,而其內部的總原子數(shù)為19的立方(立方體相對的兩個面上各被剝去了一層原子,所以整個邊長相當于是減少了2,所以是19),所以該氯化鈉顆粒中表面原子占總原子數(shù)的百分比為 =26%,另外列一種比較直觀明了的解法: 由于立方體中的總原子數(shù)為n3(n為棱上原子數(shù)) 因此邊長為氯化鈉晶胞邊長的10倍的氯化鈉顆粒中總原子數(shù)為213,而其內部的總原子數(shù)為193(相當于將外面剝掉一層),所以其表面的原子數(shù)為213-193。表面原子占總原子數(shù)的百分數(shù):
=26%,另外列一種比較直觀明了的解法: 由于立方體中的總原子數(shù)為n3(n為棱上原子數(shù)) 因此邊長為氯化鈉晶胞邊長的10倍的氯化鈉顆粒中總原子數(shù)為213,而其內部的總原子數(shù)為193(相當于將外面剝掉一層),所以其表面的原子數(shù)為213-193。表面原子占總原子數(shù)的百分數(shù):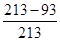 =26%。
=26%。
考點:考查物質結構。


 閱讀快車系列答案
閱讀快車系列答案湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com