
【題目】下列關于生物體內化合物的說法不正確的是( )
A. 脂肪是既能儲能又具有保溫作用的物質
B. 蛋白質是控制細胞生命活動的大分子
C. 無機鹽離子可以維持內環境的滲透壓
D. 核酸承擔了遺傳信息貯存和傳遞的任務
科目:高中化學 來源: 題型:
【題目】下列有關電池的說法不正確的是( )
A.手機上用的鋰離子電池屬于二次電池
B.鐵件上鍍銅,鍍件連接電源的正極,用含Cu2+的鹽溶液作電解質溶液
C.甲醇燃料電池可把化學能轉化為電能
D.鋅錳干電池中,鋅電極是負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃下,稀釋HA、HB兩種酸溶液,濃液pH變化的曲線如圖3所示,其中V1表示稀釋前酸的體積,V2表示稀釋后溶液的體積,下列說法不正確的是
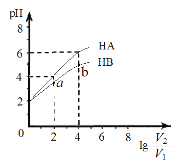
A. a、b兩點水的電離程度a小于b
B. HA、HB兩種酸溶液pH相同時,c(HA)
C. 曲線上a、b兩點![]() 一定相等
一定相等
D. 25℃時,NaA溶液中c(A-)一定大于NaB溶液中c(B-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】要從乙酸的乙醇溶液中回收乙酸,合理的操作組合是( ) ①蒸餾 ②過濾 ③靜置分液 ④加足量鈉 ⑤加入足量H2SO4 ⑥加入足量NaOH溶液 ⑦加入乙酸與濃H2SO4混合液后加熱 ⑧加入濃溴水.
A.⑦③
B.⑧⑤②
C.⑥①⑤②
D.⑥①⑤①
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是原電池的裝置圖(![]() 為電流表)。請回答:
為電流表)。請回答:
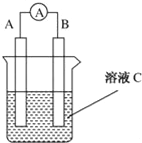
(1)若C為稀H2SO4溶液,電流表指針發生偏轉,B電極材料為Fe且做負極,則A電極上發生的電極反應式為____________;
(2)若C為CuSO4溶液,A電極材料為Zn,B電極材料為石墨,電流表指針發生偏轉,此時B為______極,反應一段時間后B電極上能夠觀察到的現象是______________________;
(3)若C為NaOH溶液,A電極材料為Al,B電極材料為Mg,負極上發生的電極反式為___________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知298K時,某堿MOH的電離平衡常數Kb=1.0×10-5;電離度a=![]() 。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L鹽酸,測得溶液的pH、溫度與所加鹽酸的體積的關系如圖所示。下列說法不正確的是
。在20.00mL0.1000mol/LMOH溶液中滴加0.10mol/L鹽酸,測得溶液的pH、溫度與所加鹽酸的體積的關系如圖所示。下列說法不正確的是
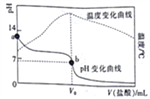
A. a點對應的溶液中:c(OH-)=(M+)+<(H+)
B. b點對應的V。=20.00mL
C. 298K時,0.1000mol/LMOH溶液中,MOH的電離度a=1%
D. 298K時,將0.1molMOH和0.1moMCl溶于水配制成1L混合溶液,溶液的pH>9
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣主要的危害是形成光化學煙霧,危害人類健康.HNCO可用于消除汽車尾氣中的NO和NO2 , 其反應原理為:HNCO+NOx→N2+CO2+H2O,下列說法正確的是( )
A.CO2分子中既含有極性鍵又含有非極性鍵
B.4.3g HNCO中含有0.1NA個原子
C.反應中NOx是還原劑
D.若NOx中x=2,1mol NO2在反應中轉移4NA個電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在A1C13和MgCl2的混合溶液中,逐滴加入NaOH溶液直至過量,經測定,加入NaOH的體積和所得沉淀的物質的量的關系如圖所示(b處NaOH的體積為l L)
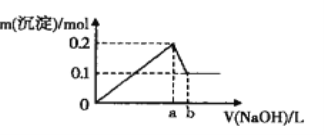
則下列判斷正確的是
A. 圖中線段oa:ab=3:l B. NaOH溶液物質的量濃度為0.6 mol·L-1
C. 在b點處溶液中的溶質只有NaAlO2 D. 混合溶液中Al3+與Mg2+物質的量比值為2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一)十氫萘是具有高儲氫密度的氫能載體,經歷“十氫萘(C10H18)→四氫萘(C10H12)→萘(C10H8)”的脫氫過程釋放氫氣。已知:ΔH1>ΔH2>0
C10H18(l)![]() C10H12(l)+3H2(g) ΔH1
C10H12(l)+3H2(g) ΔH1
C10H12(l)![]() C10H8(l)+2H2(g) ΔH2
C10H8(l)+2H2(g) ΔH2
請回答:
(1)則C10H8(l)+5H2(g)![]() C10H18(l) ΔH3=___________。
C10H18(l) ΔH3=___________。
(2)有利于提高上述反應平衡轉化率的條件是:___________。
A.高溫高壓 B.低溫低壓 C.高溫低壓 D.低溫高壓
(3)研究表明,將適量十氫萘置于恒容密閉反應器中,升高溫度帶來高壓,該條件下也可顯著釋氫,理由是:_______________________________。
(4)溫度335℃時,在恒容密閉反應器中進行高壓液態十氫萘(1.00mol)催化脫氫實驗,測得C10H12和C10H8的產率x1和x2(以物質的量分數計)隨時間的變化關系,如下圖所示。
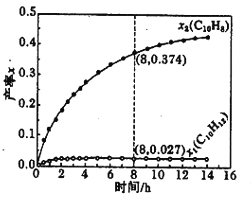
在8h時,反應體系內氫氣的量為:_________ mol(忽略其他副反應)。
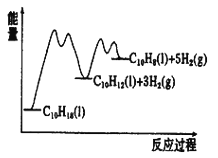
②已知反應過程中的能量變化如圖所示,x1顯著低于x2的原因是:_________________________。
(二)科學家發現,以H2O和N2為原料,熔融NaOH—KOH為電解質,納米Fe2O3作催化劑,在250℃和常壓下可實現電化學合成氨。
(5)陰極區發生的變化可視為按兩步進行。先發生的電極反應式為:________________________,隨后發生反應:2Fe+3H2O+N2==2NH3+Fe2O3。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com