
| A. | Y元素最高價氧化物對應水化物的化學式為H2YO4 | |
| B. | X與W可以形成W2X、W2X2兩種化合物 | |
| C. | Z的氫化物的沸點比X的氫化物的沸點高 | |
| D. | Y、Z兩元素的簡單離子的半徑Y>Z |
分析 X、Y、Z、W為四種短周期元素.X原子最外層電子數是核外電子層數的3倍,原子只能有2個電子層,最外層電子數為6,則X為O元素;X、Z同主族,則Z為S元素;Y、Z同周期,Y的最高正價與最低負價的代數和為6,則Y的最高價為+7價,所以Y為Cl元素;W與X、Y既不同主族也不同周期,則W為H元素,據此解答.
解答 解:X、Y、Z、W為四種短周期元素.X原子最外層電子數是核外電子層數的3倍,原子只能有2個電子層,最外層電子數為6,則X為O元素;X、Z同主族,則Z為S元素;Y、Z同周期,Y的最高正價與最低負價的代數和為6,則Y的最高價為+7價,所以Y為Cl元素;W與X、Y既不同主族也不同周期,則W為H元素.
A.Y為Cl元素,最高價氧化物對應水化物的化學式為HClO4,故A錯誤;
B.X與W可以形成H2O、H2O2兩種化合物,故B正確;
C.Z的氫化物為H2S,X的氫化物為H2O,H2O分子之間存在氫鍵,沸點高于H2S,故C錯誤;
D.Y、Z兩元素的簡單離子分別為Cl-、S2-,電子層結構相同,核電荷數越大離子半徑越小,故離子半徑:Cl-<S2-,故D錯誤,
故選:B.
點評 本題考查位置結構性質的相互關系應用,推斷元素是解題關鍵,題目難度不大,有利于基礎知識的鞏固.


 南大教輔搶先起跑暑假銜接教程南京大學出版社系列答案
南大教輔搶先起跑暑假銜接教程南京大學出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①⑤ | B. | ①③④ | C. | ②④⑥ | D. | ⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ②④⑥ | C. | ①②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HClO的電子式: | |
| B. | 中子數為20的氯原子:1720Cl | |
| C. | CCl4的電子式: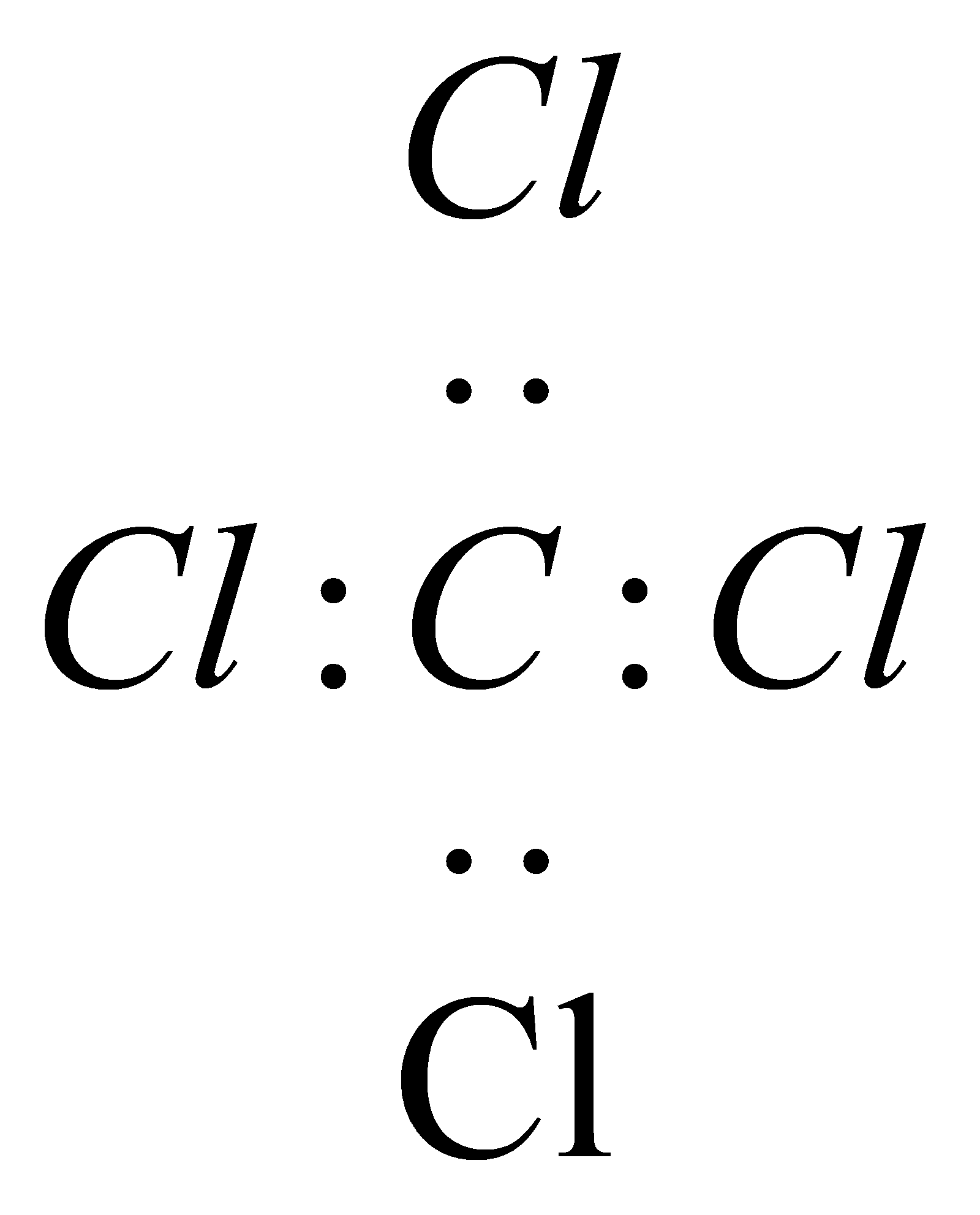 | |
| D. | Cl-的結構示意圖: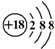 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硅的單質都可用作半導體材料 | B. | 石英可用來制造光導纖維 | ||
| C. | 碳化硅可用作砂紙、砂輪的磨料 | D. | 水玻璃可作黏合劑及耐火材料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com